-
氢气是一种新型的绿色能源,又是一种重要的化工原料.
(1)氢气燃烧热值高.实验测得,在常温常压下,1g H2完全燃烧生成液态水,放出142.9kJ热量.则H2燃烧的热化学方程式为______.
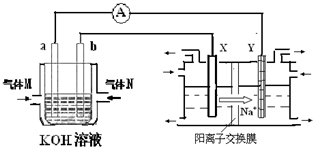
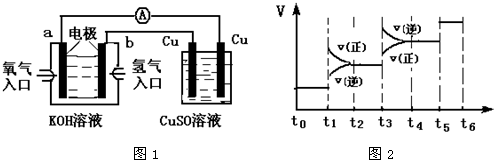
(2)氢氧燃料电池能量转化率高,具有广阔的发展前景.现用氢氧燃料电池进行如图1所示实验:
①氢氧燃料电池中,正极的电极反应式为______.
②如图1装置中,某一铜电极的质量减轻3.2g,则a极上消耗的O2在标准状况下的体积为______L.
(3)氢气是合成氨的重要原料,合成氨反应的热化学方程式如下:N2(g)+3H2(g)⇌2NH3(g)△H=-92.4kJ/mol.
①当合成氨反应达到平衡后,改变某一外界条件(不改变N2、H2和NH3的量),反应速率与时间的关系如图2所示.图中t1时引起平衡移动的条件可能是______.其中表示平衡混合物中NH3的含量最高的一段时间是______.
②温度为T℃时,将2a mol H2和a mol N2放入0.5L密闭容器中,充分反应后测得N2的转化率为50%.则反应的平衡常数为______.
-
(12分)氢气是一种新型的绿色能源,又是一种重要的化工原料。
(1)氢气燃烧热值高,实验测得,在常温常压下, 1 g H2完全燃烧生成液态水,放出
142.9 kJ热量,则H2燃烧的热化学方程式为__________________________________。
(2)氢氧燃料电池能量转化率高,具有广阔的发展前景。现将氢氧燃料电池进行下图所示实验:①氢氧燃料电池中,负极的电极反应式为__________________, ②如图实验装置中,某一铜电极的质量减轻3.2 g,则 a极上消耗的O2在标准状况下的体积____________L。
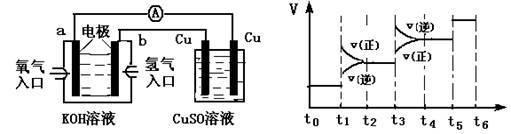
(3)氢气是合成氨的重要原料,合成氨反应的热化学方程式如下:
N2(g)+3H2(g)  2NH3(g);ΔH=-92.4 kJ/mol,
2NH3(g);ΔH=-92.4 kJ/mol,
①当合成氨反应达到平衡后,改变某一外界条件(不改变N2、H2和NH3的量),反应速率与时间的关系如图所示: 图中t1时引起平衡移动的条件可能是_________________,其中表示平衡混合物中NH3的含量最高的一段时间是____________。
②温度为T ℃时,将2 a mol H2和a mol N2放入0.5 L密闭容器中,充分反应后测得N2的转化率为50% ,则反应的平衡常数为____________。
-
氢气是一种新型的绿色能源,又是一种重要的化工原料.
(1)氢气燃烧热值高.实验测得,在常温常压下,1g H2完全燃烧生成液态水,放出142.9kJ热量.则H2燃烧的热化学方程式为______.
(2)氢氧燃料电池能量转化率高,具有广阔的发展前景.现氢氧燃料电池进行图1所示实验: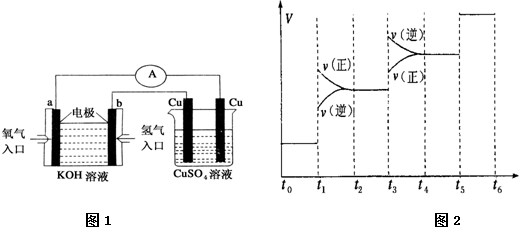
①氢氧燃料电池中,正极的电极反应式为______;
②右图装置中,某一铜电极的质量减轻3.2g,则a极上消耗的O2在标准状况下的体积为______L.
(3)氢气是合成氨的重要原料,合成氨反应的热化方程式如下:N2(g)+3H2(g)⇌2NH3(g);△H=-92.4kJ/mol
①当合成氨反应达到平衡后,改变某一外界条件(不改变N2、H2和NH3的量),反应速率与时间的关系如图2所示.图2中t1时引起平衡移动的条件可能是______,其中表示平衡混合物中NH3的含量最高的一段时间是______,若t-t1,t1-t3,t3-t5这三段平衡常数分别用K1,K2,K3表示,那么K1,K2,K3的大小关系是______.
②若在恒温、恒压条件下向平衡体系中通入氩气,平衡______移动(填“向左”、“向右”或“不”);使用催化剂反应的△H______(填“增大”、“减小”或“不改变”).
温度为T℃时,将2a mol H2和 a mol N2放入0.5L密闭容器中,充分反应后测得N2的转化率为50%.则反应的平衡常数为______.
-
氢气是一种新型的绿色能源,又是一种重要的化工原料.
(1)氢气燃烧热值高.实验测得,在常温常压下,1g H2完全燃烧生成液态水,放出142.9kJ热量.则H2燃烧的热化学方程式为________.
(2)氢气是合成氨的重要原料,合成氨反应的热化方程式如下:
N2(g)+3H2(g)⇌2NH3(g);△H=-92.4kJ/mol
①当合成氨反应达到平衡后,改变某一外界条件(不改变N2、H2和NH3的量),反应速率与时间的关系如图所示.
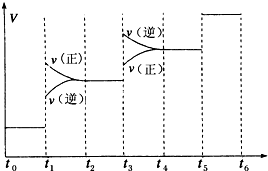
图中t1时引起平衡移动的条件可能是________其中表示平衡混合物中NH3的含量最高的一段时间是________
②温度为T℃时,将2a mol H2和a mol N2放入0.5L密闭容器中,充分反应后测得N2的转化率为50%.则反应的平衡常数为________.
-
本题为《化学反应原理(选修4)》模块选做题,
(1)氢气是一种新型的绿色能源,又是一种重要的化工原料。
①氢气燃烧热值高。实验测得,在常温常压下,1molH2完全燃烧生成液态水,放出285.8kJ热量。则表示H2燃烧热的热化学方程式是( )
A.H2(g) +1/2 O2(g)=H2O(g) ΔH =+285.8 kJ/mol
B.H2 (g) +1/2 O2(g)=H2O(l) ΔH =-285.8 kJ/mol
C.H2(g) +1/2 O2(g)=H2O(l) ΔH =+285.8 kJ/mol
D.H2 +1/2 O2 =H2O ΔH =-285.8 kJ/mol
②氢氧燃料电池能量转化率高,具有广阔的发展前景。氢氧燃料电池中,发生还原反应的物质是 (填“氢气”或“氧气”)。
③氢气是合成氨的重要原料,合成氨反应的热化学方程式如下:N2(g)+3H2(g)  2NH3(g) ΔH=-92.4 kJ/mol ,反应达到平衡后,升高温度则反应速率 (填“增大”或“减小”);平衡将向 (填“正反应方向”或“逆反应方向”)移动。
2NH3(g) ΔH=-92.4 kJ/mol ,反应达到平衡后,升高温度则反应速率 (填“增大”或“减小”);平衡将向 (填“正反应方向”或“逆反应方向”)移动。
(2)锌银电池能量大、电压平稳,广泛用于电子手表、照相机、计算器和其他微型电子仪器。电解质溶液是KOH溶液,电池总反应为Zn+Ag2O=ZnO+2Ag。请回答下列问题:
①该电池的负极材料是 ;电池工作时,阳离子向 (填“正极”或“负极”)移动;
②电极材料锌可由闪锌矿在空气中煅烧成氧化锌,然后用碳还原氧化锌来制取,该反应的化学方程式为 ZnO+C Zn+CO↑,此法属 (填选项字母代号)。
Zn+CO↑,此法属 (填选项字母代号)。
A.电解法 B.热还原法 C.热分解法
(3)今有常温下两种溶液:(A)0.1mol/L的NaCl溶液 (B) 0.1mol/LNH4Cl溶液
①溶液(A)的pH 7(填“>”、“<”或“=”);
②溶液(B)呈 性(填“酸”、“碱”或“中”),升高温度可以 (填“促进”或“抑制”)NH4Cl的水解。
-
氢气是一种新型的绿色能源,又是一种重要的化工原料。
(1)氢气燃烧热值高。实验测得,在常温常压下,1 g H2完全燃烧生成液态水,放出142.9 kJ热量。则H2燃烧热的化学方程式为 ________。
(2)氢气是合成氨的重要原料,合成氨反应的热化方程式如下:N2(g)+3H2(g) 2NH3(g);ΔH=-92.4 kJ/mol
2NH3(g);ΔH=-92.4 kJ/mol
①当合成氨反应达到平衡后,改变某一外界条件(不改变N2、H2和NH3的量),反应速率与时间的关系如下图所示。图中t1时引起平衡移动的条件可能是________其中表示平衡混合物中NH3的含量最高的一段时间是________

②温度为T ℃时,将2 a mol H2和a mol N2放入0.5 L密闭容器中,充分反应后测得N2的转化率为50%。则反应的平衡常数为________
-
氢气是一种新型的绿色能源,又是一种重要的化工原料.
(1)氢气燃烧热值高.实验测得常温常压下,1g H2完全燃烧生成液态水,放出142.9kJ热量,则表示H2的标准燃烧热的热化学方程式为:______.
(2)氢氧燃料电池能量转化率高,具有广阔的发展前景.用氢氧燃料电池进行下图所示实验(其中下图中电极均为惰性电极):该氢氧燃料电池中,b极的电极反应式为______;d极的电极反应式为______;若标准状况下氧气消耗为5.6L,则导线中转移的电子的物质的量为______.
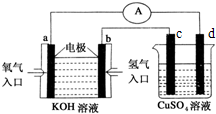
-
氢气是一种新型的绿色能源,又是一种重要的化工原料。
(1)氢气燃烧热值高。实验测得,在常温常压下,1 g H2完全燃烧生成液态水,放出142.9 kJ热量。则H2燃烧的热化学方程式为__________________________________。
(2)氢氧燃料电池能量转化率高,具有广阔的发展前景。现氢氧燃料电池进行下图所示实验:①氢氧燃料电池中,正极的电极反应式为_____ _。

②如图装置中,某一铜电极的质量减轻3.2 g,则a极上消耗的O2在标准状况下的体积为____________L
(3)氢气是合成氨的重要原料,合成氨反应的热化方程式如下:N2(g)+3H2(g) 2NH3(g);ΔH=-92.4 kJ/mol①当合成氨反应达到平衡后,改变某一外界条件(不改变N2、H2和NH3的量),
2NH3(g);ΔH=-92.4 kJ/mol①当合成氨反应达到平衡后,改变某一外界条件(不改变N2、H2和NH3的量),
反应速率与时间的关系如下图所示。

图中t1时引起平衡移动的条件可能是__________其中表示平衡混合物中NH3的含量最高的一段时间是_____
②温度为T ℃时,将2 a mol H2和a mol N2放入0.5 L密闭容器中,充分反应
后测得N2的转化率为50%。则反应的平衡常数为____________。
-
氢气是一种新型的绿色能源,又是一种重要的化工原料。
(1)氢气燃烧热值高。实验测得,在常温常压下1gH2完全燃烧生成液态水,放出142.9kJ热量。则表示H2燃烧热的热化学方程式为___________ 。
又已知:N2(g)+3H2(g) 2NH3(g) ΔH=-92.4kJ/mol,则氨在空气中燃烧生成液态水和氮气时的热化学方程式为 。
2NH3(g) ΔH=-92.4kJ/mol,则氨在空气中燃烧生成液态水和氮气时的热化学方程式为 。
(2)氢气是合成氨的重要原料。
①当合成氨反应达到平衡后,改变某一外界条件(不改变 N2、H2和NH3的量),反应速率与时间的关系如下图一所示。
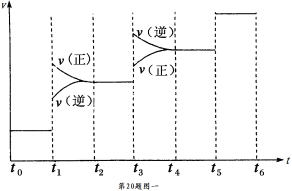
图中t1时引起平衡移动的条件可能是 ,其中表示平衡混合物中NH3的含量最高的一段时间
是 。
②温度为T℃时,将2a molH2和a molN2放入0.5L密闭容器中,充分反应后测得N2的转化率为50%。则反应
的平衡常数为 。
③氨催化氧化可以制硝酸,此过程中涉及氮氧化物,如NO、NO2、N2O4等。对于反应:N2O4(g) 2NO2(g) △H﹥0,在温度为T1、T2时,平衡体系中NO2的体积
2NO2(g) △H﹥0,在温度为T1、T2时,平衡体系中NO2的体积
分数随压强变化曲线如下图二所示。
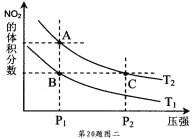
下列说法正确的是 。
a.A、C两点的反应速率:A﹤C
b.A、C两点的气体颜色:A浅,C深
c.B、C两点的气体平均相对分子质量:B﹤C
d.A、C两点的化学平衡常数:A﹥C
e.由状态B到状态A,可以用加热的方法
-
化学在能源开发与利用中起到十分关键的作用.氢气是一种新型的绿色能源,又是一种重要的化工原料.
Ⅰ(1)在298K、101kPa时,2g H2完全燃烧生成液态水,放出285.8kJ热量.则表示氢气燃烧热的热化学方程式为:______.
氢氧燃料电池能量转化率高,具有广阔的发展前景.现用氢氧燃料电池进行下图饱和食盐水电解实验(图中所用电极均为惰性电极).分析该装置、回答下列问题:
(2)氢氧燃料电池中,a电极为电池的是______(填“正极”或“负极”),气体M的分子式______,a电极上发生的电极反应式为:______.
(3)若右上图装置中盛有100mL5.0mol/LNaCl溶液,电解一段时间后须加入10.0mol/L盐酸溶液50mL(密度为1.02g/mL)才能使溶液恢复至原来状态.则在此电解过程中导线上转移的电子数为______mol.(保留小数点后2位)
Ⅱ氢气是合成氨的重要原料.工业上合成氨的反应是:
N2(g)+3H2(g)⇌2NH3 (g)△H=-92.2kJ•mol-1
(4)下列事实中,不能说明上述可逆反应已经达到平衡的是______.
①N2、H2、NH3的体积分数不再改变;
②单位时间内生成2n mol NH3的同时生成3n mol H2;
③单位时间内生成3n mol N-H键的同时生成n mol N≡N;
④用N2、H2、NH3的物质的量浓度变化表示的反应速率之比为1:3:2;
⑤混合气体的平均摩尔质量不再改变;
⑥混合气体的总物质的量不再改变.
(5)已知合成氨反应在某温度下2.00L的密闭容器中反应,测得如下数据:
| 物质的量/(mol)/时间(h) | | 1 | 2 | 3 | 4 |
| N2 | 1.50 | n1 | 1.20 | n3 | 1.00 |
| H2 | 4.50 | 4.20 | 3.60 | n4 | 3.00 |
| NH3 | 0.00 | 0.20 | n2 | 1.00 | 1.00 |
根据表中数据计算:
①反应进行到2小时时放出的热量为______kJ.
②0~1小时内N2的平均反应速率______mol•L-1•h-1.
③此条件下该反应的化学平衡常数K═______(保留两位小数).
④反应达到平衡后,若往平衡体系中再加入N2、H2 和NH3各1mol,化学平衡向______方向移动(填“正反应”或“逆反应”或“不移动”.)