A.方案甲:试液
B.方案乙:试液
C.方案丙:试液
D.方案丁:试液
高二化学选择题中等难度题
高二化学选择题中等难度题
高二化学选择题中等难度题查看答案及解析
用下面的方案进行某些离子的检验,其中方案设计得最严密的是( )
A.检验试液中的:试液
无沉淀
白色沉淀
B.检验试液中的Fe2+:试液无明显现象
红色溶液
C.检验试液中的I-:试液棕黄色溶液
蓝色溶液
D.检验试液中的:试液
白色沉淀
沉淀溶解
高二化学单选题中等难度题查看答案及解析
下列有关离子(或物质)的检验及结论中,正确的是( )
A. 取少量试液于试管中,加入稀硝酸酸化的氯化钡溶液,若有白色沉淀生成,说明试液中含有SO42-
B. 某溶液中加硝酸银溶液生成白色沉淀,说明原溶液中有Cl-
C. 向某溶液中滴加NaOH溶液,加热,产生能使湿润的红色石蕊试纸变蓝的气体,说明原溶液中有NH4+
D. 向某溶液中先滴加几滴氯水,再滴入几滴KSCN溶液后变成红色,说明原溶液中有Fe3+
高二化学单选题中等难度题查看答案及解析
在检验SO42-的过程中,下列操作中正确的是:
A.先加入稀硝酸,没有产生沉淀,然后再加硝酸钡,产生白色沉淀,证明有SO42-存在
B.先加入硝酸钡,产生白色沉淀,然后再加稀硝酸,沉淀不溶解,证明有SO42-存在
C.先加入稀盐酸,没有产生沉淀,然后再加氯化钡,产生白色沉淀,证明有SO42-存在
D.先加入氯化钡,产生白色沉淀,然后再加稀盐酸,沉淀不溶解,证明有SO42-存在
【解析】】在检验SO42-时,必须首先排出其他离子的干扰,所以要先加入盐酸,若没有现象,再加入氯化钡溶液来检验。硝酸具有氧化性,因此若含有SO32-,则被氧化生成SO42-,因此无法证明原溶液中是否SO42-,因此正确的答案是C。
高二化学选择题简单题查看答案及解析
下列有关物质检验的实验结论正确的是( )
| 实验操作 | 现象 | 结论 | |
| A | 某溶液中加入氯化钡溶液 | 生成白色沉淀 | 该溶液一定含有SO42- |
| B | 某溶液中加入无色酚酞试液 | 溶液变红色 | 该溶液一定是碱溶液 |
| C | 将某溶液做焰色反应 | 焰色呈黄色 | 该溶液一定含有Na+ |
| D | 往某溶液中加入盐酸 | 产生无色气体 | 该溶液一定含有CO32- |
A.A B.B C.C D.D
高二化学单选题中等难度题查看答案及解析
下列实验设计能够成功的是( )
A.检验试液中的SO:试液无沉淀
白色沉淀
B.除去乙酸乙酯中混有的乙酸:混合液溶液分层
得上层液体
C.证明酸性条件下H2O2氧化性比I2强:NaI溶液溶液变蓝色
D.鉴定盐A的成分是FeBr3: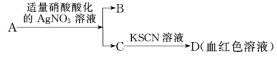
高二化学选择题简单题查看答案及解析
为了研究难溶盐的沉淀溶解平衡和沉淀转化,某同学设计如下实验。
| 步骤1:向2 mL 0.005 mol/LAgNO3溶液中加入2 mL 0.005 mol/LKSCN溶液,静置。 | 出现白色沉淀。 |
| 步骤2:取1 mL上层清液于试管中,滴加1滴2 mol/LFe(NO3)3溶液。 | 溶液变为红色。 |
| 步骤3:向步骤2的溶液中,继续加入5滴3 mol/LAgNO3溶液。 | 现象a,且溶液红色变浅。 |
| 步骤4:向步骤1余下的浊液中加入5滴3mol/L KI溶液。 | 出现黄色沉淀。 |
已知:25℃,Ksp(AgI,黄色)= 8.3×10‾17 ,Ksp (AgSCN,白色 )= 1.0×10‾12 。
回答下列问题:
(1)步骤3中现象a是________________________________。
(2)用沉淀溶解平衡原理解释步骤4的实验现象________________。
(3)向50 mL 0.005 mol/L的AgNO3溶液中加入150 mL0.005 mol/L的 KSCN溶液,若混合后溶液体积为200mL,则溶液中Ag+的浓度约为_____mol/L 。
高二化学综合题中等难度题查看答案及解析
为了研究难溶盐的沉淀溶解平衡和沉淀转化,某同学设计如下实验。
| 步骤1:向2 mL 0.005 mol/LAgNO3溶液中加入2 mL 0.005 mol/LKSCN溶液,静置。 | 出现白色沉淀。 |
| 步骤2:取1 mL上层清液于试管中,滴加1滴2 mol/LFe(NO3)3溶液。 | 溶液变为红色。 |
| 步骤3:向步骤2的溶液中,继续加入5滴3 mol/LAgNO3溶液。 | 现象a,且溶液红色变浅。 |
| 步骤4:向步骤1余下的浊液中加入5滴3mol/L KI溶液。 | 出现黄色沉淀。 |
已知:25℃,Ksp(AgI,黄色)= 8.3×10‾17 ,Ksp (AgSCN,白色 )= 1.0×10‾12 。
回答下列问题:
(1)步骤3中现象a是________________________________。
(2)用沉淀溶解平衡原理解释步骤4的实验现象________________。
(3)向50 mL 0.005 mol/L的AgNO3溶液中加入150 mL0.005 mol/L的 KSCN溶液,若混合后溶液体积为200mL,则溶液中Ag+的浓度约为_____mol/L 。
高二化学综合题中等难度题查看答案及解析
下列有关离子检验的操作和实验结论都正确的是( )
| 选项 | 实验操作及现象 | 实验结论 |
| A | 向某溶液中加入氯化钡溶液,有白色沉淀生成,再加盐酸酸化,沉淀不溶解 | 该溶液中一定含有SO42﹣ |
| B | 向某溶液中加入NaOH溶液并加热,产生能使湿润的红色石蕊试纸变蓝的气体 | 原溶液中一定含有NH4+ |
| C | 向某溶液中加入稀盐酸,产生能使澄清石灰水变浑浊的无色无味气体 | 该溶液中一定含有CO32﹣ |
| D | 用铂丝蘸取某溶液在无色火焰上灼烧直接观察火焰颜色未见紫色 | 原溶液中不含K+ |
A. A B. B C. C D. D
高二化学单选题中等难度题查看答案及解析
(10分)为除去粗盐中的Ca2+、Mg2+、Fe3+、SO42+以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):

(1)判断BaCl2已过量的方法是_________________________。
(2)第④步中,相关的离子方程式是___________;________。
(3)若先用盐酸调pH值再过滤,将对实验结果产生影响,其原因是_____________。

(4)为检验精盐纯度,需配制150 mL.0.2 mol/L NaCl(精盐)溶液,上图是该同学转移溶液的示意图,图中的错误是__________。
高二化学实验题简单题查看答案及解析