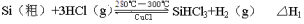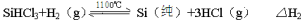-
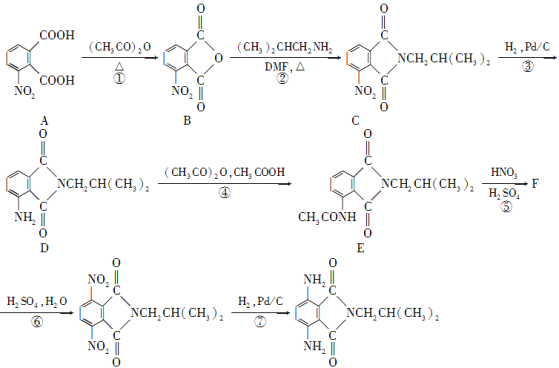
(15分)有机物H是一种新型大环芳酰胺的合成原料,可通过以下方法合成:
已知:①苯胺( )有还原性,易被氧化;
)有还原性,易被氧化;
②硝基苯直接硝化主要产物为间二硝基苯。
(1)写出A中含氧官能团的名称:________和________。
(2)写出F的结构简式:________。
(3)步骤④和步骤⑥的目的是____。
(4)写出一种符合下列条件的化合物C的同分异构体的结构简式:____。
①分子中含有2个苯环;
②能与FeCl3溶液发生显色反应;
⑧分子中有3种不同化学环境的氢原子。
(5)对苯二胺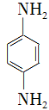 )是一种重要的染料中间体。根据已有知识并结合相关信息,写出以苯、(CH3CO)2O及CH3COOH为主要有机原料制备对苯二胺的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:
)是一种重要的染料中间体。根据已有知识并结合相关信息,写出以苯、(CH3CO)2O及CH3COOH为主要有机原料制备对苯二胺的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:

-
有机物H是一种新型大环芳酰胺的合成原料,可通过以下方法合成:
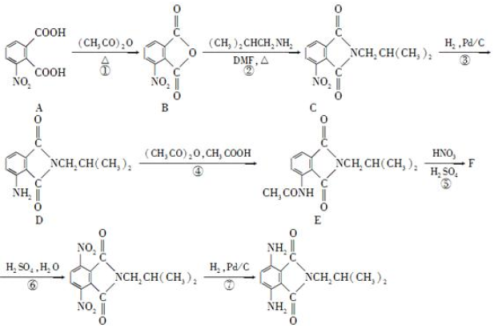
已知:①苯胺(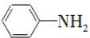 )有还原性,易被氧化;
)有还原性,易被氧化;
②硝基苯直接硝化主要产物为二硝基苯。
(1)写出A中含氧官能团的名称: 。
(2)④的反应类型为 ;F的结构简式为 。
(3)流程中设计步骤④和⑥的目的是 。
(4)写出一种符合下列条件的化合物C的同分异构体的结构简式 。
①分子中含有2个苯环;②能与FeCl3溶液发生显色反应;③分子中有3种不同化学环境的氢子。
(5)对苯二胺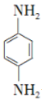 是一种重要的染料中间体。根据已有知识并结合相关信息,写出以苯、(CH3CO)2O及CH3COOH为主要有机原料制备对苯二胺的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:
是一种重要的染料中间体。根据已有知识并结合相关信息,写出以苯、(CH3CO)2O及CH3COOH为主要有机原料制备对苯二胺的合成路线流程图(无机试剂任用)。合成路线流程图示例如下: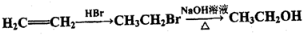
-
化合物H是合成治疗心血管疾病药物的中间体,可通过以下途径合成:

已知:①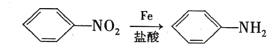 (苯胺易被氧化)
(苯胺易被氧化)
②甲苯发生一硝基取代反应与A类似。
回答下列问题:
(1)写出C中官能团的名称:___________。
(2)写出有关反应类型:B C _______;F
C _______;F G______ o
G______ o
(3)写出A B的反应方程式:___________ 。
B的反应方程式:___________ 。
(4)写出同时满足下列条件D的所有同分异构体的结构简式:_______________
①能发生银镜反应
②能发生水解反应,水解产物之一与FeCl3溶液反应显紫色
③核磁共振氢谱(1 显示分子中有4种不同化学环境的氢
显示分子中有4种不同化学环境的氢
(5)合成途径中,C转化为D的目的是___________________
(6)参照上述合成路线,以甲苯和 为原料(无机试剂任选),设计制备
为原料(无机试剂任选),设计制备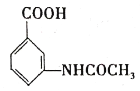 的合成路线。__________
的合成路线。__________
-
[选修5有机化学基础]
化合物A(HOCH2CH2Cl)和B[HN(CH2CH3)2]是合成药品PLKY的重要中间体.已知:硝基苯可还原成苯胺,苯胺显弱碱性,易被氧化.PLKY的合成路线如下:
(1)甲的结构简式是________,丙与B反应的反应类型是________.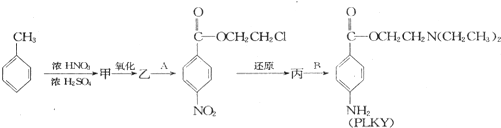
(2)乙与A反应的化学方程式是:________.
(3)PLKY有两种水解产物丁和戊.
①戊与甲互为同分异构体,戊的结构简式 是________.
②戊经聚合反应制成的髙分子纤维广泛用于通讯、宇航等领域.该聚合反应的化学方程式是________
③某有机物C的分子式为C2H4O,通过光谱分析得知分子内除C一H键、C-C键外还含有两个C一O单键,这种光谱是________光谱,C与B在一定条件下反应可生成丁,该反应的化学方程式是________.
-
阿司匹林是一种解毒镇痛药。烃A是一种有机化工原料,下图是以它为初始原料设计合成阿司匹林关系图:
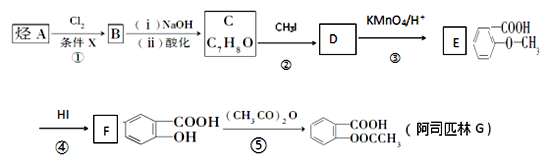
已知:(1)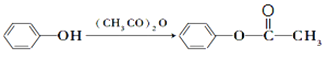
(2)烷基苯在高锰酸钾的作用下,侧链被氧化成羧基: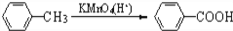
(3)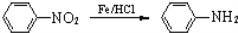 (苯胺,易被氧化)
(苯胺,易被氧化)
请根据本题所给信息与所学知识回答下列问题:
(1)C的结构简式为__________________________
(2)反应④的反应类型________,在③之前设计②这一步的目的是_____________。
(3)F中含氧官能团的名称__________________________
(4)G(阿司匹林)与足量NaOH溶液反应的化学方程式为_____________________。
(5)符合下列条件的E的同分异构体有________种。写出核磁共振氢谱中有四组峰,峰面积之比为3:2:2:1的结构简式:________________(只写一种)。
a.苯环上有两个取代基
b.遇氯化铁溶液显紫色
c.能发生水解反应
(6)利用甲苯为原料,结合以上合成路线和信息合成功能高分子材料( ,无机试剂任选)____________________
,无机试剂任选)____________________
-
(15分)芳香烃M的相对分子质量为92,是一种重要的有机黄原料,某工厂以它为初始原料设计出如下合成路线图(部分产物,反应条件省略)。其中A是一氯代物。
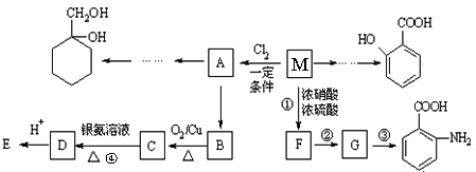
已知:Ⅰ
Ⅱ (苯胺,易被氧化)
(苯胺,易被氧化)
请根据所学知识与题中所给信息回答下列问题:
(1)M的结构简式是 ;M→A的反应条件是 。
(2)A中的共面原子最多 个。
(3)写出反应④的化学山程式 。
(4)②的反应类型属于 ;②和③的反应顺序 (填“能”或“不能”)颠倒。
(5)  有多种同分异构体,写出2种含有1个醛基和2个羟基,苯环上只能生成2种一氯取代物的芳香族化合物的结构简式: 。
有多种同分异构体,写出2种含有1个醛基和2个羟基,苯环上只能生成2种一氯取代物的芳香族化合物的结构简式: 。
(6)写出由A转化为 的合成路线(用
的合成路线(用 表示,并在箭号上写明反应试剂及反应条件)。
表示,并在箭号上写明反应试剂及反应条件)。
-
己二酸是一种重要的有机二元酸,能够发生成盐反应、酯化反应、酰胺化反应等,并能与二元胺或二元醇缩聚成高分子聚合物等,是合成尼龙-66的原料,工业上环己醇用硝酸氧化可得到己二酸,是典型的氧化还原反应。
 △H<0
△H<0
相关物理常数:
| 名称 | 相对分子质量 | 密度(20℃) g/cm3 | 熔点(℃) | 沸点(℃) | 溶解度S(g100g溶剂) |
| 水 | 乙醇 | 乙醚 |
| 环己醇 | 100 | 0.96 | 25.2 | 161 | | 可溶 | 易溶 |
| 己二酸 | 146 | 1.36 | 151 | 265 | 可溶(S随温度降低而减小) | 易溶 | 微溶 |
I.己二酸粗产品的制备
操作步骤:装置C中加入50mL中等浓度的硝酸(过量),投入沸石,并逐一安 装装置A、装置B和温度计,磁力搅拌,将溶液混合均匀,并加热到80℃。用装置A滴加2滴环己醇,反应立即开始,温度随即上升到85~90℃,从装置A中小心地逐滴加入环己醇,将混合物在85-90℃下加热2-3 分钟,共加入1.000g环己醇。
请回答下列问题:
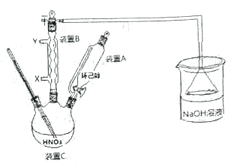
(1)反应需维持温度在85~90℃,最好采取______控温;试分析维持温度在85~90℃的原因:__________。
(2) 装置右侧烧杯中的NaOH 溶液的作用是:_______________。
II.己二酸粗产品的提纯及应用
操作流程:趁热倒出装置C 中的产品,在冷水中降温冷却,析出的晶体在布氏漏斗上进行抽滤,将晶体进行重结晶,再分别用3mL 冰水和乙醚洗涤己二酸晶体,继续抽滤,晶体再用3mL冰水洗涤一次,再抽滤。取出产品,干燥后称重,得干燥的己二酸0.860g。
请回答下列问题:
(3) 相比于普通过滤,抽滤的优点在于:_________
(4)在抽滤过程中,用冰水洗涤析出的己二酸晶体的原因:___________。
(5)该实验的产率为: _______% (结果保留3 位有效数字)
(6)工业上用己二酸与乙二醇反应形成链状高分子化合物,写出化学方程式:________。
-
已知: (苯胺,易被氧化)。甲苯是一种重要的有机化工原料,可用来合成多种重要的有机物。以甲苯为初始原料合成阿司匹林等有机物的转化关系图(部分产物、合成路线、反应条件略去)如下。
(苯胺,易被氧化)。甲苯是一种重要的有机化工原料,可用来合成多种重要的有机物。以甲苯为初始原料合成阿司匹林等有机物的转化关系图(部分产物、合成路线、反应条件略去)如下。
 请回答下列问题:
请回答下列问题:
(1)甲苯的1H核磁共振谱图中有________个特征峰。
(2)中间产物D与目标产物Y的关系是________。
(3)写出结构简式:A________,E________。
(4)写出所加试剂或反应条件:反应⑤________。
(5)写出反应③的化学方程式:
________。
(6)写出阿司匹林与足量的NaOH(aq)反应的化学方程式:
________。
-
(16分)合成喹啉及其衍生物常用的方法是Skraup合成法,以下是用苯胺、甘油、浓硫酸和硝基苯共热制备喹啉的反应流程。

(1)上图中A的名称为 ,C的分子式为
(2)II的反应类型为
(3)下列关于化合物C的说法,正确的是
A.1mol化合物C最多能与3mol氢气反应
B.可发生银镜反应
C.能使酸性高锰酸钾溶液褪色
D.属于芳香烃
(4)①化合物E和F也能发生类似II的反应,请写出生成物的结构简式。

②化合物F有多种同分异构体,其中属于醛类的有(不包括该物质本身) (写结构简式)
-
(15分)太阳能电池是利用光电效应实现能量变化的一种新型装置,目前多采用单晶硅和多晶硅作为基础材料。高纯度的晶体硅可通过以下反应获得:
反应①(合成炉):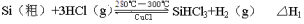
反应②(还原炉):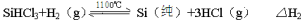
有关物质的沸点如下表所示:
| 物质 | BCl3 | PCl3 | SiCl4 | AsCl3 | AlCl3 | SiHCl3 |
| 沸点 | 12.1 | 73.5 | 57.0 | 129.4 | 180(升华) | 31.2 |
请回答以下问题:
(1)太阳能电池的能量转化方式为 ;由合成炉中得到的SiHCl3往往混有硼、磷、砷、铝等氯化物杂质,分离出SiHCl3的方法是 。
(2)对于气相反应,用某组分(B)的平衡压强(PB)代替物质的量浓度(cB)也可表示平衡常数(记作KP),则反应①的KP= ;
(3)对于反应②,在0.1Mpa下,不同温度和氢气配比(H2/SiHCl3)对SiHCl3剩余量的影响如下表所示:

①该反应的△H2 0(填“>”、“<”、“=”)
②按氢气配比5:1投入还原炉中,反应至4min时测得HCl的浓度为0.12mol·L—1,则SiHCl3在这段时间内的反应速率为 。
③对上表的数据进行分析,在温度、配比对剩余量的影响中,还原炉中的反应温度选择在1100℃,而不选择775℃,其中的一个原因是在相同配比下,温度对SiHCl3 剩余量的影响,请分析另一原因是 。
(4)对于反应②,在1100℃下,不同压强和氢气配比(H2/SiHCl3)对SiHCl3剩余量的影响如图27—1所示:

① 图中P1 P2(填“>”、“<”、“=”)
②在图27—2中画出氢气配比相同情况下,1200℃和1100℃的温度下,系统中SiHCl3剩余量随压强变化的两条变化趋势示意图。

)有还原性,易被氧化;
 )是一种重要的染料中间体。根据已有知识并结合相关信息,写出以苯、(CH3CO)2O及CH3COOH为主要有机原料制备对苯二胺的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:
)是一种重要的染料中间体。根据已有知识并结合相关信息,写出以苯、(CH3CO)2O及CH3COOH为主要有机原料制备对苯二胺的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:
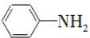 )有还原性,易被氧化;
)有还原性,易被氧化; 是一种重要的染料中间体。根据已有知识并结合相关信息,写出以苯、(CH3CO)2O及CH3COOH为主要有机原料制备对苯二胺的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:
是一种重要的染料中间体。根据已有知识并结合相关信息,写出以苯、(CH3CO)2O及CH3COOH为主要有机原料制备对苯二胺的合成路线流程图(无机试剂任用)。合成路线流程图示例如下: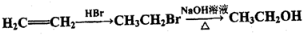

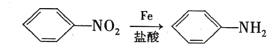 (苯胺易被氧化)
(苯胺易被氧化) 的合成路线。__________
的合成路线。__________

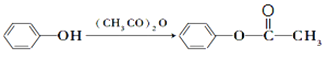
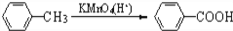
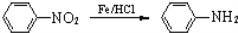 (苯胺,易被氧化)
(苯胺,易被氧化) ,无机试剂任选)____________________
,无机试剂任选)____________________
 表示,并在箭号上写明反应试剂及反应条件)。
表示,并在箭号上写明反应试剂及反应条件)。 △H<0
△H<0
 请回答下列问题:
请回答下列问题: