-
下列实验操作正确的是
A. 向过量稀硫酸中加入除去油污的废铁屑,是制备硫酸亚铁的可行方案
B. 向碳酸钠粉末中加入乙二酸溶液,生成大量气泡,说明乙二酸的酸性比碳酸强
C. 向铝屑与硫酸反应后的溶液中加入氢氧化钠溶液,是制备氢氧化铝的最佳方案
D. 在测定硫酸铜晶体中结晶水含量时,将晶体加热至完全变白色后,在空气中冷却后称量
高二化学选择题简单题查看答案及解析
-
(12分)硫酸亚铁铵[(NH4)2SO4·FeSO4·6H2O]为浅绿色晶体,实验室中常以废铁屑为原料来制备,其步骤如下:
步骤1 将废铁屑放入碳酸钠溶液中煮沸除油污,分离出液体,用水洗净铁屑。
步骤2 向处理过的铁屑中加入过量的3mol·L-1 H2SO4溶液,在60℃左右使其反应到不再产生气体,趁热过滤,得FeSO4溶液。
步骤3 向所得FeSO4溶液中加入饱和(NH4)2SO4溶液,经过“一系列操作”后得到硫酸亚铁铵晶体。
请回答下列问题:
(1)在步骤1的操作中,下列仪器中不必用到的有__________(填仪器编号)
①铁架台 ②燃烧匙 ③锥形瓶 ④广口瓶 ⑤研钵 ⑥玻璃棒 ⑦酒精灯
(2)在步骤2中趁热过滤,其原因是________________________________;
(3)在步骤3制的的硫酸亚铁铵晶体常含有Fe3+杂质。检验Fe3+的试剂可以用K4〔Fe(CN)6〕生成普鲁士蓝沉淀,有关的离子方程式是_________________________ _____。
(4)制得的晶体经过过滤后用无水乙醇洗涤而不用蒸馏水,理由是__________________;(任说两点)
(5)在25℃时,相同物质的量浓度的(NH4)2CO3、(NH4)2SO4、硫酸亚铁铵三种盐溶液a、b、c,其铵根离子浓度由小到大的排列顺序为_______________(用a、b、c回答)
高二化学实验题简单题查看答案及解析
-
硫酸亚铁铵[(NH4)2SO4·FeSO4·6H2O]为浅绿色晶体,实验室中常以废铁屑为原料来制备,其步骤如下:
步骤1:将废铁屑放入碳酸钠溶液中煮沸除油污,分离出液体,用水洗净铁屑。
步骤2:向处理过的铁屑中加入过量的3 mol·L-1 H2SO4溶液,在60℃左右使其反应到不再产生气体,趁热过滤,得FeSO4溶液。
步骤3:向所得FeSO4溶液中加入饱和(NH4)2SO4溶液,经过“一系列操作”后得到硫酸亚铁铵晶体。
请回答下列问题:
(1)在步骤1的操作中,下列仪器中不必用到的有________(填仪器编号)
①铁架台 ②燃烧匙 ③锥形瓶 ④广口瓶 ⑤研体 ⑥玻璃棒 ⑦酒精灯
(2)在步骤1中用碳酸钠溶液除去油污的化学原理是________
(3)在步骤2中所加的硫酸必须过量,其原因是__________________________________
(4)在步骤3中,“一系列操作”依次为________、________ 和过滤;
(5)本实验制备的硫酸亚铁铵晶体常含有杂质Fe3+。检验Fe3+常用的试剂是________________,可以观察到得现象是_____________________________
高二化学实验题简单题查看答案及解析
-
实验室制备少量硫酸亚铁晶体的实验步骤如下:①趁热过滤 ②洗涤、滤纸吸干 ③静置、冷却④水浴加热⑤抽滤 ⑥过量铁屑,加入20%-30%的稀硫酸溶液。则实验步骤
正确的顺序为
A. ⑥⑤④①③② B. ⑥④⑤②①③ C. ⑥④①③⑤② D. ②⑥④①③⑤
高二化学选择题简单题查看答案及解析
-
下列实验操作能达到相应目的的是
A.在3mL甲酸浓溶液中加入2滴新制氢氧化铜,加热来检验醛基
B.用加入过量氢氧化钠溶液,振荡、分液的方法除去苯中混有的苯酚杂质
C.将铁屑、溴水、苯混合以制取溴苯
D.除去乙烷中少量的乙烯的方法是:光照条件下通入Cl2,气、液分离
高二化学选择题中等难度题查看答案及解析
-
下列能用平衡移动原理解释的是
A.实验室可以用排饱和食盐水法收集氯气
B.向H2O2溶液中加入MnO2,反应速率加快
C.实验室制备氢气,用粗锌代替纯锌,反应速率加快
D.在实验室里,可用碳酸钙粉末和稀硫酸制取二氧化碳气体
高二化学选择题中等难度题查看答案及解析
-
下列实验事实的描述中,正确的是( )
A. 除去苯中的苯酚可以加入过量浓溴水后过滤
B. 向浓硫酸中缓慢加入乙醇和冰醋酸用以制备乙酸乙酯
C. 向2mL 10% NaOH溶液中,加入2mL 2mol/L CuSO4溶液,振荡制Cu(OH)2悬浊液,用于检验醛的性质
D. 加入Mg(OH)2固体可除去MgCl2溶液中混有的少量FeCl3
高二化学选择题中等难度题查看答案及解析
-
下列实验事实的描述中,正确的是( )
A. 除去苯中的苯酚可以加入过量浓溴水后过滤
B. 向浓硫酸中缓慢加入乙醇和冰醋酸用以制备乙酸乙酯
C. 将2%的NaOH溶液4至5滴,滴入2 mL10%的CuSO4溶液中制得Cu(OH)2悬浊液,加入乙醛溶液加热,用以检验醛基存在。
D. 除去MgCl2溶液中混有的少量FeCl3可加入Mg(OH)2固体
高二化学选择题中等难度题查看答案及解析
-
下列实验操作正确的是
A. 淀粉中加入20%的硫酸溶液,在酒精灯上加热,使其水解
B. 除去乙醇中的乙酸,加入NaOH溶液后分液
C. 用酸性KMnO4溶液直接检验乙醇与浓硫酸反应是否得到乙烯
D. 取少量卤代烃加入NaOH水溶液共热,冷却,再加入AgNO3溶液检验卤代烃中卤原子的存在
高二化学单选题中等难度题查看答案及解析
-
(1)硫酸亚铁晶体(FeSO4·7H2O)在医药上作补血剂,实验室通过如下实验由废铁屑制备FeSO4·7H2O晶体:
a.将5% Na2CO3溶液加入到盛有一定量废铁屑的烧杯中,加热数分钟,用倾析法除去Na2CO3
溶液,然后将废铁屑用水洗涤2~3遍;
b.向洗涤过的废铁屑中加入过量的稀硫酸,控制温度在50~80℃之间至铁屑耗尽;
c.趁热过滤,将滤液转入到密闭容器中,静置、冷却结晶;
d.待结晶完毕后,滤出晶体,用少量冰水洗涤2~3次,再用滤纸将晶体吸干;
e.将制得的FeSO4·7H2O晶体放在一个小广口瓶中,密闭保存。请回答下列问题:
①实验步骤b明显不合理,理由是 。
②实验步骤d中用少量冰水洗涤晶体,其目的是 , 。
(2)经查阅资料后发现,硫酸亚铁在不同温度下结晶可分别得到FeSO4·7H2O、FeSO4·4H2O和FeSO4·H2O。硫酸亚铁在不同温度下的溶解度和该温度下析出晶体的组成如下表所示(仅在56.7℃、64℃温度下可同时析出两种晶体)。硫酸亚铁的溶解度和析出晶体的组成
温度/℃
0
10
30
50
56.7
60
64
70
80
90
溶解度/g
14.0
17.0
25.0
33.0
35.2
35.3
35.6
33.0
30.5
27.0
析出晶体
FeSO4·7H2O
FeSO4·4H2O
FeSO4·H2O
请根据表中数据作出硫酸亚铁的溶解度曲线。
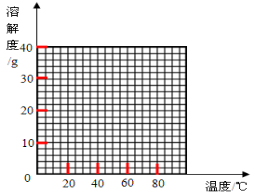
(3)若需从硫酸亚铁溶液中结晶出FeSO4·4H2O,应控制的结晶温度(t)的范围为 .
(4)硫酸亚铁晶体(FeSO4·7H2O)在医药上作补血剂。某课外小组测定该补血剂中铁元素的含量。实验步骤如下:
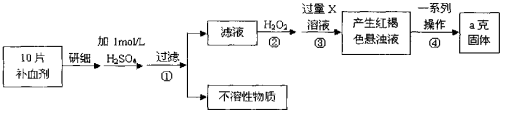
请回答下列问题:
①证明步骤①滤液中含有Fe2+的方法是先滴加KSCN溶液,再滴加 ,该过程的现象为: 。
②步骤④中一系列处理的操作步骤:过滤、 、灼烧、 、称量。
③若实验无损耗,则每片补血剂含铁元素的质量 g。
④该小组有些同学认为用酸性KMnO4溶液滴定也能进行铁元素(Fe2+)含量的测定,请写出该反应的化学方程式 。
高二化学实验题极难题查看答案及解析