-
(本题10分)工业合成氨N2+3H2 2NH3反应过程中的能量变化如图所示,据图回答下列问题:
2NH3反应过程中的能量变化如图所示,据图回答下列问题:

(1)该反应通常用活性铁作催化剂,加活性铁会使图中B点升高还是降低 ,理由是 。
(2)该反应的平衡常数表达式为:K= ,当浓度商Qc K(填“<”、“>”或“=”)时,反应向右进行。
(3)450 ℃时该反应的平衡常数 500 ℃时的平衡常数(填“<”、“>”或“=”)。
(4)一定条件下的密闭容器中,该反应达到平衡,要提高H2的转化率,可以采取的合理措施有 (填字母序号)。
a.高温高压
b.加入催化剂
c.增加N2的浓度
d.增加H2的浓度
e.分离出NH3
-
合成氨反应(N2(g)+3H2(g)⇌2NH3(g))在工业生产中的大量运用,满足了人口的急剧增长对粮食的需求,也为化工生产提供了足够的原料.按要求回答下
列问题:
(1)合成氨反应的能量变化如图所示,则该反应的热化学方式为:________.
(2)在温度恒定为298K,体积恒定为10L的密闭容器中加入氢气、氮气的物质的量分别为0.7mol、0.6mol,平衡时测得氮气的转化率为 ,则此温度下题给该反应的平衡常数K=________.
,则此温度下题给该反应的平衡常数K=________.
(3)标况下,若将22.4mL的氨气通入100mLpH为2的盐酸中,则溶液中各离子浓度的顺序由大到小为________.
(4)将氨气通入盛有CaSO4悬浊液的沉淀池中,再通入足量的CO2,过滤后即可得到(NH4)2SO4.该过程的化学方程式为________,由此可知Ksp(CaSO4)________Ksp(CaCO3)(填“大于”、“小于”或“等于”)

-
合成氨工业的核心反应是:N2(g)+3H2(g)  2NH3(g) ΔH=Q kJ·mol-1,能量变化如下图,回答下列问题:
2NH3(g) ΔH=Q kJ·mol-1,能量变化如下图,回答下列问题:

(1)在反应体系中加入催化剂,反应速率增大,E1和E2的变化是:E1________,E2________(填“增大”、“减小”或“不变”)。
(2)在500℃、2×107Pa和催化剂条件下向一密闭容器中充入0.5 mol N2和1.5 mol H2,充分反应后,放出的热量________ 46.2 kJ(填“<”、“>”或“=”)。
(3)关于该反应的下列说法中,正确的是________。
A.ΔH>0,ΔS>0 B.ΔH>0,ΔS<0
C.ΔH<0,ΔS>0 D.ΔH<0,ΔS<0
(4)将一定量的N2(g)和H2(g)放入1 L密闭容器中,在500℃、2×107Pa下达到平衡,测得N2为0.10 mol,H2为0.30 mol,NH3为0.10 mol。计算该条件下达到平衡时H2转化为NH3的转化率________。若升高温度,K值变化________(填“增大”、“减小”或“不变”)。
(5)在上述(4)反应条件的密闭容器中,欲提高合成氨中H2的转化率,下列措施可行的是________(填字母)。
A.向容器中按原比例再充入原料气
B.向容器中再充入惰性气体
C.改变反应的催化剂
D.分离出氨气
-
氮元素的氢化物和氧化物在工业生产和防建设中都有广泛的应用.请回答下列问题:
(1)氨气可由N2和H2反应制取,N2(g)+3H2(g)⇌2NH3(g)反应过程的能量变化如图所示:已知1molN2分子中的化学键断裂时需要吸收942kJ的能量;1molH2分子中的化学键断裂时需要吸收436kJ的能量;形成1molN﹣H键时释放390.8kJ的能量.
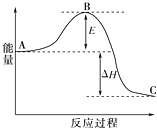
①图中E的大小对该反应热有无影响?____________________________.该反应需要用铁触媒作催化剂,加铁触媒会使图中B点升高还是降低?______________________,理由_________________.
②图中△H=___kJ/mol.
③如果反应速率v(H2)为0.15mol/(L•min),则v(N2)=_____________mol/(L•min),v(NH3)=_________________________________________.
(2)肼可作为火箭发动机的燃料,与氧化剂N2O4反应生成N2和水蒸气.
已知:N2(g)+2O2(g)=N2O4(l) △H=﹣19.5kJ•mol﹣1
N2H4(l)+O2(g)=N2(g)+2H2O(g)△H=﹣534.2kJ•mol﹣1
请写出肼和 N2O4反应的热化学反应方程式_______________________ .
-
下图为合成氨N2(g)+3H2(g) 2NH3(g)反应过程中的能量变化情况,请回答下列问题:
2NH3(g)反应过程中的能量变化情况,请回答下列问题:
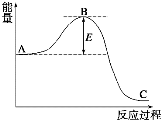
(1)反应中用活性铁作催化剂,使用活性铁会使图中B点升高还是降低________,理由是___________。
(2)该反应平衡常数为K,当浓度商Qc______K(填“<”、“>”或“=”)时,反应向右进行。
(3)400 ℃时该反应的平衡常数_______450 ℃时的平衡常数(填“<”、“>”或“=”)。
(4)一定条件下的密闭容器中,该反应达到平衡,要提高H2的转化率,可以采取的合理措施有(填字母)________。
A.高温高压
B.加入催化剂
C.增加N2的浓度
D.增加H2的浓度
E.分离出NH3
-
合成氨反应过程中的能量变化如图所示,下列说法正确的是

A.NH3的能量较低,比N2、H2更稳定
B.2NH3(g)→2N(g)+6H(g)-2346 kJ
C.N2(g)+3H2(g) 2NH3(g)-92 kJ
2NH3(g)-92 kJ
D.加入催化剂,可以减小反应的热效应
-
氮及其化合物与人类生产、生活息息相关。其中尿素(H2NCONH2) 是人类最早合成的有机物,工业上生产尿素的反应为: N2+3H2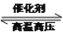 2NH3,2NH3+CO2
2NH3,2NH3+CO2 H2NCONH2+H2O。回答下列问题:
H2NCONH2+H2O。回答下列问题:
(1)纳米氧化铜、纳米氧化锌均可作合成氨的催化剂,Cu2+价层电子的轨道表达式为______,Zn位于元素周期表的_______区。
(2)C、N、O三种元素第一电离能从大到小的顺序是___________。
(3)上述化学方程式中的无机化合物,沸点由高到低的顺序是____________,原因: ___________。
(4)尿素分子中,原子杂化轨道类型有____________,σ键与π键数目之比为_______。
(5)氮化硼(BN)是一种性能优异、潜力巨大的新型材料,主要结构有立方氮化硼(如图1) 和六方氮化硼(如图2),前者类似于金刚石,后者与石墨相似。
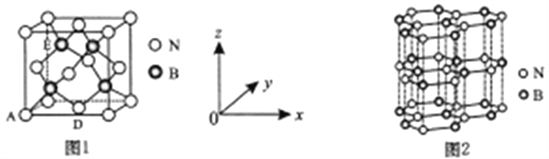
①晶胞中的原子坐标参数可表亓晶胞内部各原子的相对位置。图1中原子坐标参数A为(0,0,0),D为( ),则E原子的坐标参数为_____。X-射线衍射实验测得立方氮化硼晶胞参数为361.5pm,则立方氮化硼晶体N 与B的原子半径之和为______pm。(
),则E原子的坐标参数为_____。X-射线衍射实验测得立方氮化硼晶胞参数为361.5pm,则立方氮化硼晶体N 与B的原子半径之和为______pm。( )
)
②已知六方氮化硼同层中B-N距离为acm,密度为dg/cm3,则层与层之间距离的计算表达式为_______pm。
-
氢能是重要的新能源。储氢作为氢能利用的关键技术,是当前关注的热点之一。
(1)可逆反应N2+3H2 2NH3是工业上合成氨的重要反应
2NH3是工业上合成氨的重要反应
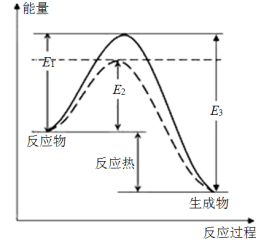
图1(图中表示生成1 mol物质时的能量)
根据图1请写出合成氨的热化学方程式:__________________(热量用E1、E2或E3表示)。
(2)LiAlH4是一种重要的储氢载体,能与水反应达到LiAlO2和氢气,该反应消耗1 mol LiAlH4时转移的电子数目为__________。
(3)氮化锂是非常有前途的储氢材料,其在氢气中加热时可得到氨基锂(LiNH2),其反应的化学方程式为:Li3N+2H2 LiNH2+2LiH,氧化产物为_________(填化学式),在270℃时,该反应可逆向发生放出H2,因而氮化锂可作为储氢材料,储存氢气最多可达Li3N质量的_____%(精确到0.1)。
LiNH2+2LiH,氧化产物为_________(填化学式),在270℃时,该反应可逆向发生放出H2,因而氮化锂可作为储氢材料,储存氢气最多可达Li3N质量的_____%(精确到0.1)。
(4)LiFePO4新型锂离子动力电池以其独特的优势成为奥运会绿色能源的新宠,已知电池放电时总反应式为FePO4+Li LiFePO4 ,电池正极反应为____________________。
LiFePO4 ,电池正极反应为____________________。
(5)一定条件下,如图所示装置可实现有机物的电化学储氢(忽略其它有机物)。
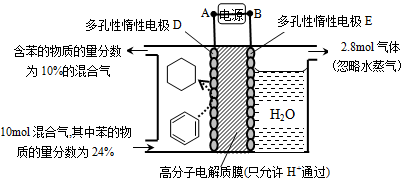
①导线中电子移动方向为____________。(用A、D表示)
②生成目标产物的电极反应式为__________________________。
③该储氢装置的电流效率 =__________________________。
=__________________________。
( =
= ×100%,计算结果保留小数点后1位)
×100%,计算结果保留小数点后1位)
-
如图所示是298 K时N2与H2反应过程中能量变化的曲线图。下列叙述正确的是( )
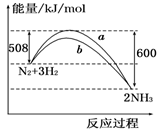
A.该反应的热化学方程式为:N2+3H2 2NH3 ΔH=-92 kJ/mol
2NH3 ΔH=-92 kJ/mol
B.a曲线是加入催化剂时的能量变化曲线
C.加入催化剂,该化学反应的反应热改变
D.在温度、体积一定的条件下,通入1 mol N2和3 mol H2反应后放出的热量为Q1 kJ,若通入2 mol N2和6 mol H2反应后放出的热量为Q2 kJ,则184>Q2>2Q1
-
合成氨反应过程中的能量变化如图所示,下列说法正确的是
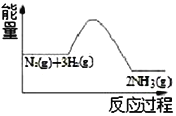
A. 反应体系中加入催化剂,会改变反应的热效应
B. 反应物的总能量低于生成物的总能量
C. 该反应的热化学方程式为3H2(g)+N2(g) 2NH3(g)+Q(Q>0)
2NH3(g)+Q(Q>0)
D. 该反应是吸热反应
2NH3反应过程中的能量变化如图所示,据图回答下列问题:






 2NH3,2NH3+CO2
2NH3,2NH3+CO2


 ×100%,计算结果保留小数点后1位)
×100%,计算结果保留小数点后1位)
