-
化学兴趣小组对某品牌牙膏中摩擦剂成分及其含量进行以下探究:
查得资料:该牙膏摩擦剂由碳酸钙、氢氧化铝组成;牙膏中其它成分遇到盐酸时无气体生成.
Ⅰ.摩擦剂中氢氧化铝的定性检验取适量牙膏样品,加水成分搅拌、过滤.
(1)往滤渣中加入过量NaOH溶液,过滤.氢氧化铝与NaOH溶液反应的离子方程式是______.
(2)往(1)所得滤液中先通入过量二氧化碳,再加入过量稀盐酸.观察到的现象是______.
Ⅱ.牙膏样品中碳酸钙的定量测定
利用如图所示装置(图中夹持仪器略去)进行实验,充分反应后,测定C中生成的BaCO3沉淀质量,以确定碳酸钙的质量分数.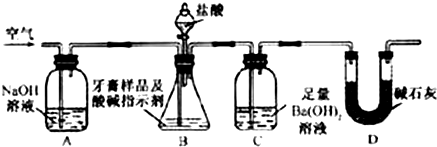
依据实验过程回答下列问题:
(3)实验过程中需持续缓缓通入空气.其作用除了可搅拌B、C中的反应物外,还有:______.
(4)下列各项措施中,不能提高测定准确度的是______(填标号).
a.在加入盐酸之前,应排净装置内的CO2气体
b.滴加盐酸不宜过快
c.在A-B之间增添盛有浓硫酸的洗气装置
d.在B-C之间增添盛有饱和碳酸氢钠溶液的洗气装置
(5)实验中准确称取8.00g样品三份,进行三次测定,测得BaCO3平均质量为3.94g.则样品中碳酸钙的质量分数为______.
-
化学兴趣小组对某品牌牙膏中摩擦剂成分及其含量进行探究:
Ⅰ.查资料:该摩擦剂由碳酸钙、氢氧化铝组成;牙膏中其它成分遇到盐酸无气体生成.
Ⅱ.牙膏样品中碳酸钙的定量测定:
利用图所示装置(图中夹持仪器略去)进行实验,测定C中生成的BaCO3沉淀质量,以确定碳酸钙的质量分数.
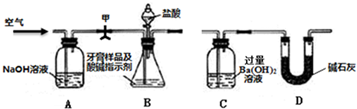
实验步骤:
①如图所示连接好装置,先检查装置的气密性;
②准确称取牙膏样品的质量4.00g,并在各仪器中加入相应试剂;
③打开弹簧夹甲,缓缓通入空气,然后接上C;
④打开B的分液漏斗滴加盐酸反应,同时再次持续缓缓通入空气;
⑤待B中不再产生气体后停止滴加盐酸;
⑥将C中沉淀过滤、洗涤、干燥,得BaCO3固体,称量BaCO3的质量为1.97g.
(1)A中放NaOH溶液的作用是______;
(2)步骤④通入空气的作用是______;
(3)步骤⑥中检验沉淀洗干净的方法是______;
(4)本实验测定得到的样品中碳酸钙的质量分数为______;
若采取下列措施,对测定结果的准确度没有影响的是______(填标号);
a.省略步骤③b.滴加盐酸快一些 c.多次实验,取平均值计算
(5)有同学认为不必测定C中生成BaCO3质量,只要测定装置C在吸收CO2前后质量差,一样可以准确测定碳酸钙质量分数.请说明是否可以并说明理由______.
-
学习小组对某品牌牙膏中摩擦剂成分及其含量进行以下探究:
查得资料: 该牙膏摩擦剂由碳酸钙、氢氧化铝组成;牙膏中其它成分遇到盐酸时无气体生成。
Ⅰ.摩擦剂中氢氧化铝的定性检验: 取适量牙膏样品,加水搅拌、过滤。
(1)往滤渣中加入过量NaOH溶液,过滤。氢氧化铝与NaOH溶液反应的离子方程式是______________。
(2)往(1)所得滤液中先通入过量二氧化碳,再加入过量稀盐酸。观察到的现象是________________。
Ⅱ.牙膏样品中碳酸钙的定量测定:利用下图所示装置(图中夹持仪器略去)进行实验,充分反应后,测定C中生成的BaCO3沉淀质量,以确定碳酸钙的质量分数。
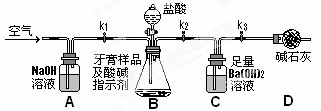
依据实验过程回答下列问题:
(3)实验过程中需持续缓缓通入空气。其作用除了可搅拌B、C中的反应物外,还有______
(4)C中反应生成BaCO3的化学方程式是__________________________
(5)下列各项措施中,不能提高测定准确度的是_________(填标号)。
A.在加入盐酸之前,应排净装置内的CO2气体;
B.滴加盐酸不宜过快;
C.在A—B之间增添盛有浓硫酸的洗气装置
D.在B—C之间增添盛有饱和碳酸氢钠溶液的洗气装置
(6)实验中准确称取8.00g样品三份,进行三次测定,测得BaCO3平均质量为3.94g 。则样品中碳酸钙的质量分数为_________。
(7)有人认为不必测定C中生成的BaCO3质量,只要测定装置C在吸收CO2前后的质量差,一样可以确定碳酸钙的质量分数。实验证明按此方法测定的结果明显偏高,原因是______________。
-
某化学兴趣小组拟通过中和滴定实验验证某品牌陈醋的酸度。
(1)查阅资料:
①食醋组成极为复杂,除水以外的主要成分是醋酸CH3COOH,此外还有其他各种有机物和一些无机物等微量成分,醋酸的含量远远多于其他成分的含量。另外其中含一些色素成分,使食醋呈棕色(白醋除外)。
②0.1 mol·L-1醋酸与氢氧化钠恰好完全反应时的pH约为________。
A.5.6 B.7.0 C.8.8 D.13.0
③包装显示该陈醋的酸度约是3.6 g/100 mL。
(2)由以上资料,同学们认为:
①测量时可以忽略老陈醋其他成分特别是有机酸所带来的影响。
②根据陈醋的特点,只能选用________来指示滴定终点。
A.甲基橙 B.酚酞 C.石蕊
③为使滴定时溶液中的醋酸浓度接近0.1 mol·L-1,应将10 mL样品醋稀释至________。
A.36 mL B.60 mL C.360 mL D.600 mL
(3)配制标准氢氧化钠溶液
由于NaOH在称量过程中极易吸水,配好的溶液浓度往往比预期偏小。故实验小组先用0.101 0 mol·L-1的KHP标准溶液准确测定NaOH溶液的浓度(KHP与NaOH按物质的量比1∶1完全反应)。向锥形瓶中盛入20.00 mL NaOH溶液时,应用________量取。
A.20 mL的量筒 B.100 mL的容量瓶 C.碱式滴定管 D.酸式滴定管
(4)用标准氢氧化钠溶液测定醋酸的浓度,并换算为酸度。
| V(NaOH) | V(KHP)平均 |
| 20.00 mL | 18.00 mL |
| V(稀释后的醋) | V(NaOH)平均 |
| 18.00 mL | 20.00 mL |
| | | |
计算得出该陈醋样品的酸度为________ g/100 mL。(计算结果保留4位有效数字)
-
发酵粉是一种化学膨松剂,可由小苏打、臭粉(碳酸氢铵)、明矾中的两种物质组成。某小组为探究不同品牌的发酵粉的化学成分,进行如下实验。
【提出假设】
(1)假设1:由小苏打和臭粉组成 假设2:由小苏打和明矾组成 假设3:由______组成
【方案与流程】
为探究甲品牌的发酵粉的成分,某同学设计如下实验,得到如下现象:
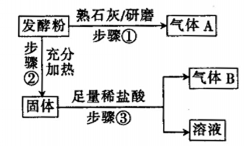
(2)结合步骤①~③分析,气体A为____________,该发酵粉的成分为__________ (填化学式)。
(3)乙品牌的发酵粉的化学组成可能为假设2情况,请你设计实验验证。
实验仪器和用品任选,限选试剂:稀盐酸、0.1mol/LnaOH溶液
写出实验步骤、预期现象和结论。
| 实验步骤 | 预期现象和结论 |
| 步骤1:取少量样品溶于足量的盐酸后,将溶液分成两份,分别装入A、B试管中。 | |
| 步骤2:________ | 焰色呈黄色证明有Na+,发酵粉中有NaHCO3 |
| 步骤3:________ | 看到有白色沉淀生成(或先产生白色沉淀后沉淀溶解),证明发酵粉中有明矾。 |
-
化学学习小组为测定某补血剂中硫酸亚铁的含量进行了以下探究:
【查阅资料】本品为糖衣片,除去糖衣后显淡蓝绿色,主要成分为FeSO4·7H2O。
【实验步骤】取本品10片,在适当的条件下配成100 mL溶液,分别准确量取20 mL溶液,用下列两种方法进行实验:
方法①:用一定物质的量浓度的酸性高锰酸钾溶液滴定。
方法②:加过量H2O2溶液,然后再加入过量NaOH溶液,得红褐色沉淀,将沉淀过滤并充分加热得红棕色固体,称量该固体的质量。
请回答下列问题:
(1)方法①中,配制100mL一定物质的量浓度的酸性高锰酸钾溶液时,所需要的玻璃仪器除量筒、玻璃棒、胶头滴管、烧杯外还有______________。
(2)方法②中,加过量H2O2溶液的目的是_____________,所得红褐色沉淀是__________(填化学式,下同),红棕色固体是__________。
(3)有同学认为可以将方法②中的H2O2换成氯气,与使用氯气相比,用H2O2溶液的好处是______________________。
(4)在方法①中,若每消耗1 mL酸性高锰酸钾溶液相当于0.152 g FeSO4,则该溶液中高锰酸钾的物质的量浓度是__________。在方法②中,若称得红棕色固体的质量为a g,则每片补血剂含FeSO4_________________g。
-
由短周期元素组成的化合物X是某抗酸药的有效成分。某同学欲探究X的组成。
查阅资料:①由短周期元素组成的抗酸药的有效成分有碳酸氢钠、碳酸镁、氢氧化铝、硅酸镁铝、磷酸铝、碱式碳酸镁铝。
②Al3+在pH=5.0时沉淀完全;Mg2+在pH=8.8时开始沉淀,在pH=11.4时沉淀完全。
实验过程:
Ⅰ.向化合物X粉末中加入过量盐酸,产生气体A,得到无色溶液。
Ⅱ.用铂丝蘸取少量Ⅰ中所得的溶液,在火焰上灼烧,无黄色火焰。
Ⅲ.向Ⅰ中所得的溶液中滴加氨水,调节pH至5~6,产生白色沉淀B,过滤。
Ⅳ.向沉淀B中加过量NaOH溶液,沉淀全部溶解。
Ⅴ.向Ⅲ中得到的滤液中滴加NaOH溶液,调节pH至12,得到白色沉淀C。
(1)Ⅰ中气体A可使澄清石灰水变浑浊,A的化学式是________。
(2)由Ⅰ、Ⅱ判断X一定不含有的元素是磷、________。
(3)Ⅲ中生成B的离子方程式是__________________________________________________。
(4)Ⅳ中B溶解的离子方程式是__________________________________________________。
(5)沉淀C的化学式是________。
(6)若上述n(A)∶n(B)∶n(C)=1∶1∶3,则X的化学式是__________________________。
-
化学家庭小实验是利用家庭日常生活用品进行化学学习和探究的活动。下列家庭小实验设计肯定不合理的是( )
A.用米汤水(含淀粉)检验食盐中是否含碘 B.用食醋检验牙膏中的摩擦剂是否是碳酸钙
C.用食用碱(Na2CO3)溶液洗涤餐具上的油污 D.用鸡蛋膜除去淀粉溶液中含有的氯化钠
-
化学家庭小实验是利用家庭日常生活用品进行化学学习和探究的活动.下列家庭小实验设计肯定不合理的是( )
A.用米汤水(含淀粉)检验食盐中是否含碘
B.用食醋检验牙膏中的摩擦剂是否是碳酸钙
C.用食用碱(Na2CO3)溶液洗涤餐具上的油污
D.用鸡蛋膜除去淀粉溶液中含有的氯化钠
-
下列有关实验的描述或操作错误的是( )
A.牙膏中含有不溶于水的成分,如碳酸钙、磷酸钙、氢氧化铝、二氧化硅等,它们主要起摩擦剂的作用
B.纸层析法通常以滤纸作为惰性支持物.滤纸纤维具有亲水性,它所吸附的水作为固定相
C.欲检验火柴头燃烧后的气体中是否含有CO2,可将气体依次通过足量NaHCO3溶液和澄清石灰水
D.减压过滤不宜用于过滤胶状沉淀或颗粒太小的沉淀



