-
(18分)硫酸铜溶液常用于农业上制波尔多液。下图是用废铜料(铁、铜混合物)来生产硫酸铜的过程,请根据图示回答下列问题。
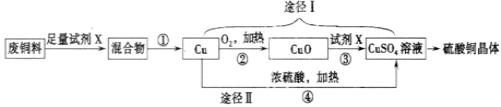
(1)试剂X的化学式为_______________,操作①的名称为_______________。
(2)甲同学认为途径Ⅰ比途径Ⅱ更为合理,其理由是_________(填编号)
a.对环境污染少 b.反应速率快
c.铜的利用率高 d.硫酸的利用率高
(3)实验室用浓硫酸与铜反应,采用下列装置制备并收集干燥的SO2气体。
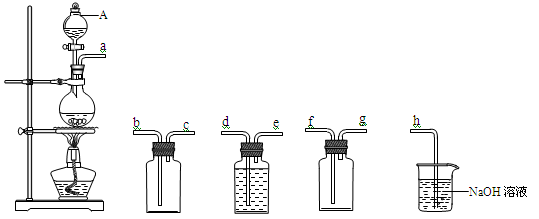
①A装置的名称_______________。
②连接上述仪器的正确顺序是(填各接口处的字母):a接______,______接______,______接______,______接h。
③反应终止后,发现烧瓶中有黑色物质出现,其中可能含有CuO、CuS等杂质。已知硫化铜不与H+反应,与足量稀硝酸反应生成Cu2+、+6价的S和NO气体,该反应的离子方程式为____________。利用所给试剂设计实验,检测黑色物质中是否存在CuS。其方案为:将烧瓶中混合物加入到蒸馏水中,充分反应后过滤,向滤渣中 _____________(补充实验操作、现象和结论)。
供选择的试剂:稀盐酸、稀硫酸、稀硝酸、氯化钡溶液、硝酸银溶液
-
氮及其化合物与工农业生产及人们的日常生活密切相关。回答下列问题:
(1)利用某废铜下脚料(主要成分是 )可制备硫酸铜晶体(蓝矾),制备方法如图所示:
)可制备硫酸铜晶体(蓝矾),制备方法如图所示:
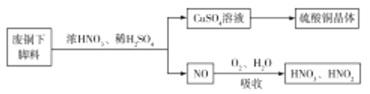
①蓝矾的化学式为:____________。
②废铜与浓硝酸,稀硫酸反应的化学方程式为______________。
(2)工业上制备尿素的反应是: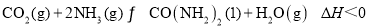 。一定温度下,在容积为
。一定温度下,在容积为 的恒溶液密闭容器中加入
的恒溶液密闭容器中加入 和
和 ,反应过程中有关物质的物质的量(n)与时间的关系如图所示,
,反应过程中有关物质的物质的量(n)与时间的关系如图所示, 是反应达到平衡状态。
是反应达到平衡状态。
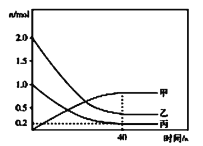
①曲线甲表示的物质是__________(写化学式)。反应开始至达到平衡时,平均反应速率 __________
__________ ,
, 的平衡转化率是__________。
的平衡转化率是__________。
②升高温度,平衡__________(填“不移动”“向正反方向移动”或“向逆反应方向移动”,下同);及时从容器中分离出尿素,平衡__________。
(3)用 电极作阳极可处理酸化后的亚硝酸盐污水,使
电极作阳极可处理酸化后的亚硝酸盐污水,使 转化为无害气体,且溶液逐渐变为黄色,则
转化为无害气体,且溶液逐渐变为黄色,则 转化为无害气体的离子方程式为__________。
转化为无害气体的离子方程式为__________。
-
运用化学反应原理研究氮、硫等单质及其化合物的反应有重要意义
(1)硫酸生产过程中2SO2(g)+O2(g) 2SO3(g),平衡混合体系中SO3的百分含量和温度的关系如右图所示,根据下图回答下列问题:
2SO3(g),平衡混合体系中SO3的百分含量和温度的关系如右图所示,根据下图回答下列问题:
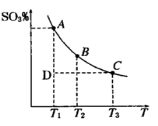
①2SO2(g)+O2(g) 2SO3(g)的△H__________0(填“>”或“<”),
2SO3(g)的△H__________0(填“>”或“<”),
②一定条件下,将SO2与O2以体积比2:1置于一体积不变的密闭容器中发生以上反应,能说明该反应已达到平衡的是 。
A.体系的密度不发生变化 B.SO2与SO3的体积比保持不变
C.体系中硫元素的质量百分含量不再变化 D.单位时间内转移4 mol 电子,同时消耗2 mol SO3
E.容器内的气体分子总数不再变化
(2)一定的条件下,合成氨反应为:N2(g)+3H2(g)  2NH3(g)。图1表示在此反应过程中的能量的变化,图2表示在2L的密闭容器中反应时N2的物质的量随时间的变化曲线。图3表示在其他条件不变的情况下,改变起始物氢气的物质的量对此反应平衡的影响。
2NH3(g)。图1表示在此反应过程中的能量的变化,图2表示在2L的密闭容器中反应时N2的物质的量随时间的变化曲线。图3表示在其他条件不变的情况下,改变起始物氢气的物质的量对此反应平衡的影响。

图1 图2 图3
①该反应的平衡常数表达式为 ,升高温度,平衡常数 (填“增大”或“减小”或“不变”)。
②由图2信息,计算0~10min内该反应的平均速率v(H2)= ,从11min起其它条件不变,压缩容器的体积为1L,则n(N2)的变化曲线为 (填“a”或“b”或“c”或“d”)
③图3 a、b、c三点所处的平衡状态中,反应物N2的转化率最高的是 点,温度T1 T2(填“>”或“=”或“<”)
(3)若将等物质的量的SO2与NH3溶于水充分反应,所得溶液呈 性,所得溶液中c(H+)- c(OH-)= (填写表达式)(已知:H2SO3:Ka1=1.7×10-2,Ka2=6.0×10-8,NH3·H2O:Kb=1.8×10-5)
-
工业上以废铜为原料经一系列化学反应可生产氯化亚铜(CuCl),其工艺流程如图所示:

试根据如图转化回答下列问题:
(1)工业生产Cl2时,尾气常用石灰乳吸收,而不用烧碱溶液吸收的原因是__________。
(2)还原过程中的产物为Na[CuCl2],试写出反应的化学方程式__________,制备中当氯化完成后必须经还原过程再制得CuCl,为什么不用一步法制得CuCl?(已知Cu2++Cu+2Cl-═2CuCl↓) __________。
(3)还原过程中加入少量盐酸的作用是__________,加入NaCl且过量的原因是__________。
(4)合成结束后所得产品用酒精淋洗的目的是__________。
(5)实验室中在CuCl2热溶液中通入SO2气体也可制备白色的CuCl沉淀,试写出该反应的离子方程式__________。
-
化学与人类生产、生活密切相关,下列有关说法不正确的是( )
A. “地沟油”禁止食用,但可用来制取肥皂
B. 在厨房里可用米汤检验加碘食盐中的碘
C. 波尔多液是由硫酸铜溶液、生石灰和水制得,可用于防治植物的病虫害
D. 纤维素在人体内不能水解为葡萄糖
-
化学与人类生产、生活密切相关,下列有关说法错误的是( )
A. Al2O3作耐火材料是因为氧化铝熔点高
B. 用加热灼烧的方法可以区分羊毛毛线和腈纶毛线
C. 波尔多液是由硫酸铜溶液、生石灰和水制得,可用于防治植物的病虫害
D. 玉米油和鸡蛋清均是高分子化合物,它们均能水解生成氨基酸
-
(1)在硫酸生产中,SO2催化氧化生成SO3是反应的关键,其反应的化学方程式为: ,反应混合体系SO3的百分含量和温度的关系如图所示(曲线上任何一点都表示平衡状态),根据图示回答下列问题:
,反应混合体系SO3的百分含量和温度的关系如图所示(曲线上任何一点都表示平衡状态),根据图示回答下列问题:
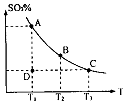
①反应 ________0(填“>”或“<”)。若在恒温恒容条件下,上述反应达到平衡,再给该平衡体系中通入SO3气体,容器内的压强________(填“增大”、“减小”或“不变”),平衡________移动(填“向正反应方何”、“逆反应方向’或“不”)若在恒温恒压条件下,上述反应达到平衡,再给该平衡体系中通人大量氮气后,体系重新达到平衡,此平衡与原平衡相比较,SO2的物质的量__________(填“增大”、“减小”或“不变”),O2的物质的量浓度________(填“增大”、“减小”或“不变”)。
________0(填“>”或“<”)。若在恒温恒容条件下,上述反应达到平衡,再给该平衡体系中通入SO3气体,容器内的压强________(填“增大”、“减小”或“不变”),平衡________移动(填“向正反应方何”、“逆反应方向’或“不”)若在恒温恒压条件下,上述反应达到平衡,再给该平衡体系中通人大量氮气后,体系重新达到平衡,此平衡与原平衡相比较,SO2的物质的量__________(填“增大”、“减小”或“不变”),O2的物质的量浓度________(填“增大”、“减小”或“不变”)。
②若温度为T1、 T2,反应的平衡常数分别为K1、K2 则K1________K2(填“>”、“<”或“=”),反应进行到D点状态时,V正________V逆(填“>”、“<”或“=”)
③在一个固定容积为5L的密闭容器中充入0.20 mol SO2和0.10 mol O2,在500℃开始反应,半分钟达到平衡,测得容器内含SO3 0.18 mol,则v(O2)=________mol·L-1·min-1,若继续通入0.20 mol SO2和0.10 mol O2,平衡发生了移动,再次达到平衡后, ________mol<n(SO3)<________mol.
(2)已知三种无色溶液:a.NaHCO3溶液,b.AlCl3溶液,c.NaAlO2溶液,它们两两反应均能生成Al(OH)3沉淀。请回答下列问题:
①两种溶液恰好完全反应,所得溶液中c(OH—)= 是水的离子积),则这两种溶液可为________(填字母)。
是水的离子积),则这两种溶液可为________(填字母)。
②能体现出NaHCO3在反应中,HCO—3的水解程度小于电离程度的离于方程式为________。
-
根据图示回答,下列说法不正确的是
A.此装置用于铁表面镀铜时,a为铁
B.此装置用于电镀铜时,硫酸铜溶液的浓度不变
C.燃料电池中正极反应为 O2+2H++2e-=H2O
O2+2H++2e-=H2O
D.若a为粗铜,b为纯铜,该装置可用于铜的精炼
-
溴、碘及其化合物在工农业生产和日常生活中有重要用途。
Ⅰ.氢溴酸在医药和石化工业上有广泛用途,下图是模拟工业制备氢溴酸的流程:
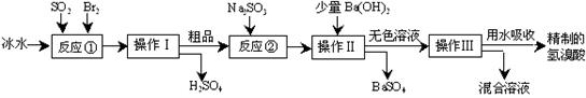
根据上述流程回答下列问题:
(1)反应①中发生反应的离子方程式为 ;使用冰水的目的是
(2)操作Ⅰ的名称是 ;操作Ⅱ的名称是 ;
(3)反应②中加入Na2SO3的目的是 ;但要防止过量,原因是 (用离子方程式表示)
Ⅱ.卤素互化物是指不同卤素原子之间以共价键结合形成的化合物。XX′型卤素互化物与卤素单质结构相似、性质相近, 能与大多数金属反应生成金属卤化物,能与许多非金属单质反应生成相应卤化物,能与水反应等。试回答下列问题:
(4)溴化碘(IBr)与水反应的方程式为IBr +H2O=HBr+HIO下列关于IBr的叙述中不正确的是
A.IBr中溴和碘的化合价均为0价 B.在许多反应中IBr是强氧化剂
C.在IBr与水的反应中,它既是氧化剂又是还原剂 D.与NaOH溶液反应生成NaIO、NaBr和H2O
(5) 在粗碘中含有IBr和ICl,受热时,I2、ICl、IBr均可升华。在粗碘中加入一种物质后,再进行升华,可制得精碘,应加入的物质是
A.H2O B.KI C.Zn D.KCl
-
(15分)运用化学反应原理研究氮、硫等单质及其化合物的反应有重要意义。
(1)硫酸生产过程中2SO2(g)+O2(g) 2SO3(g),平衡混合体系中SO3的百分含量和温度的关系如图所示,根据下图回答下列问题:
2SO3(g),平衡混合体系中SO3的百分含量和温度的关系如图所示,根据下图回答下列问题:
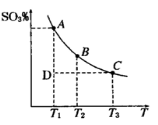
①2SO2(g)+O2(g) 2SO3(g)的△H______0(填“>”或“<”)。
2SO3(g)的△H______0(填“>”或“<”)。
②一定条件下,将SO2与O2以体积比2:1置于一体积不变的密闭容器中发生以上反应,能说明该反应已达到平衡的是___________(填字母编号)。
a.体系的密度不发生变化
b.SO2与SO3的体积比保持不变
c.体系中硫元素的质量百分含量不再变化
d.单位时间内转移4 mol 电子,同时消耗2 mol SO3
e.容器内的气体分子总数不再变化
(2)一定的条件下,合成氨反应为:N2(g)+3H2(g) 2NH3(g)。图1表示在此反应过程中的能量的变化,图2表示在2L的密闭容器中反应时N2的物质的量随时间的变化曲线。图3表示在其他条件不变的情况下,改变起始物氢气的物质的量对此反应平衡的影响。
2NH3(g)。图1表示在此反应过程中的能量的变化,图2表示在2L的密闭容器中反应时N2的物质的量随时间的变化曲线。图3表示在其他条件不变的情况下,改变起始物氢气的物质的量对此反应平衡的影响。

①该反应的平衡常数表达式为 ,升高温度,平衡常数 (填“增大”或“减小”或“不变”)。
②由图2信息,计算0~10min内该反应的平均速率v(H2)= ,从11min起其它条件不变,压缩容器的体积为1L,则n(N2)的变化曲线为 (填“a”或“b”或“c”或“d”)。
③图3 a、b、c三点所处的平衡状态中,反应物N2的转化率最高的是 点,温度T1 T2(填“>”或“=”或“<”)
(3)若将等物质的量的SO2与NH3溶于水充分反应,所得溶液呈 性,所得溶液中c(H+)- c(OH-)= (填写表达式)(已知:H2SO3:Ka1=1.7×10-2,Ka2=6.0×10-8,NH3·H2O:Kb=1.8×10-5)。



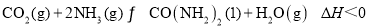 。一定温度下,在容积为
。一定温度下,在容积为






