-
实验是解决化学问题的基本途径,下列有关实验的叙述不正确的是 ( )
A.240 mL 0.2 mol·L-1 的NaCl溶液配制:需要使用天平、250 mL容量瓶等仪器
B.向FeCl3稀溶液中滴加NaOH溶液,并加热煮沸,可制备Fe(OH)3胶体
C.不慎将NaOH溶液溅到皮肤上,应立即用较多的水冲洗
D.用苯萃取碘水中的碘时,萃取后的油层不能从分液漏斗下端放出
高二化学选择题简单题查看答案及解析
-
下列有关化学实验的叙述中,正确的是( )
A. 用碱式滴定管量取20mL0.1000mol/LKMnO4溶液
B. 只用浓氨水就可以鉴别NaCl、AlCl3、MgCl2、Na2SO4四种溶液
C. 用四氯化碳萃取溴水中的溴并分液,有机层应从分液漏斗的上口倒出
D. 测定中和反应的反应热时,将碱缓缓倒入酸中,测出的温度变化值偏小
高二化学单选题中等难度题查看答案及解析
-
如图是某学校实验室从化学试剂商店买回的硫酸试剂的标签部分内容。据此判断,下列说法正确的是( )

A. 1 mol Al 与足量的该硫酸产生2 g氢气
B. 配制 240 mL 4.6 mol/L 的稀硫酸需取该硫酸 40 mL
C. 洗净的锥形瓶和容量瓶可以放进烘箱中烘干
D. 该硫酸与等质量的水混合后所得溶液的物质的量浓度小于9.2 mol/L
高二化学选择题困难题查看答案及解析
-
(8分)某同学按下列步骤配制500 mL 0.2 mol·L-1 KCl溶液,请回答有关问题。
实验步骤
有关问题
①计算所需KCl的质量
需要KCl的质量为________g(保留小数点后一位)
②称量KCl固体
称量需要用到的主要仪器是________________
③将KCl加入100 mL烧杯中,并加入适量水
为了加快溶解速率,可以采取哪些措施?
________________
④将烧杯中溶液转移至500 mL容量瓶中
为了防止溶液溅出,应采取什么措施?
__________________
⑤向容量瓶中加蒸馏水至刻度线
在进行此操作时当加水至离刻度线1 cm~2 cm处应如何操作?____________________
(1)上述实验中使用容量瓶前应检验_________________________________________________。
(2)在进行④步操作时未将洗涤烧杯、玻璃棒的洗涤液转移至容量瓶,则配制溶液浓度
________(填“偏高”、“偏低”或“不影响”)。
(3)若进行⑤步操作时加蒸馏水超过刻度线,则需________。
高二化学填空题中等难度题查看答案及解析
-
常温下,向20 mL 0.2 mol/L 二元酸H2A溶液中滴加0.2 mol/L NaOH溶液,有关微粒物质的量变化如右图。下列叙述正确的是
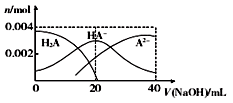
A. 从图象中可知H2A为强酸
B. 当V(NaOH)=20 mL时,溶液中各离子浓度的大小
顺序为c(Na+)>c(HA-)> c(H+) >c( A2-) >c(OH-)
C. 当V(NaOH) =20 mL时混合溶液的pH值大于7
D. 当V(NaOH) =40 mL时,升高温度,c(Na+)/c(A2-)减小
高二化学选择题困难题查看答案及解析
-
常温下,向20 mL 0.2 mol/L 二元酸H2A溶液中滴加0.2 mol/L NaOH溶液,有关微粒物质的量变化如右图。下列叙述正确的是
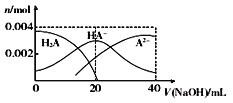
A. 从图象中可知H2A为强酸
B. 当V(NaOH)=20 mL时,溶液中各离子浓度的大小
顺序为c(Na+)>c(HA-)> c(H+) >c( A2-) >c(OH-)
C. 当V(NaOH) =20 mL时混合溶液的pH值大于7
D. 当V(NaOH) =40 mL时,升高温度,c(Na+)/c(A2-)减小
高二化学单选题困难题查看答案及解析
-
实验室用固体氯化钠配制0.5 L 0.2 mol·L-1的NaCl溶液,下列哪种仪器不是必须使用的
A.500 mL容量瓶
B.胶头滴管
C.试管
D.托盘天平
高二化学选择题简单题查看答案及解析
-
实验室用密度为1.25 g·mL-1,质量分数为36.5%的浓盐酸配制240 mL 0.1 mol·L-1的盐酸,请回答下列问题:
(1)浓盐酸的物质的量浓度为____ ____。
(2)配制240 mL 0.1 mol·L-1的盐酸应量取浓盐酸体积________mL,应选用容量瓶的规格________mL。
(3)配制时,其正确的操作顺序是 (用字母表示,每个字母只能用一次)________。
A.用30 mL水洗涤烧杯2~3次,洗涤液均注入容量瓶,振荡
B.用量筒准确量取所需的浓盐酸的体积,沿玻璃棒倒入烧杯中,再加入少量水(约30 mL),用玻璃棒慢慢搅动,使其混合均匀
C.将已冷却的盐酸沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,振荡、摇匀
E.改用胶头滴管加水,使溶液凹液面恰好与刻度线相切
F.继续往容量瓶内小心加水,直到液面接近刻度线1~2 cm处
(4) 填“偏大”、“偏小”或“无影响”
①用量筒量取浓盐酸倒入小烧杯后,用蒸馏水洗涤量筒并将洗涤液转移至小烧杯中________。
②用量筒量取浓盐酸时,仰视读数________。
③定容摇匀后,发现液面下降,继续加水至刻度线______。
④定容时仰视刻度线________。
(5)若实验过程中出现如下情况如何处理?
①加蒸馏水时不慎超过了刻度线____________________________________________。
②向容量瓶中转移溶液时不慎有溶液溅出____________________________________。
高二化学填空题简单题查看答案及解析
-
下列实验不正确的是
序号
实验内容
实验目的
A
向5mL0.1mol/LK2Cr2O7溶液中滴加5滴浓硫酸
探究反应物浓度增大对化学平衡的影响
B
向盛有1mL硝酸银溶液的试管中滴加NaCl溶液,至不再有沉淀生成,再向其中滴加Na2S溶 液
说明一种沉淀能转化为另 一种溶解度更小的沉淀
C
室温下,用pH计测定浓度为0.1mol·L−1NaClO溶液和0.1mol·L−1CH3COONa溶液的pH
比较 HClO 和 CH3COOH 的 酸性强弱
D
室温下,分别向2支试管中加入相同体积、相同浓度的Na2S2O3溶液,再分别加入相同体积不同浓度的稀硫酸
研究浓度对反应速率的影响
A. A B. B C. C D. D
高二化学单选题中等难度题查看答案及解析
-
下列实验不正确的是
序号
实验内容
实验目的
A
向5mL0.1mol/LK2Cr2O7溶液中滴加5滴浓硫酸
探究反应物浓度增大对化学平衡的影响
B
向盛有1mL硝酸银溶液的试管中滴加NaCl溶液,至不再有沉淀生成,再向其中滴加Na2S溶 液
说明一种沉淀能转化为另 一种溶解度更小的沉淀
C
室温下,用pH计测定浓度为0.1mol·L−1NaClO溶液和0.1mol·L−1CH3COONa溶液的pH
比较 HClO 和 CH3COOH 的 酸性强弱
D
室温下,分别向2支试管中加入相同体积、相同浓度的Na2S2O3溶液,再分别加入相同体积不同浓度的稀硫酸
研究浓度对反应速率的影响
A. A B. B C. C D. D
高二化学单选题中等难度题查看答案及解析