-
(题文)某兴趣小组设计了如图所示装置(部分夹持装置已略去)进行实验探究。
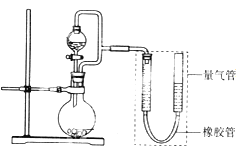
(实验一)探究影响化学反应速率的因素。
圆底烧瓶中装锌片(两次实验中所用锌片大小和外形相同)、恒压分液漏斗中装稀硫酸,以生成20.0mL气体为计时终点,结果为t1>t2。
| 序号 | V(H2SO4)/mL | c(H2SO4)/mol·L-1 | t/s |
| I | 40 | 1 | t1 |
| II | 40 | 3 | t2 |
| 序号 | V(H2SO4)/mL | c(H2SO4)/mol·L-1 | t/s | |
| I | 40 | 1 | t1 | |
| II | 40 | 3 | t2 | |
| | | | | | | |
检查该装置气密性的方法是_______________________________________________。
比较实验I和Ⅱ可以得出的结论是____________________________________________。
(实验二)探究铁的电化学腐蚀。
①圆底烧瓶中装铁粉和碳粉混合物,恒压分液漏斗中装稀硫酸,打开活塞加入稀硫酸后量气管中出现的现象是:左侧液面_________右侧液面_________(选填“上升”、“下降”)。
②圆底烧瓶中装与①相同量的铁粉但不加入碳粉,其他试剂和操作相同,发现左、右侧液面变化较_______(选填“快”、“慢”,下同),说明原电池反应比一般化学反应_______。
③圆底烧瓶中装与①相同量的铁粉和碳粉混合物,恒压分液漏斗中装食盐水,打开活塞加入食盐水后,你预测量气管中出现的现象是:___________________________________,正极的电极反应是___________________________。
-
某同学设计了如下图所示装置(部分夹持装置已略去)进行实验探究。

请回答:
(1)用上述装置探究影响化学反应速率的因素。
①圆底烧瓶中发生反应的离子方程式是 。
②用上述装置进行实验,以生成9.0 mL气体为计时终点,结果为t1>t2。
| 序号 | V(H2SO4)/mL | c(H2SO4)/mol·L-1 | t/s |
| I | 40 | 1 | t1 |
| II | 40 | 4 | t2 |
比较实验I和Ⅱ可以得出的实验结论是 。
③若将锌片换成含杂质的粗锌片,且控制其他条件使其与上述实验完全一致,所测得的反应速率均大于上述实验对应的数据。粗锌片中所含杂质可能是(填序号) 。
a.沙粒(二氧化硅) b.银 c.铜 d.石墨
(2)用上述装置验证生铁在潮湿空气中会发生吸氧腐蚀。生铁放在烧瓶中,则
①分液漏斗中的试剂可选用(填序号) 。
a.C2H5OH b.NaOH溶液 c.NaCl溶液 d.稀硫酸
②能证明生铁在潮湿空气中会发生吸氧腐蚀的现象是 。
-
(12分)某同学设计了如下图所示装置(部分夹持装置已略去)进行实验研究。

请回答:
(1)用上述装置探究影响化学反应速率的因素。
① 圆底烧瓶中发生反应的离子方程式是________。
② 用上述装置进行实验,以生成9.0 mL气体为计时终点,结果为t1>t2。
| 序号 | V(H2SO4)/mL | c(H2SO4)/mol·L-1 | t/s |
| Ⅰ | 40 | 1 | t1 |
| Ⅱ | 40 | 4 | t2 |
比较实验Ⅰ和Ⅱ可以得出的实验结论是________。
实验过程中,对量气管的操作是________。
③ 若将锌片换成含杂质的粗锌片,且控制其他条件使其与上述实验完全一致,所测得的反应速率均大于上述实验对应的数据。粗锌片中所含杂质可能是(填序号)________。
a.石墨 b.银 c.铜 d.沙粒(二氧化硅)
(2)用上述装置验证生铁在潮湿空气中会发生吸氧腐蚀。
① 圆底烧瓶中的试剂可选用(填序号)________。
a.NaOH溶液 b.C2H5OH c.NaCl溶液 d.稀硫酸
② 能证明生铁在潮湿空气中会发生吸氧腐蚀的现象是________。
-
某同学设计计如下图所示装罝(部分夹持装置己略去)进行实验探究:

(1)用上述装置探究影响化学反应速率的因素。以生成9.0 mL气体为计时终点,结果为t1>t2。
| 序号 | V(H2SO4)/mL | C(H2SO4)/mol·L-1 | t/s |
| I | 40 | 1 | t1 |
| II | 40 | 4 | t2 |
①比较实验I和Ⅱ可以得出的实验结论是_______________。
②若将锌片换成含杂质的粗锌片,其他条件使其与上述一致,所测得的反应速率均大于上述实验对应的数据。粗锌片中所含杂质可能是_________(填序号)。
A.二氧化硅 B.银 C.铜 D.石墨
(2)用上述装置验证生铁在潮湿空气中会发生吸氧腐蚀。
①圆底烧瓶中的试剂可选用________(填序号)。
A.稀HCl B .NaCl溶液 C.乙醇 D.NaOH溶液
②能证明生铁在潮湿空气中会发生吸氧腐蚀的现象是_____________。
-
某同学设计计如下图所示装罝(部分夹持装置己略去)进行实验探究:

(1)用上述装置探究影响化学反应速率的因素。以生成9.0 mL气体为计时终点,结果为t1>t2。
| 序号 | V(H2SO4)/mL | C(H2SO4)/mol·L-1 | t/s |
| I | 40 | 1 | t1 |
| II | 40 | 4 | t2 |
①比较实验I和Ⅱ可以得出的实验结论是_______________。
②若将锌片换成含杂质的粗锌片,其他条件使其与上述一致,所测得的反应速率均大于上述实验对应的数据。粗锌片中所含杂质可能是_________(填序号)。
A.二氧化硅 B.银 C.铜 D.石墨
(2)用上述装置验证生铁在潮湿空气中会发生吸氧腐蚀。
①圆底烧瓶中的试剂可选用________(填序号)。
A.稀HCl B .NaCl溶液 C.乙醇 D.NaOH溶液
②能证明生铁在潮湿空气中会发生吸氧腐蚀的现象是_____________。
-
硫代硫酸钠又名大苏打、海波,可以用于治疗氰化物中毒等,某化学兴趣小组通过查阅资料,设计了如下的装置(略去部分夹持仪器)来制取Na2S2O3·5H2O晶体并探究其性质。
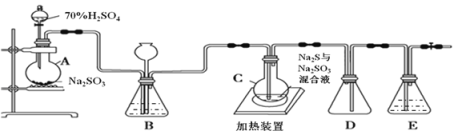
已知烧瓶C中发生如下三个反应:
Na2S(aq)+H2O(l)+SO2(g) = Na2SO3(aq)+H2S(aq)
2H2S(aq)+SO2(g) =3S(s)+2H2O(l) ;S(s)+Na2SO3(aq)  Na2S2O3(aq)
Na2S2O3(aq)
(1)装置B的作用之一是观察SO2的生成速率。控制SO2生成速率可以采取的措施有_________________________(写一条)
(2)常温下,用pH试纸测定0.1 mol·L-1 Na2S2O3溶液pH值约为8,测定时的具体操作是_______________________________。
(3)向新制氯水中滴加少量Na2S2O3溶液,氯水颜色变浅,有硫酸根离子生成,写出该反应的离子方程式_____________________。
-
某化学兴趣小组对2-溴丙烷与NaOH溶液发生的反应进行探究,实验装置如下(夹持和加热装置已略去):
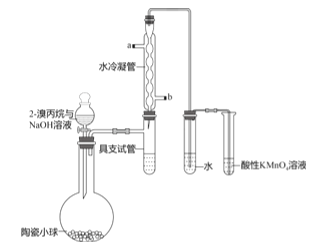
实验步骤:
ⅰ.将圆底烧瓶用水浴加热,冷凝管中通入冷凝水;
ⅱ.将分液漏斗中的2-溴丙烷与NaOH溶液的混合液滴入圆底烧瓶内。
(1)水冷凝管a口是__________(填“进水口”或“出水口”)。
(2)取具支试管中收集到的液体,经红外光谱检测,其中一种物质中存在C-O键和O-H键。则该物质的结构简式是_________________。
(3)实验中酸性KMnO4溶液褪色,生成该使酸性KMnO4溶液褪色的物质的反应的化学方程式是____________________________________________________________。
(4)通过该实验得到的结论是___________________________________________________。
-
铋酸钠(NaBiO3)是分析化学中的重要试剂,在水中缓慢分解,遇沸水或酸则迅速分解。某兴趣小组设计实验制取铋酸钠并探究其应用。回答下列问题:
Ⅰ.制取铋酸钠
制取装置如图(加热和夹持仪器已略去),部分物质性质如下:
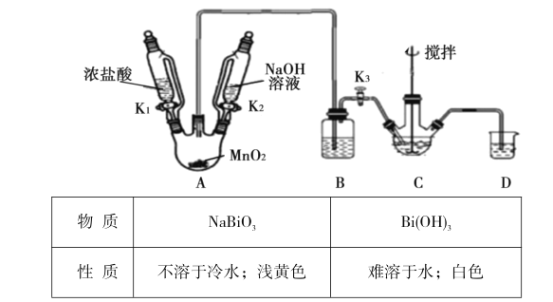
(1)C中盛放Bi(OH)3与NaOH的混合物,与Cl2反应生成NaBiO3,反应的化学方程式为__。B装置的作用是__。
(2)当观察到__(填现象)时,可以初步判断C中反应已经完成。
(3)拆除装置前必须先除去残留的Cl2,以免污染空气。除去烧瓶A中残留Cl2的操作是:关闭__;打开__。
(4)反应结束后,为从装置C中获得尽可能多的产品,需要的操作有_。
Ⅱ.铋酸钠的应用——检验Mn2+
(5)往待检液中加入铋酸钠晶体,加硫酸酸化,生成Bi3+,且溶液变为紫红色,证明待检液中存在Mn2+。产生紫红色现象的离子方程式为__。
Ⅲ.产品纯度的测定
(6)取上述NaBiO3产品ag,加入足量稀硫酸和MnSO4稀溶液使其完全反应,再用bmo1•L-1的H2C2O4标准溶液滴定生成的MnO4-(已知:H2C2O4+MnO4-—CO2+Mn2++H2O,未配平),当溶液紫红色恰好褪去时,消耗cmL标准溶液。该产品的纯度为__(用含a、b、c的代数式表示)。
-
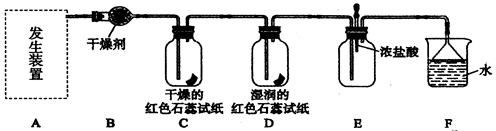
某化学兴趣小组为了制取并探究氨气性质,按下列装置(部分夹持装置已略去)进行实验。
【实验探究】
(1)实验室制取氨气应选用下图中________发生装置进行实验,反应的化学方程式为
_________________________

(2)B装 置中的干燥剂可选用________(填“碱石灰”或“浓硫酸”)。
置中的干燥剂可选用________(填“碱石灰”或“浓硫酸”)。
(3)气体通过C、D装置时,试纸颜色会发生变化的是____(填“C”或“D”)。
(4)当实验进行一段时间后,挤压E装置中的胶头滴管,滴入1~2滴浓盐酸,可观察到的现象是____________________________________________________________。
(5)F装置中倒置漏斗的作用_______________________ _________________________。
_________________________。
(6)某同学用右图所示装置进行氨气的性质实验,根据烧瓶内产生红色喷泉的现象,说明氨气具有________性质(填序号)。
a.还原性 b.极易溶于水 c.与水反应生成碱性物质
(7)氨气的用途很广。如可用氨气处理二氧化氮:8NH3 + 6NO2 ==7N2 + 12H2O
该反应中氨气体现________(填“氧化性”或“还原性”)。请你列举出氨气的另一种用途_____________________________________________。
-
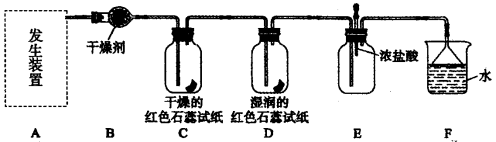
某化学兴趣小组为了制取并探究氨气性质,按下列装置(部分夹持装置已略去)进行实验。[制取氨气的反应原理:2NH4Cl+Ca(OH)2=CaCl2+2NH3↑+2H2O]
【实验探究】
(1)利用上述原理,实验室制取氨气应选用下图中 发生装置进行实验。
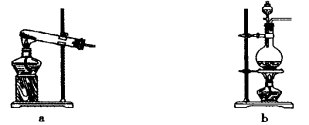
(2)B装置中的干燥剂可选用 (填“碱石灰”或“浓硫酸”)。
(3)用5.35 g NH4Cl固体与足量Ca(OH)2反应,最多可制得标准状况下氨气的体积为 L。(NH4Cl的摩尔质量为53.5 g·mol-1)
(4)气体通过C、D装置时,试纸颜色会发生变化的是 (填“C”或“D”)。
(5)当实验进行一段时间后,挤压E装置中的胶头滴管,滴入1~2滴浓盐酸,可观察到的现象是 。
(6)F装置中倒置漏斗的作用 。
【拓展应用】
(7)某同学用氨气和滴加酚酞的水做喷泉实验,根据烧瓶内产生红色喷泉的现象,说明氨气具有 性质(填序号)。
a.还原性 b.极易溶于水 c.与水反应生成碱性物质
(8)氨气的用途很广。如可用氨气处理二氧化氮: 8NH3 + 6NO2 =7N2 + 12H2O
该反应中氨气体现 (填“氧化性”或“还原性”)。
请你列举出氨气的另一种用途 。