常温下浓度均为0.1 mol/L的四种盐溶液,其pH如下表所示,下列说法正确的是
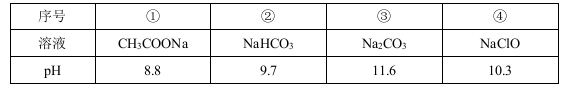
A.将等浓度的CH3COOH和HClO溶液,pH小的是HClO
B.Na2CO3和NaHCO3溶液中粒子种类不同
C.溶液水的电离程度①>②>④>③
D.NaHCO3溶液中,c(Na +)=c(CO3 2- )+c(HCO3- )+c(H2CO3)
高三化学选择题中等难度题
常温下浓度均为0.1 mol/L的四种盐溶液,其pH如下表所示,下列说法正确的是

A.将等浓度的CH3COOH和HClO溶液,pH小的是HClO
B.Na2CO3和NaHCO3溶液中粒子种类不同
C.溶液水的电离程度①>②>④>③
D.NaHCO3溶液中,c(Na +)=c(CO3 2- )+c(HCO3- )+c(H2CO3)
高三化学选择题中等难度题
常温下浓度均为0.1 mol/L的四种盐溶液,其pH如下表所示,下列说法正确的是

A.将等浓度的CH3COOH和HClO溶液,pH小的是HClO
B.Na2CO3和NaHCO3溶液中粒子种类不同
C.溶液水的电离程度①>②>④>③
D.NaHCO3溶液中,c(Na +)=c(CO3 2- )+c(HCO3- )+c(H2CO3)
高三化学选择题中等难度题查看答案及解析
下列叙述正确的是( )
A.常温下,用精密pH试纸分别测定浓度均为0.1mol/L的NaClO溶液和CH3COONa溶液的pH比较HClO和CH3COOH的酸性强弱
B.向CuSO4溶液中加入铁粉,有红色固体析出,Fe2+的氧化性强于Cu2+的氧化性
C.向NaCl、NaI混合溶液中滴入少量AgNO3溶液,有黄色沉淀生成,说明Ksp(AgCl) >Ksp(AgI)
D.反应Al2O3(s)+3Cl2(g)+3C(s)=2AlCl3(g)+3CO(g)室温下不能自发进行,则△H>0
高三化学单选题中等难度题查看答案及解析
常温下,浓度均为0.1 mol/L的6种盐溶液pH如下:

下列说法正确的是
A. Cl2和Na2CO3按物质的量之比1:1反应的化学方程式为Cl2+Na2CO3+H2O=HClO+NaHCO3+NaCl
B.相同条件下电离程度比较:HCO3->HSO3->HClO
C.6种溶液中,Na2SiO3溶液中水的电离程度最小
D.NaHSO3溶液中离子浓度大小顺序为c(Na+)>c(H+)>c(HSO3-)>c(SO32-)>c(OH-)
高三化学选择题中等难度题查看答案及解析
常温下向l0mL0.1mol·L-1ICH3COONa溶液中,不断通入HCl气体后,CH3COO-与CH3COOH浓度的变化趋势如下图所示(不考虑溶液休积变化),下列说法不正确的是( )

A. 当n(HCl)=1.0×10-3mol时,溶液中 c(Na+)=c(Cl-)>c(H+)>c(CH3COO-)>c(OH-)
B. M点溶液中水的电离程度比原溶液小
C. 随着HCl的通入,c(OH-)/c(CH3COO-) 值不断减小
D. 在M 点时,c(H+)-c(OH-)=(a-0.05)mol/L
高三化学选择题困难题查看答案及解析
已知:25℃时某些弱酸的电离平衡常数(如下表)。下面图象表示常温下稀释CH3COOH、HClO两种酸的稀溶液时,溶液pH随加水量的变化。下列说法正确的是( )

A.相同浓度CH3COONa和NaClO的混合液中,各离子浓度的大小关系是c(Na+)>c(ClO-)>c(CH3COO-)>c(OH-)>c(H+)
B.向NaClO溶液中通入少量二氧化碳的离子方程式为:2ClO-+CO2+H2O═2HClO+CO
C.图象中a、c两点处的溶液中相等(HR代表CH3COOH或HClO)
D.图象中a点酸的浓度大于b点酸的浓度
高三化学单选题困难题查看答案及解析
高三化学选择题中等难度题查看答案及解析
常温下,有物质的量浓度均为0.1mol·L—1的CH3COOH溶液和NaOH溶液,下列说法正确的是
A.CH3COOH溶液的pH=1
B.往醋酸溶液中加水,c(OH—) 和c(H+)均增大
C.两溶液等体积混合, c(Na+)﹥c(CH3COO—)
D.两溶液按一定体积比混合,可能存在:c(CH3COO—) ﹥c(Na+)
高三化学选择题简单题查看答案及解析
已知常温下Ka(CH3COOH)>Ka(HClO)、Ksp(AgCl)>Ksp(AgBr)。下列分析不正确的是( )
A.将10 mL 0.1 mol/L Na2CO3溶液逐滴滴加到10 mL 0.1 mol/L盐酸中:c(Na+)>c(Cl-)>c(CO32-)>c(HCO3-)
B.现有①200 mL 0.1 mol/L NaClO溶液,②100 mL0.1 mol/L CH3COONa溶液,两种溶液中的阴离子的物质的量浓度之和:②>①
C.向0.1 mol/L NH4Cl溶液中加入少量NH4Cl固体:比值减小
D.将AgBr和AgCl的饱和溶液等体积混合,再加入足量AgNO3浓溶液:产生的AgCl沉淀多于AgBr沉淀
高三化学单选题困难题查看答案及解析
已知常温时CH3COOH和NH3•H2O 的电离常数相等,现向10 mL浓度为0.1 mol•L-1的CH3COOH溶液中滴加相同浓度的氨水,在滴加过程中下列说法正确的是
A.水的电离程度始终增大
B.c(NH4+)/c(NH3•H2O)先增大再减小
C.当加入氨水的体积为10 mL时,溶液中的离子浓度:c(NH4+)=c(CH3COO-)﹥c(H+)= c(OH-)
D.当加入氨水的体积为10 mL时,溶液中的pH=7,由水电离出的c(H+)=1×10-7
高三化学选择题中等难度题查看答案及解析
已知常温下CH3COOH和NH3·H2O的电离平衡常数分别为Ka、Kb。若在常温下向0.1mol/L的醋酸溶液中逐滴加入相同浓度的氨水直至完全过量,则下列说法正确的是
A. 加入氨水的过程中,溶液的导电性一直不断增强
B. CH3COONH4在水溶液中的水解平衡常数Kh=Kw/(Ka+Kb)
C. 若Ka≈Kb,当加入等体积的氨水时,溶液基本呈中性
D. 该等式在滴加过程中始终成立c(CH3COO-)+c(CH3COOH)=c(NH4+)+c(NH3·H2O)
高三化学单选题困难题查看答案及解析