-
氟是一种非金属性极强的元素,它的单质甚至能与稀有气体氙反应生成XeF2、XeF4、XeF6等固体,这些固体都极易与水反应。试回答下列问题:
(1)已知XeF4与H2O反应的化学反应方程式为:6XeF4+12H2O=4Xe↑+3O2↑+2XeO3+24HF,该反应中1molH2O可以还原__________molXeF4。
(2)已知XeF6与H2O发生非氧化还原反应而完全水解(XeF6+3H2O=XeO3+6HF)。现有14.7gXeF6完全水解后,再加入100mL0.600mol·L-1Mn2+的水溶液恰好完全反应,放出的气体干燥后再通过红热的金属铜,气体体积减少20%。
①通过计算可确定Mn2+的氧化产物为_________________离子;
②已知氢氟酸溶液中存在电离平衡,其含氟各物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与pH 的关系如图所示,图中a 点pH=-lg(4.0×10-4)。
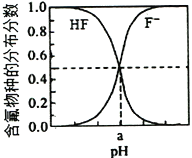
写出氢氟酸的电离平衡常数Ka的数学表达式_________________,将上述(2)中所得溶液稀释到1000mL(不考虑稀释对氢氟酸电离平衡的影响),则稀释后溶液中。H+浓度约为__________ mol·L-1,F-浓度约为__________ mol·L-1。
(3)若先向FeCl3溶液中加入足量NaF溶液,再滴加KSCN溶液,不呈红色,若再加入足够量FeCl3溶液,呈现红色。请对上述实验现象作出解释____________________________。
-
F2和Xe在一定条件下生成氧化性极强且极易与水反应的XeF2、XeF4和XeF6三种化合物。其中XeF4与H2O可以发生如下反应:6 XeF4+12H2O=2XeO3+4Xe↑+24HF+3O2↑。下列判断正确的是
A. 上述反应中氧化剂和还原剂的物质的量之比为l:2
B. XeF4按以上方式与水反应,每生成3molO2转移12mol电子
C. XeF2加入水中,在水分子的作用下,将重新生成Xe和F2
D. XeF2、XeF4和XeF6在空气中都能长期存放
-
F2和Xe在一定条件下生成氧化性极强且极易与水反应的XeF2、XeF4和XeF6三种化合物。其中XeF4与水可发生如下反应:6XeF4+12H2O═2XeO3+4Xe↑+24HF+3O2↑.下列判断中正确的是
A. 上述反应中氧化剂和还原剂的物质的量之比为1∶2
B. XeF4按以上方式与水反应,每生成3molO2,转移12mol电子
C. XeF2加入水中,在水分子的作用下,将重新生成Xe和F2
D. XeF2、XeF4和XeF6在空气中都能长期存放
-
F2和Xe在一定条件下可生成氧化性极强且极易水解的XeF2、XeF4和XeF6三种化合物。如XeF4与水可发生如下反应:6XeF4+12H2O==2XeO3+4Xe↑+24HF+3O2↑。
下列判断中正确的是
A.F一般无正价,但在HFO中的F价态为+1
B.XeF2分子中各原子均达到8电子结构
C.XeF4按已知方式水解,反应中氧化剂为XeF4、还原剂为H2O
D.XeF4按已知方式水解,每生成4molXe,转移16mol电子
-
F2和Xe在一定条件下可生成氧化性极强且极易水解的XeF2、XeF4和XeF6三种化合物。如XeF4与水可发生如下反应:
6XeF4+12H2O==2XeO3+4Xe↑+24HF+3O2↑。下列判断中正确的是:
A.XeF2分子中各原子均达到八电子结构
B.XeF6分子中Xe的化合价为0价
C.上述反应中氧化剂和还原剂的物质的量之比为1∶2
D.XeF4按已知方式水解,每生成4molXe,转移12mol电子
-
F2和Xe在一定条件下可生成氧化性极强且极易水解的XeF2、XeF4和XeF6三种化合物.如XeF4与水可发生如下反应:6XeF4+12H2O═2XeO3+4Xe↑+24HF+3O2↑.下列判断中正确的是( )
A.XeF2分子中各原子均达到8电子结构
B.XeF6分子中Xe的化合价为+6价
C.XeF4按已知方式水解,反应中氧化剂和还原剂的物质的量之比为1:2
D.XeF4按已知方式水解,每生成4molXe,转移12mol电子
-
稀有气体在一定条件下也能与某些物质反应,如:Xe与F2在一定条件下可以形成XeF4、XeF6.现有标准状况下的XeF4、XeF6的混合气体1L,密度为10.26g/L.
(1)混合气体的平均摩尔质量为______.(保留两位小数,下同)
(2)混合气体中XeF4的质量为______g.
(3)氟化氙都是强氧化剂,如在水中都能将Cl-氧化成Cl2,并生成Xe(g)和HF.将上述标准状况下的混合气体1L通入含过量Cl-的溶液中,能生成Cl2______mol.
-
(11分)都由短周期元素形成的常见非金属固体单质A与常见金属单质B,在加热条件下反应生成化合物C,C与水反应生成白色沉淀D和气体E,D既能溶于强酸,也能溶于强碱。E在足量空气中燃烧产生刺激性气味气体G,G在大气中能导致酸雨的形成。E被足量氢氧化钠溶液吸收得到无色溶液F,溶液F在空气中长期放置发生反应,生成物之一为H。 H与一种相对分子质量为78的供氧剂的结构和化学性质相似,其溶液显黄色.
请回答下列问题:
(1)组成单质A的元素位于周期表中的位置________。
(2)指出H物质中的化学键类型________。
(3)写出B与氢氧化钠溶液反应的离子方程式:______________________。
(4)E被足量NaOH溶液吸收得到溶液中的离子浓度由大到小关系是________。
(5)G与氯酸钠在酸性条件下反应可生成消毒杀菌剂二氧化氯.当生成2 mol二氧化氯时,转移电子________mol.
(6)溶液F在空气中长期放置生成H的化学反应方程式为:________。
-
(15分)
短周期元素形成的常见非金属固体单质A与常见金属单质B,在加热条件下反应生成化合物C,C与水反应生成白色沉淀D和气体E,D既能溶于强酸,也能溶于强碱。E在足量空气中燃烧产生刺激性气体G,G在大气中能导致酸雨的形成。E被足量氢氧化钠溶液吸收得到无色溶液F。溶液F在空气中长期放置发生反应,生成物之一为H。H与过氧化钠的结构和化学性质相似,其溶液显黄色。
请回答下列问题:
(1)组成单质A的元素位于周期表中第________周期,第________族。
(2)B与氢氧化钠溶液反应的化学方程式为:
________。
(1)G与氯酸钠在酸性条件下反应可生成消毒杀菌剂二氧化氯。该反应的氧化产物为________
________,当生成2 二氧化氯时,转移电子________
二氧化氯时,转移电子________ 。
。
(2)溶液F在空气中长期放置生成H的化学反应方程式为:
________。
(3)H的溶液与稀硫酸反应产生的现象为________
________。
-
(10分)短周期元素形成的常见非金属固体单质A与常见金属单质B,在加热条件下反应生成化合物C,C与水反应生成白色沉D和气体E,D既能溶于强酸,也能溶于强碱。E在足量空气中燃烧产生刺激性气体G,G在大气中能导致酸雨的形成。E被足量氢氧化钠溶液吸收得到无色溶液F。溶液F在空气中长期放置发生反应,生成物之一为H。H与过氧化钠的结构和化学性质相似,其溶液显黄色。
请回答下列问题:
(1)组成单质A的元素在周期表中的位置是________。
(2)组成单质B的元素的原子结构示意图为________。
(3)G与氯酸钠在酸性条件下反应可生成消霉杀菌剂二氧化氯.该反应的氧化剂
为________。
(4)溶液F在空气中长期放置生成H的化学反应万程式为:________
________。
(5)H的溶液与稀硫酸反应产生的现象为________
________。
