-
(1)常温下,将NH3·H2O与盐酸等体积混合,实验数据如下:
| 组别 | NH3·H2O | HCl | 混合溶液的pH值 |
| 甲 | c(NH3·H2O)=0.1mol·L-1 | c(HCl)=0.1mol·L-1 | pH=a |
| 乙 | NH3·H2O的pH=12 | HCl的pH=2 | pH=b |
| 丙 | c(NH3·H2O)=A mol·L-1 | c(HCl)=0.1mol·L-1 | pH=c |
针对甲、乙、丙三组实验,回答下列问题:
①甲组反应后,溶液中离子浓度的大小顺序为__________________;
②乙组b________7(填“>”、“<”或“=”)
③丙组溶液混合后c=7,A________0.1mol·L-1(填“>”、“<”或“=”)
④甲中a=6,混合溶液中c(Cl-)-c(NH4+)= ____________mol·L-1 (列式表示结果,不能做近似计算)。(2)常温下,在20.0mL 0.20mol/LCH3COONa溶液中滴加0.20mol/L的稀盐酸。溶液的PH 的变化关系如右图所示。
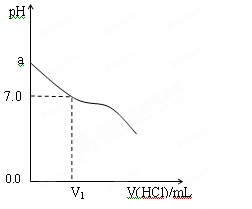
①a >7.0的理由是(用离子方程式表示)。
②当加入的盐酸的体积为20.0mL时,测定溶液中的c(H+)为1.3×10-3 mol/L,求CH3COOH的电离平衡常数Ka________(设混合后的体积为二者的体积之和,计算结果保留两位有效数字。)
-
在生产生活中,酸碱中和及溶液酸碱性研究具有十分重要的意义。
(1)常温下,将2种一元酸分别和NaOH溶液等体积混合,实验数据如下:
| 组别 | c(一元酸) | c(NaOH) | 混合溶液的pH |
| 甲 | c(HY)=0.1mol/L | 0.1mol/L | pH=7 |
| 乙 | c(HZ)=0.1mol/L | 0.1mol/L | pH=9 |
①甲组实验中HY为_________(填强、弱)酸,0.1 moL/L HY溶液的pH=_____________。
②乙组实验中发生反应的离子方程式为_________________________________。
③乙组实验所得溶液中由水电离出的c(OH-)=________ mol/L。
(2)常温下,用0.1000mol/L NaOH溶液分别滴定20.00mL0.1000mol/LHCl溶液和20.00mL 0.1000mol/LCH3COOH溶液,得到2条滴定曲线,如下图所示。

①滴定HCl溶液的曲线是___________(填“I”或“Ⅱ”);
②a=__________ mL。
③c(Na+)=c(CH3COO-)的点是_____________。
④E点对应离子浓度由大到小的顺序为_________________。
(3)将一定量某浓度的NaOH溶液,加入MgCO3悬浊液中,可以生成更难溶的Mg(OH)2。该反应的离子方程式为_____________________________。
-
(8分)常温下,将3种一元酸分别和NaOH溶液等体积混合,实验数据如下:
| 组别 | 一元酸 | NaOH | 混合溶液的pH |
| 甲 | c(HX)="0.1" mol/L | c(NaOH)=0.1mol/L | pH = a |
| 乙 | c(HY)=c1 mol/L | c(NaOH)=0.1mol/L | pH = 7 |
| 丙 | c(HZ)="0.1" mol/L | c(NaOH)=0.1mol/L | pH = 9 |
| 丁 | pH=2 HZ | pH=12 NaOH | pH = b |
(1)甲组实验中HX为弱酸,a________7(填“<”,“=”或“>”),
混合溶液中离子浓度由大到小顺序为________。
(2)乙组实验中HY为强酸,则HY溶液的pH=________。
(3)丙组实验发生反应的离子方程式为________,
所得溶液中由水电离出的c (OH-) = ________mol/L。
(4)丁组实验中b ________7(填“<”,“=”或“>”)。
-
下列说法中错误的是( )
A. 0.1 mol/L的HCl与0.1 mol/L的NH3·H2O等体积混合,溶液中的c(NH4+)>c(Cl-)
B. 常温下pH=3的HCl与pH=11的氨水等体积混合,溶液中的c(OH-)>c(H+)
C. pH=11的NaCN溶液中,由水电离出来的c(OH-)=c(H+)
D. CO2、SO2的水溶液能导电,但它们是非电解质
-
室温下,将稀盐酸和一元碱BOH溶液等体积混合(忽略混合后溶液的体积变化),实验数据如下表:

请回答:
(1)HCl溶液和BOH溶液反应的离子方程式为___________________;
(2)实验①反应后的溶液中由水电离出的c(OH-)=_________mol·L-1;实验③反应后的溶液中由水电离出的c(OH-)=_________mol·L-1
(3)x_________0.2 mol·L-1(填“>”“<”或“=”;)
-
常温下,下列溶液中各离子浓度关系正确的是 ( )
A. 等体积等物质的量浓度的氨水和盐酸混合后的溶液:c(H+)=c(OH-)+c(NH3·H2O)
B. 浓度为0.1 mol·L-1的碳酸钠溶液:c(Na+)=2c(CO32-+c(HCO3-)+c(H2CO3)
C. pH=12的氨水与pH=2的盐酸等体积混合:c(Cl-)>c(NH4+)>c(H+)>c(OH-)
D. 醋酸溶液与NaOH溶液相混合后,所得溶液呈中性:c(Na+)>c(CH3COO-)
-
常温下,向1 L 0.1 mol·L-1一元酸HR溶液中逐渐通入氨气[已知常温下NH3·H2O电离平衡常数K=1.76×10-5],使溶液温度和体积保持不变,混合溶液的pH与离子浓度变化的关系如下图所示。下列叙述正确的是
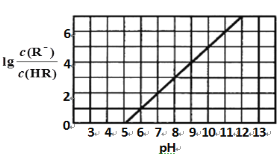
A. 0.1 mol·L-1 HR溶液的pH为5
B. HR为弱酸,常温时随着氨气的通入,c(R-)/[c(OH-).c(HR)] 逐渐增大
C. 当通入0.1 mol NH3时,c(NH4+)>c(R-)>c(OH-)>c(H+)
D. 当c(R-)= c(HR)时,溶液必为中性
-
某无色混合气体可能由H2、O2、NH3、N2、CO2、HCl和He中的两种或多种组成。常温下取此气体200mL进行实验,实验的过程和结果如下(上述气体的体积都是折算成相同条件下的体积)。下列说法错误是
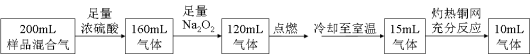
A.原混合气体中有5ml O2
B.原混合气体中肯定存在NH3,肯定不存在HCl
C.原混合气体中CO2的体积分数为40%
D.可能存在N2或He,它们在原混合气体中的体积分数不可能超过5%
-
下列事实能说明NH3·H2O一定是弱电解质的是
A.常温下,NH3·H2O溶液能使酚酞变红;
B.氨气极易溶于水;
C.常温下,体积、pH均相同的NH3·H2O溶液和NaOH溶液,与同浓度HCl溶液中和时,消耗HCl溶液的体积:前者>后者;
D.常温下,将pH=13的醋酸钠溶液稀释到1000倍,测得pH>10
-
室温下将a mL三种一元酸分别和NaOH溶液等体积混合,实验数据如下:
| 组别 | c(一元酸) | c(NaOH) / mol·L-1 | 混合溶液的pH |
| 甲 | c(HX)=0.1 mol·L-1 | 0.1 | pH = 10 |
| 乙 | c(HY)=0.1 mol·L-1 | 0.1 | pH = 7 |
| 丙 | c(HZ)=0.1 mol·L-1 | 0.1 | pH = 9 |
(1)根据表中数据比较HX、HY、HZ三种酸的酸性由强到弱的顺序为_________,丙组实验发生反应的离子方程式为 ,所得溶液中由水电离出的c(OH-)= mol·L-1。
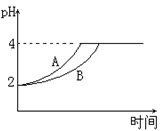
(2)部分实验反应过程中的pH变化曲线如下图:

①表示乙组实验的pH变化曲线是________________(填“图1”或“图2”)
②以上两图中表示溶液恰好完全反应的点是________________。
(3)常温下,将pH=3的盐酸aL分别与下列三种溶液混合,所得溶液均呈中性。
①浓度为1.0×10-3 mol·L-1的氨水b L
②c(OH-)=1.0×10-3 mol·L-1的氨水c L
③c(OH-)=1.0×10-3 mol·L-1的氢氧化钡溶液d L。则a、b、c、d的大小关系是_________________。
(4)常温下,取pH=2的盐酸和醋酸溶液各100mL,向其中分别加入适量的Zn粒,反应过程中两溶液的pH变化如图所示.则图中表示醋酸溶液中pH变化曲线的是__________(填“A”或“B”);设盐酸中加入的Zn质量为m1,醋酸溶液中加入的Zn质量为m2.则m1__________m2(填“<”、“=”、“>”)