-
固体储氢材料氨硼烷,化学式为 NH3BH3,可用如下反应制取: Ni(NH3)6Cl2+2NaBH4 =2NH3BH3+4NH3↑+2NaCl+H2↑+Ni。下列说法正确的是
A.NaBH4中B元素化合价为+3 B.每生成11.2 L H2转移 NA个电子
C.NaBH4在反应中作氧化剂 D.NH3BH3在反应中属于还原产物
高三化学选择题中等难度题查看答案及解析
-
非金属硼的合金及其化合物有着广泛的用途。
(1)硼钢合金的硬度是普通钢材的 4 倍,其主要成分是铁。 画出基态铁原子的价电子排布图_____。
(2)氨硼烷(NH3BH3)是一种新型储氢材料,其分子中存在配位键, 则氨硼烷分子结构式为_____。写出一种与氨硼烷互为等电子体的分子_____(填化学式)。
(3)常温常压下硼酸(H3BO3)晶体结构为层状,其二维平面结构如右图所示。
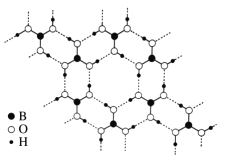
①1 mol H3BO3晶体中含有______mol 氢键。
②请从氢键的角度解释硼酸在冷水中的溶解度小而加热时溶解度增大的原因:__________。
(4)硼氢化钠是一种常用的还原剂。其晶胞结构如右图所示:
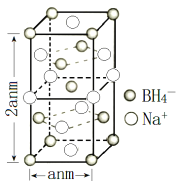
①该晶体中Na+的配位数为_____。
②H3BO3 分子中的 O—B—O 的键角_____(填“大于”、“等于”或“小于”) BH4-中的 H—B—H 的键角,判断依据是_____。
③已知硼氢化钠晶体的密度为 ρ g/cm3, NA代表阿伏伽德罗常数的值,则 a=_____(用含 ρ、 NA的代数式表示);④若硼氢化钠晶胞上下底心处的 Na+被 Li+取代,得到的晶体的化学式为_____。
高三化学填空题困难题查看答案及解析
-
氢化铝锂(LiAlH4)和硼氢化钠(NaBH4)都是有机合成中非常重要的还原剂,可发生如下反应:① LiAlH4+4H2O=LiOH+Al(OH)3+4H2↑;② NaBH4+NH4Cl=NH3BH3+NaCl+H2↑。则下列说法中错误的是( )
A.LiAlH4 中 H 元素为-1 价
B.反应②中,每生成 1mol NH3BH3 会转移 2 mol e-
C.两个反应中,H2 均既是氧化产物,又是还原产物
D.两个反应中 LiAlH4 和 NaBH4 均作还原剂
高三化学单选题中等难度题查看答案及解析
-
镍配合物在传感器、磁记录材料、储氢材料、电极催化剂和化学键研究等方面有着广泛的应用。以纯镍片为原料制备一种镍配合物[Ni(NH3)xCly]Clz·nH2O的主要流程如下:
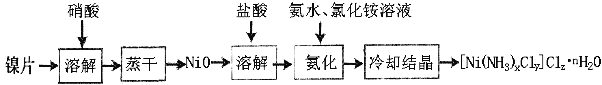
(1)工业上镍氢电池总反应式为:LaNi5H6 + NiOOH
LaNi5 + Ni(OH)2,其中KOH作电解质溶液,负极电极反应式为:_______________________
(2)常温下,镍投入60%的浓硝酸无明显现象,流程中需控制反应温度50-60oC,控温原因可能是_______,写出离子反应方程式:____________________________。
(3)冷却结晶后洗涤、过滤、干燥得到[Ni(NH3)xCly]Clz·nH2O,其中洗涤的正确操作是___________________________________________________________________。
(4)氨化过程中应控制溶液pH范围8~9,其原因是_____________________________。上述流程中,有关说法正确的是___________
A.氨化操作为在过量氨水和氯化铵缓冲溶液中,缓慢滴入酸化的NiCl2溶液,并不断搅拌
B.此缓冲溶液中微粒浓度大小顺序为:c(Cl—)> c(NH3·H2O) >c(NH4+) > c(OH—)> c(H+)
C.冷却结晶后的母液加适量氨水调节pH后可以循环利用
D.可以用热的浓硫酸和浓硝酸混合溶液代替浓硝酸溶解镍片
(5)为测定化合物[Ni(NH3)xCly]Clz·nH2O的组成,进行如下实验:
实验一:称取样品0.6460 g,加入过量的浓NaOH溶液,煮沸,冷却,蒸出的氨用40.00 mL 0.5000 mol·L-1的盐酸完全吸收,并用蒸馏水定容至100 mL,得溶液B。取B溶液20.00 mL,加入指示剂少量,用0.1000 mol·L-1NaOH滴定,消耗NaOH溶液20.00 mL。
实验二:另取该样品0.6460 g,溶于水,以0.1000 mol·L-1AgNO3溶液滴定至恰好反应完全,消耗AgNO3溶液20.00 mL。相应反应化学方程式为: [Ni(NH3)xCly]Clz+zAgNO3=[Ni (NH3)xCly] (NO3)z+zAgCl↓ 测得该镍配合物的化学式为______________。
高三化学综合题中等难度题查看答案及解析
-
硼、铝属元素周期表IIIA短周期元素。回答下列问题:
(1)基态B原子的价电子轨道表达式为__________,其第一电离能比Be ________(填“大”或“小”)。
(2)氨硼烷(NH3BH3)是最具潜力的储氢材料之一,分子中存在配位键,能体现配位键的结构式为__________,与氨硼烷互为等电子体的烃的分子式为__________。
(3)插图
(4)插图
(5)插图
(3)常温常压下硼酸晶体为结构层状,其二维平面结构如图所示:
硼酸的化学式为__________,B原子的杂化类型为_______。从氢键的角度解释硼酸在冷水中的溶解度小而加热时溶解度增大:_____________________________________。
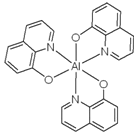
(4)8-羟基喹啉铝是一种黄色粉末,它是OLED中的重要发光材料及电子传输材料,其微观结构如图所示,8-羟基喹啉铝中存在的化学键为______________。
A.金属键 B.极性键 C.非极性键 D.配位键 E.π键
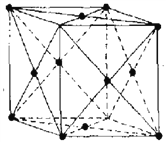
(5)金属铝晶体中原子呈面心立方紧密堆积(如上图)。该晶胞空间利用率为_________________(用含π的代数式表示);铝的密度是2.7g•cm-3,阿伏伽德罗常数为NA,依此可计算出Al原子半径r(Al)=__________cm.
高三化学综合题困难题查看答案及解析
-
硼及其化合物应用广泛。回答下列问题:
(1)基态B原子的价电子轨道表达式为________,其第一电离能比Be ________(填“大”或“小”)。
(2)氨硼烷(NH3BH3)被认为是最具潜力的新型储氢材料之一,分子中存在配位键,提供孤电子对的成键原子是________,写出一种与氨硼烷互为等电子体的分子________(填化学式)。

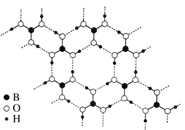
(3)常温常压下硼酸(H3BO3)晶体结构为层状,其二维平面结构如图a。
① B原子的杂化方式为________。从氢键的角度解释硼酸在冷水中的溶解度小而加热时溶解度增大:________。
② 路易斯酸碱理论认为,任何可接受电子对的分子或离子叫路易斯酸,任何可给出电子对的分子或离子叫路易斯碱。从结构角度分析硼酸是路易斯酸:________。
(4)立方氮化硼(BN)是特殊的耐磨和切削材料,其晶胞结构与金刚石相似,如图b所示。
① 与氮原子直接连接的硼原子构成的几何形状为________。硼原子和氮原子所连接的最小环为________元环。
② 晶胞有两个基本要素:
原子坐标参数,表示晶胞内部各原子的相对位置。如图b所示,其中原子坐标参数X为(0,0,0),Y原子的坐标参数为(1/2,0,1/2),则Z原子的坐标参数为________。
晶胞参数,描述晶胞的大小和形状。已知立方氮化硼的密度为d g∙cm-3,阿伏加德罗常数值为NA,则晶胞参数a=________nm。(列出计算式即可)
高三化学简答题困难题查看答案及解析
-
硼及其化合物应用广泛。回答下列问题:
(1)基态B原子的价电子轨道表达式为________,其第一电离能比Be ________(填“大”或“小”)。
(2)氨硼烷(NH3BH3)被认为是最具潜力的新型储氢材料之一,分子中存在配位键,提供孤电子对的成键原子是________,写出一种与氨硼烷互为等电子体的分子________(填化学式)。
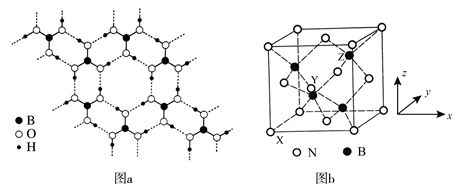
(3)常温常压下硼酸(H3BO3)晶体结构为层状,其二维平面结构如图a。
① B原子的杂化方式为________。从氢键的角度解释硼酸在冷水中的溶解度小而加热时溶解度增大:________。
② 路易斯酸碱理论认为,任何可接受电子对的分子或离子叫路易斯酸,任何可给出电子对的分子或离子叫路易斯碱。从结构角度分析硼酸是路易斯酸:________。
(4)立方氮化硼(BN)是特殊的耐磨和切削材料,其晶胞结构与金刚石相似,如图b所示。
① 与氮原子直接连接的硼原子构成的几何形状为________。硼原子和氮原子所连接的最小环为________元环。
② 晶胞有两个基本要素:
原子坐标参数,表示晶胞内部各原子的相对位置。如图b所示,其中原子坐标参数X为(0,0,0),Y原子的坐标参数为(1/2,0,1/2),则Z原子的坐标参数为________。
晶胞参数,描述晶胞的大小和形状。已知立方氮化硼的密度为d g∙cm-3,阿伏加德罗常数值为NA,则晶胞参数a=________nm。(列出计算式即可)
高三化学简答题困难题查看答案及解析
-
硼及其化合物应用广泛。回答下列问题:
(1)基态B原子的价电子轨道表达式为________,其第一电离能比Be ________(填“大”或“小”)。
(2)氨硼烷(NH3BH3)被认为是最具潜力的新型储氢材料之一,分子中存在配位键,提供孤电子对的成键原子是________,写出一种与氨硼烷互为等电子体的分子________(填化学式)。

(3)常温常压下硼酸(H3BO3)晶体结构为层状,其二维平面结构如图a。
① B原子的杂化方式为________。从氢键的角度解释硼酸在冷水中的溶解度小而加热时溶解度增大:________。
② 路易斯酸碱理论认为,任何可接受电子对的分子或离子叫路易斯酸,任何可给出电子对的分子或离子叫路易斯碱。从结构角度分析硼酸是路易斯酸:________。
(4)立方氮化硼(BN)是特殊的耐磨和切削材料,其晶胞结构与金刚石相似,如图b所示。
① 与氮原子直接连接的硼原子构成的几何形状为________。硼原子和氮原子所连接的最小环为________元环。
② 晶胞有两个基本要素:
原子坐标参数,表示晶胞内部各原子的相对位置。如图b所示,其中原子坐标参数X为(0,0,0),Y原子的坐标参数为(1/2,0,1/2),则Z原子的坐标参数为________。
晶胞参数,描述晶胞的大小和形状。已知立方氮化硼的密度为d g∙cm-3,阿伏加德罗常数值为NA,则晶胞参数a=________nm。(列出计算式即可)
高三化学简答题困难题查看答案及解析
-
(15分)氨基甲酸铵(H2NCOONH4)是一种白色固体,易分解、易水解,可用做肥料、灭火剂、洗涤剂等。某化学兴趣小组用如下方法制备氨基甲酸铵,反应的化学方程式如下:
2NH3(g)+CO2(g)
H2NCOONH4(s) ΔH<0
(1)实验室通常采用图1装置制取氨气,你所选择的试剂是 。
(2)制备氨基甲酸铵的装置如图2所示,把氨气和二氧化碳通入四氯化碳中,不断搅拌混合,生成的氨基甲酸铵小晶体悬浮在四氯化碳中。当悬浮物较多时,停止制备。
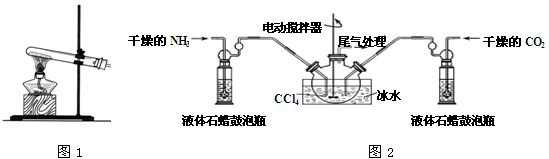
注:四氯化碳与液体石蜡均为惰性介质。
①发生器用冰水冷却的原因是 。
液体石蜡鼓泡瓶的作用是 。
②从反应后的混合物中分离出产品的实验方法 (填操作名称)。为了得到干燥产品,应采取的方法是________(填写选项序号)。
a.常压加热烘干 b.高压加热烘干 c.真空40 ℃以下烘干
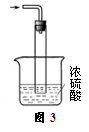
③尾气处理装置如图3所示。能否将浓H2SO4改为稀H2SO4 (填“能”或“否”),理由是 。
(3)取因部分变质而混有碳酸氢铵的氨基甲酸铵样品1.570 g,用足量石灰水充分处理后,使碳元素完全转化为碳酸钙,过滤、洗涤、干燥,测得质量为2.000 g。则样品中氨基甲酸铵的质量分数为_______。
[Mr(NH2COONH4)=78、Mr(NH4HCO3) =79、Mr(CaCO3)=100]
高三化学填空题困难题查看答案及解析
-
NH3中氢原子可被锂原子替代。亚氨基锂(Li2NH)是一种良好的固体储氢材料,其储氢原理可表示为Li2NH+H2→LiNH2+LiH。下列有关说法正确的是
A.Li2NH中N的化合价为-1
B.此法储氢和钢瓶储氢的原理相同
C.LiH中的阳离子半径大于阴离子半径
D.该反应中H2既是氧化剂又是还原剂
高三化学选择题中等难度题查看答案及解析