-
亚硝酸钠是一种防腐剂和增色剂,但在食品中过量时会对人体产生危害。其在酸性条件下会产生NO和NO2。下列有关说法错误的是
A.NaNO2既具有氧化性又具有还原性
B.食用“醋溜豆芽”可能会减少亚硝酸钠对人体的危害
C.NaNO2和胃酸作用的离子方程式为:2NO2-+2H+=NO↑+NO2↑+H2O
D.1 mol NaNO2在酸性条件下完全反应生成NO和NO2,转移电子的物质的量为1 mol
高三化学选择题中等难度题查看答案及解析
-
亚硝酸钠是一种防腐剂和增色剂,但在食品中过量时会对人体产生危害。其在酸性条件
下会产生NO和NO2。下列有关说法错误的是( )
A.NaNO2既具有氧化性又具有还原性
B.食用“醋溜豆芽”可能会减少亚硝酸钠对人体的危害
C.NaNO2和胃酸作用的离子方程式为:2NO2—+2H+=NO↑+NO2↑+H2O
D.1 mol NaNO2在酸性条件下完全反应生成NO和NO2,转移电子的物质的量为1 mol
高三化学单选题中等难度题查看答案及解析
-
亚硝酸钠是一种防腐剂和增色剂,但在食品中过量时会对人体产生危害。其在酸性条件下会产生NO和NO2。下列有关说法错误的是( )
A.NaNO2既具有氧化性又具有还原性
B.食用“醋溜豆芽”可能会减少亚硝酸钠对人体的危害
C.NaNO2和胃酸作用的离子方程式为:
D.1 mol NaNO2在酸性条件下完全反应生成NO和NO2,转移电子的物质的量为1 mol
高三化学选择题中等难度题查看答案及解析
-
亚硝酸钠是一种防腐剂和增色剂,但在食品中过量时会对人体产生危害。其在酸性条件
下会产生NO和NO2。下列有关说法错误的是( )
A.NaNO2既具有氧化性又具有还原性
B.食用“醋溜豆芽”可能会减少亚硝酸钠对人体的危害
C.NaNO2和胃酸作用的离子方程式为:
2NO2—+2H+=NO↑+NO2↑+H2O
D.1 mol NaNO2在酸性条件下完全反应生成NO和NO2,转移电子的物质的量为1 mol
高三化学选择题中等难度题查看答案及解析
-
亚硝酸钠广泛用于印染、漂白等行业,在建筑行业用作防冻剂,在食品工业作防腐剂和增色剂,它是一种潜在致癌物质,过量或长期食用对人产生危害,由于亚硝酸钠有咸味,外观与NaCl相似,曾多次发生被当食盐误食的事件。某化学兴趣小组以碳和浓硝酸为起始原料,设计如下装置,利用一氧化氮与过氧化钠反应制备亚硝酸钠。(夹持装置和A中加热装置已略,气密性已检验),
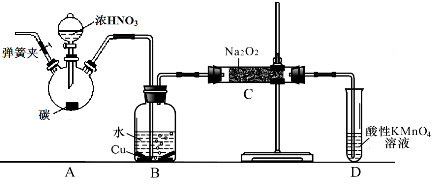
查阅资料:①HNO2为弱酸,室温下存在反应3HNO2=HNO3+2NO↑+H2O;
②NO2-能被很多常见的强氧化剂氧化,如在酸性溶液中可将MnO4-还原为Mn2+且无气体生成。
③NO不与碱反应,可被酸性KMnO4溶液氧化为硝酸
④HNO2在酸性溶液也是一种氧化剂,如能把I-氧化成I2。
⑤AgNO2是一种难溶于水易溶于酸的白色化合物。
(1)写出C中制备亚硝酸钠反应的化学方程式(反应物的物质的量之比为2:1) 。
(2)D装置的作用是 。
(3)经检验C产物中亚硝酸钠含量较少。甲同学认为C中产物不仅有亚硝酸钠,还有碳酸钠和氢氧化钠。为排除干扰甲同学在B、C装置间增加装置E,E中盛放的试剂应是________(写名称)。
(4)人体正常的血红蛋白中含Fe2+。若误食亚硝酸盐(如NaNO2),则导致血红蛋白中Fe2+转化为Fe3+而中毒,服用维生素C可解毒。下列叙述不正确的是 。
A.亚硝酸盐是还原剂 B.维生素C是还原剂
C.维生素C将Fe3+还原为Fe2+ D.亚硝酸盐被还原
(5)能用来鉴别NaNO2和NaCl的方法是
A .测溶液pH法
B.加酸法
C.AgNO3和HNO3两种试剂法
D.加KI淀粉(酸性)法
E.以上四种方法都可
(6)某同学把溴水加到NaNO2溶液观察到溴水褪色,请写出此反应的离子方程式 。
高三化学实验题困难题查看答案及解析
-
亚硝酸钠广泛用于印染、漂白等行业,在建筑行业用作防冻剂,在食品工业作防腐剂和增色剂,它是一种潜在致癌物质,过量或长期食用对人产生危害,由于亚硝酸钠有咸味,外观与NaCl相似,曾多次发生被当食盐误食的事件。某化学兴趣小组以碳和浓硝酸为起始原料,设计如下装置,利用一氧化氮与过氧化钠反应制备亚硝酸钠。(夹持装置和A中加热装置已略,气密性已检验)

查阅资料:
①HNO2为弱酸,室温下存在反应3HNO2==HNO3+2NO↑+H2O;
②NO2-能被很多常见的强氧化剂氧化,如在酸性溶液中可将MnO4-还原为Mn2+且无气体生成。
③NO不与碱反应,可被酸性KMnO4溶液氧化为硝酸
④HNO2在酸性溶液也是一种氧化剂,如能把I-氧化成I2。
⑤AgNO2是一种难溶于水易溶于酸的白色化合物。
(1)写出C中制备亚硝酸钠反应的化学方程式(反应物的物质的量之比为2:1)________________________________________________________________________________________________________ 。
(2)D装置的作用是________________________________________________________________________________________________________ 。
(3)经检验C产物中亚硝酸钠含量较少。甲同学认为C中产物不仅有亚硝酸钠,还有碳酸钠和氢氧化钠。为排除干扰甲同学在B、C装置间增加装置E,E中盛放的试剂应是________(写名称)。
(4)人体正常的血红蛋白中含Fe2+。若误食亚硝酸盐(如NaNO2),则导致血红蛋白中Fe2+转化为Fe3+而中毒,服用维生素C可解毒。下列叙述不正确的是________________________________________。
A亚硝酸盐是还原剂
B维生素C是还原剂
C维生素C将Fe3+还原Fe2+
D亚硝酸盐被还原
(5)能用来鉴别NaNO2和NaCl的方法是
A 测溶液pH法
B.加酸法
C.AgNO3和HNO3两种试剂法
D.加KI淀粉(酸性)法
E.以上四种方法都可
(6)某同学把溴水加到NaNO2溶液观察到溴水褪色,请写出此反应的离子方程式________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________ 。
高三化学实验题困难题查看答案及解析
-
亚硝酸钠(NaNO2)与食盐形态一样,是一种常用的食品添加剂,具有防腐和增色作用,过量食用会引起中毒。餐饮服务单位应加强对亚硝酸钠等食品添加剂的使用管
理。某一反应体系反应物和生成物共六种物质:NaNO2、H2O、NO、I2、NaI、HI。已知该反应中NaNO2只发生了如下过程:NaNO2→NO。请回答下列问题:
(1)该反应的氧化剂是 (填化学式)。
(2)写出并配平该反应的化学方程式,并用单线桥法标出电子转移的方向和数目: 。
(3)若有0.25mol的氧化剂被还原,则被氧化的还原剂的物质的量为 。
(4)误食NaNO2会导致血红蛋白中Fe2+转化为Fe3+而中毒,服用维生素C可以解除NaNO2的中毒。下列关于上述中毒、解毒过程的说法中,正确的是 (填序号)。
A.NaNO2是还原剂 B.维生素C是还原剂
C.维生素C能把Fe2+氧化为Fe3+ D.NaNO2被氧化
(5)根据上述反应,可以用试纸和生活中常见的物质进行实验,来鉴别NaNO2和NaCl溶液,可选用的
物质有①自来水 ②淀粉碘化钾试纸 ③淀粉 ④白糖 ⑤食醋 ⑥白酒。进行实验时,必须选用的物质有 (填序号)。
高三化学填空题困难题查看答案及解析
-
亚硝酸钠(NaNO2)是一种常用的食品添加剂,具有防腐和增色作用。下列对亚硝酸钠性质的分析中,不合理的是( )
A.亚硝酸钠中含有钠元素,焰色反应呈黄色
B.已知亚硝酸为弱酸,则亚硝酸钠溶液呈碱性
C.亚硝酸钠属于盐类物质,其水溶液能与金属钾反应生成金属钠
D.亚硝酸钠中氮元素的化合价为+3,亚硝酸钠既具有氧化性又具有还原性
高三化学选择题简单题查看答案及解析
-
脱氢醋酸钠是FAO和WHO认可的一种安全型食品防霉、防腐保鲜剂,它是脱氢醋酸的钠盐。脱氢醋酸的一种制备方法如图,下列说法错误的是
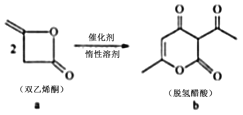
A.a分子中所有原子处于同一平面 B.a.b均能使酸性 KMnO4溶液褪色
C.a.b均能与 NaOH溶液发生反应 D.b与
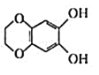 互为同分异构体
互为同分异构体高三化学单选题简单题查看答案及解析
-
亚硝酸钠(NaNO2)是重要的防腐剂。某实验小组以如图所示的装置和试剂,通过反应制备亚硝酸钠 (部分夹持装置略)。
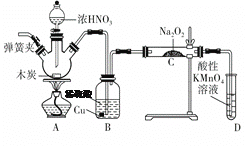
已知:室温下,①2NO+Na2O2===2NaNO2;
②酸性条件下,NO或NO2都能与MnO4-反应生成NO3-和Mn2+。
完成下列填空:
(1)写出A中三种主要玻璃仪器的名称 __________ ,___________,_________。
(2)写出浓硝酸与木炭反应的化学方程式:_______________________。
(3)B中观察到的主要现象是有无色气体产生和______________,D装置的作用是___________________________。
(4)经检验C产物中除亚硝酸钠外还含有副产物碳酸钠和氢氧化钠,为避免产生这些副产物,应在B、C装置间增加装置,则该装置中盛放的药品名称是________。
(5)若NO2可以全部转化成NO,将1.56 g过氧化钠完全转化成为亚硝酸钠,理论上至少需要木炭________g。
高三化学综合题简单题查看答案及解析