将氯气通入一定温度的溶液中,得到含有次氯酸钾、氯酸钾和氯化钾的混合溶液。若反应过程中转移
个电子,所得溶液中
则参与反应的
的物质的量为
A. B.
C.
D.
高三化学选择题中等难度题
将氯气通入一定温度的溶液中,得到含有次氯酸钾、氯酸钾和氯化钾的混合溶液。若反应过程中转移
个电子,所得溶液中
则参与反应的
的物质的量为
A. B.
C.
D.
高三化学选择题中等难度题
将氯气通入一定温度的溶液中,得到含有次氯酸钾、氯酸钾和氯化钾的混合溶液。若反应过程中转移
个电子,所得溶液中
则参与反应的
的物质的量为
A. B.
C.
D.
高三化学选择题中等难度题查看答案及解析
将氯气通入一定温度的溶液中,得到含有次氯酸钾、氯酸钾和氯化钾的混合溶液。若反应过程中转移
个电子,所得溶液中
则参与反应的
的物质的量为( )
A. B.
C.
D.
高三化学选择题简单题查看答案及解析
高三化学选择题中等难度题查看答案及解析
洁厕灵和84消毒液混合使用会发生反应:,生成有毒的氯气。NA代表阿伏加德罗常数的值,下列说法正确的是
A.每生成氯气,转移的电子数为2NA
B.含有的电子数为28NA
C.溶液中含有的次氯酸根离子数为0.2NA
D.将分子总数为NA的和
的混合气体置于标准状况下,其体积约为
高三化学单选题中等难度题查看答案及解析
NA为阿伏伽德罗常数的值。下列说法正确的是
A. 2gD2O中含有质子数、中子数、电子数均为NA
B. 0.1mol氯酸钾与足量浓盐酸反应生成氯气转移电子数为0.6NA
C. 1L 0.1mol·L-1 NaHSO4溶液中含有的阳离子数目为0.1NA
D. 标准状况下,2.24L SO2与足量氧气充分反应,生成SO3的分子数为0.1NA
高三化学单选题困难题查看答案及解析
用浓盐酸和氯酸钾固体反应制备氯气时,发现所得的气体颜色偏深,经分析该气体主要含有Cl2和ClO2两种气体,某研究性学习小组拟用如图所示装置分离制得的混合气体,并测定两种气体的物质的量之比。

[资料信息]
常温下二氧化氯是黄绿色气体,熔点-59.5℃,沸点11.0℃,能溶于水,不溶于浓硫酸、四氯化碳,有强氧化性,能与NaOH溶液反应生成等物质的量的两种盐,其中一种为氯酸钠。
[制备与分离]
(1)实验过程中加药品前应进行的操作是______________ 。
(2)装置C、E的作用分别是:______________________;________________________。
(3)根据信息写出ClO2与NaOH溶液的离子方程式为_________________________________。
[测量与计算]:
反应结束后,打开止水夹鼓入过量氮气,再测得B、C装置分别增重2.0g和14.2g,将D中的液体溶于水,配成2.5L溶液,取25.00mL该溶液,调节试样的pH<2.0,加入足量的KI晶体,振荡后,静置片刻;加入指示剂X,用0.2000mol/L Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液25.00mL。(已知:2ClO2 + 8H+ + 10I- = 5I2 + 2Cl- + 4H2O;2Na2S2O3 + I2 = Na2S4O6 +2NaI)
(4)鼓入氮气的目的是 ______________________________。指示剂X为_________,滴定终点时溶液的颜色变化是________________________。
(5)D装置收集到的ClO2的物质的量为________。
[结论] 由实验测量可知,浓盐酸和氯酸钾固体反应的化学方程式为________________。
高三化学实验题困难题查看答案及解析
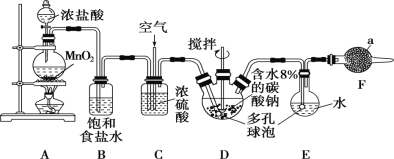
Cl2O为国际公认的高效安全灭菌消毒剂之一,实验室可利用氯气和空气(氯气与空气体积比为1∶3,空气不参与反应)的混合气与含水8%的碳酸钠反应制备,并用水吸收Cl2O制备次氯酸溶液,所用实验装置和Cl2O的性质如下:
| 颜色 | 棕黄色 |
| 状态 | 气体 |
| 气味 | 强刺激性 |
| 熔点 | -116 ℃ |
| 沸点 | 3.8 ℃ |
| 水溶性 | 极易溶于水,与水反应生成次氯酸 |
| 热稳定性 | 42 ℃以上分解为Cl2和O2 |
(1)仪器a的名称为________,所盛放的药品是________。
(2)写出装置A中发生反应的离子方程式:_______________。
(3)装置C的主要作用是___________。
(4)装置D、E中都用到多孔球泡,其作用是____________。
(5)写出装置D中Cl2与过量碳酸钠反应生成Cl2O的化学方程式:________。
(6)装置E采用棕色圆底烧瓶的原因是____________。
(7)制备Cl2O装置中存在缺陷,请提出改进措施:___________。
高三化学实验题中等难度题查看答案及解析
在一定温度下,氯气与NaOH溶液反应可生成NaCl、NaClO和NaClO3。下列判断不正确的是( )
A.若反应过程中消耗2mol氯气,则转移电子数目可能为3NA
B.反应停止后n(NaClO):n(NaCl):n(NaClO3)可能为1:6:1
C.氯气与氢氧化钠反应过程中消耗氯气与NaOH的物质的量之比一定为1:2
D.若氢氧化钠与氯气恰好完全反应,则反应后所得溶液中总是存在:c(Na+)=c(Cl-)+c(ClO-)+c(ClO3-)
高三化学单选题困难题查看答案及解析
高三化学选择题中等难度题查看答案及解析
将一定量的氯气通入30mL浓度为10.00mol/L的氢氧化钠浓溶液中,加热少许时间后溶液中形成氯化钠、次氯酸钠、氯酸钠共存体系。下列判断正确的是
A.与氢氧化钠反应的氯气为0.16mol
B.n(Na+):n(Cl-)可能为7:3
C.若反应中转移的电子为nmol,则0.15<n<0.25
D.n(NaCl):n(NaClO):n(NaClO3)可能为11:2:1
高三化学选择题困难题查看答案及解析