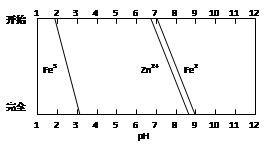-
(16分)铁酸锌(ZnFe2O4)是对可见光敏感的半导体催化剂,其实验室制备原理为:
Zn2++2Fe2++3C2O42-+6H2O ZnFe2(C2O4)3·6H2O↓…………(a)
ZnFe2(C2O4)3·6H2O↓…………(a)
ZnFe2(C2O4)3·6H2O  ZnFe2O4 + 2CO2↑+4CO↑+6H2O …………(b)
ZnFe2O4 + 2CO2↑+4CO↑+6H2O …………(b)
已知:ZnC2O4和FeC2O4难溶于水。
(1)上述制备原理中不属于氧化还原反应的是 (选填:“a”或“b”)。
(2)制备ZnFe2(C2O4)3·6H2O时,可选用的药品有:
Ⅰ.(NH4)2Fe(SO4)2·6H2O
Ⅱ.ZnSO4·7H2O
Ⅲ.(NH4)2C2O4·7H2O。
①称量药品时,必须严格控制n(Fe2+)/n (Zn2+)= 。
②选用的加料方式是 (填字母)。
a.按一定计量比,Ⅰ、Ⅱ、Ⅲ同时加入反应器并加水搅拌,然后升温至75℃。
b.按一定计量比,Ⅰ、Ⅲ同时加入反应器加水配成溶液,然后加入Ⅱ,再升温到75℃。
c.按一定计量比,将Ⅰ、Ⅱ混合并配成溶液甲,Ⅲ另配成溶液乙,甲、乙同时加热到
75℃,然后将乙溶液缓慢加入甲溶液中,并持续搅拌。
(3)从溶液中分离出ZnFe2(C2O4)3·6H2O需过滤、洗涤。已洗涤完全的依据是 。
(4)ZnFe2(C2O4)3·6H2O热分解需用酒精喷灯,还用到的硅酸盐质仪器有 。
(5)某化学课外小组拟用废旧干电池锌皮(含杂质铁),结合下图信息从提供的试剂中选取适当试剂,制取纯净的ZnSO4·7H2O。
实验步骤如下:
①将锌片完全溶于稍过量的3mol·L-1稀硫酸,加入 (选填字母,下同)。
A.30%H2O2 B.新制氯水 C.FeCl3溶液 D.KSCN溶液
②加入 。
A.纯锌粉 B.纯碳酸钙粉末 C.纯ZnO粉末 D.3mol·L-1稀硫酸
③加热到60℃左右并不断搅拌。
④趁热过滤得ZnSO4溶液,再蒸发浓缩、冷却结晶,过滤、洗涤、干燥。
其中步骤③加热的主要目的是 。
-
铁酸锌(ZnFe2O4)是对可见光敏感的半导体催化剂,其实验室制备原理为:
Zn2++2Fe2++3C2O42-+6H2O ZnFe2(C2O4)3·6H2O↓……………(a)
ZnFe2(C2O4)3·6H2O↓……………(a)
ZnFe2(C2O4)3·6H2O  ZnFe2O4+2CO2↑+4CO↑+6H2O ……………(b)
ZnFe2O4+2CO2↑+4CO↑+6H2O ……………(b)
(1)上述制备原理中属于氧化还原反应的是(选填:“a”或“b”)。
(2)制备ZnFe2(C2O4)3·6H2O时,可选用的药品有:
Ⅰ、(NH4)2Fe(SO4)2·6H2O,Ⅱ、ZnSO4·7H2O及Ⅲ、(NH4)2C2O4·7H2O。
①称量药品时,必须严格控制n(Fe2+)/n(Zn2+)=________。
②选用的加料方式是________(填字母)。
a.按一定计量比,Ⅰ、Ⅱ、Ⅲ同时加入反应器并加水搅拌,然后升温至75℃。
b.按一定计量比,Ⅰ、Ⅲ同时加入反应器加水配成溶液,然后加入Ⅱ,然后升温到75℃。
c.按一定计量比,将Ⅰ、Ⅱ混合并配成溶液甲,Ⅲ另配成配制溶液乙,甲、乙同时加热到75℃,然后将乙溶液缓慢加入甲溶液中,并持续搅拌。
(3)从溶液中分离出ZnFe2(C2O4)3·6H2O需过滤、洗涤。已洗涤完全的依据是________。
(4)ZnFe2(C2O4)3·6H2O热分解需用酒精喷灯,还用到的硅酸盐质仪器有________和________。
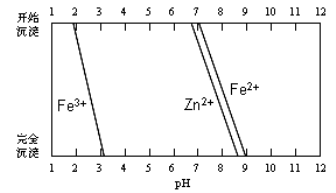
(5)某化学课外小组拟用废旧干电池锌皮(含杂质铁),结合下图信息利用实验可提供的试剂制取纯净的ZnSO4溶液。

实验中可选用的试剂如下:
(a)30%H2O2;(b)新制氯水;
(c)1.0 mol·L-1NaOH溶液;
(d)3mol·L-1稀硫酸;
(e)纯ZnO粉末;
(f)纯锌粉。
实验步骤依次为:①将锌片完全溶于稍过量的3mol·L-1稀硫酸,加入________(选填字母,下同);②加入________;③加热到60℃左右并不断搅拌;
④过滤得ZnSO4溶液。其中步骤③加热的主要目的有________。
-
铁酸锌(ZnFe2O4)是对可见光敏感的半导体催化剂,其实验室制备原理为:
Zn2++2Fe2++3C2O42-+6H2O ZnFe2(C2O4)3·6H2O↓……………(a)
ZnFe2(C2O4)3·6H2O↓……………(a)
ZnFe2(C2O4)3·6H2O  ZnFe2O4 + 2CO2↑+4CO↑+6H2O ……………(b)
ZnFe2O4 + 2CO2↑+4CO↑+6H2O ……………(b)
(1)上述制备原理中属于氧化还原反应的是 (选填:“a”或“b”)。
(2)制备ZnFe2(C2O4)3·6H2O时,可选用的药品有:
Ⅰ、(NH4)2Fe(SO4)2·6H2O,Ⅱ、ZnSO4·7H2O及Ⅲ、(NH4)2C2O4·7H2O。
①称量药品时,必须严格控制n(Fe2+)/n(Zn2+)=。
②选用的加料方式是 (填字母)。
a.按一定计量比,Ⅰ、Ⅱ、Ⅲ同时加入反应器并加水搅拌,然后升温至75℃。
b.按一定计量比,Ⅰ、Ⅲ同时加入反应器加水配成溶液,然后加入Ⅱ,然后升温到75℃。
c.按一定计量比,将Ⅰ、Ⅱ混合并配成溶液甲,Ⅲ另配成溶液乙,甲、乙同时加热到75℃,然后将乙溶液缓慢加入甲溶液中,并持续搅拌。
(3)从溶液中分离出ZnFe2(C2O4)3·6H2O需过滤、洗涤。已洗涤干净的依据是 _________________。
(4)ZnFe2(C2O4)3·6H2O热分解需用酒精喷灯,还用到的硅酸盐质仪器有: 和 。
(5)某化学课外小组拟用废旧干电池锌皮(含杂质铁),结合下图信息利用实验可提供的试剂制取纯净的ZnSO4溶液。实验中可选用的试剂如下:
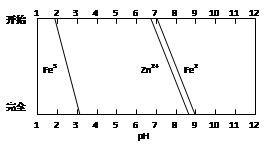
a.30%H2O2;
b.新制氯水;
c.1.0 mol·L-1NaOH溶液;
d.3 mol·L-1稀硫酸;
e.纯ZnO粉末;
f.纯锌粉。
实验步骤依次为:①将锌片完全溶于稍过量的3 mol·L-1稀硫酸,加入 (选填字母,下同);②加入 ;③加热到60℃左右并不断搅拌;④过滤得ZnSO4溶液。其中步骤③加热的主要目的有 。
-
(16分)铁酸锌(ZnFe2O4)是对可见光敏感的半导体催化剂,其实验室制备原理为:
Zn2++2Fe2++3C2O42-+6H2O ZnFe2(C2O4)3·6H2O↓ (a)
ZnFe2(C2O4)3·6H2O↓ (a)
ZnFe2(C2O4)3·6H2O  ZnFe2O4 + 2CO2↑+4CO↑+6H2O (b)
ZnFe2O4 + 2CO2↑+4CO↑+6H2O (b)
已知:ZnC2O4和FeC2O4难溶于水。
(1)上述制备原理中不属于氧化还原反应的是 (选填:“a”或“b”)。
(2)制备ZnFe2(C2O4)3·6H2O时,可选用的药品有:
Ⅰ.(NH4)2Fe(SO4)2·6H2O Ⅱ.ZnSO4·7H2O Ⅲ.(NH4)2C2O4·7H2O。
①称量药品时,必须严格控制n(Fe2+)/n (Zn2+)= 。
②选用的加料方式是 (填字母)。
a.按一定计量比,Ⅰ、Ⅱ、Ⅲ同时加入反应器并加水搅拌,然后升温至75℃。
b.按一定计量比,Ⅰ、Ⅲ同时加入反应器加水配成溶液,然后加入Ⅱ,再升温到75℃。
c.按一定计量比,将Ⅰ、Ⅱ混合并配成溶液甲,Ⅲ另配成溶液乙,甲、乙同时加热到75℃,然后将乙溶液缓慢加入甲溶液中,并持续搅拌。
(3)从溶液中分离出ZnFe2(C2O4)3·6H2O需过滤、洗涤。已洗涤完全的依据是 。
(4)ZnFe2(C2O4)3·6H2O热分解需用酒精喷灯,还用到的硅酸盐质仪器有 。
(5)某化学课外小组拟用废旧干电池锌皮(含杂质铁),结合下图信息从提供的试剂中选取适当试剂,制取纯净的ZnSO4·7H2O。

实验步骤如下:
①将锌片完全溶于稍过量的3mol·L-1稀硫酸,加入 (选填字母,下同)。
A.30%H2O2 B.新制氯水 C.FeCl3溶液 D.KSCN溶液
②加入 。
A.纯锌粉 B.纯碳酸钙粉末 C.纯ZnO粉末 D.3mol·L-1稀硫酸
③加热到60℃左右并不断搅拌。
④趁热过滤得ZnSO4溶液,再蒸发浓缩、冷却结晶,过滤、洗涤、干燥。
其中步骤③加热的主要目的是 。
-
铁酸锌(ZnFe2O4)是对可见光敏感的半导体催化剂,其实验室制备原理为:
①ZnSO4+2FeSO4+3Na2C2O4+6H2O ZnFe2(C2O4)3·6H2O↓+3Na2SO4
ZnFe2(C2O4)3·6H2O↓+3Na2SO4
②ZnFe2(C2O4)3·6H2O ZnFe2O4+2CO2 ↑+4CO↑+6H2O
ZnFe2O4+2CO2 ↑+4CO↑+6H2O
回答下列问题:
(1)基态 Fe2+的价层电子排布图为___________.
(2)电离能大小比较:I1(Zn)___________ I1(Cu),I2(Zn)___________ I2 (Cu) (填“>”“<”或“=”)。
(3)Na2SO4 中阴离子的空间构型是___________,该离子中 S 的杂化类型是_____。
(4)CO和N2的分子结构相似,标准状况下,VLCO2和CO的混合气体中含键的物质的量为___________。与CO2互为等电子体的离子有____________(写一种即可)。
(5)ZnCl2、ZnBr2、ZnI2 的熔点依次为283℃、394℃、446℃,其主要原因是___________。
(6)铁和碳组成的某种晶体的晶胞如图所示。面心上铁原子相连构成正八面体。
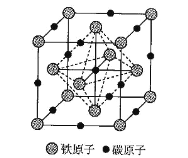
已知该晶体的密度为 dg·cm-3,NA 是阿伏加德罗常数的值。
①该晶体中Fe、C原子的最简比为___________。
②该晶胞中相邻两个面心上铁原子最近的核间距离 D=___________nm(只列计算式)。
-
K3[Fe(C2O4)3]·3H2O(三草酸合铁酸钾)为亮绿色晶体,易溶于水,难溶于乙醇,是制备负载型活性铁催化剂的主要原料。实验室用莫尔盐[(NH4)2Fe(SO4)2·6H2O]制备K3[Fe(C2O4)3]·3H2O具体流程如图:
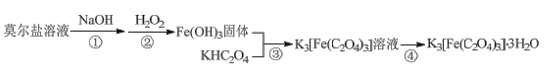
回答下列问题:
(1)步骤②滴加过量6%H2O2,生成红褐色胶状沉淀,该反应的化学方程式为___。生成的沉淀不易过滤,过滤前需要的操作是___。
(2)步骤③将Fe(OH)3加入到KHC2O4溶液中,水浴加热,控制pH为3.5-4,若pH偏高应加入适量___(填“H2C2O4”或“K2C2O4”)。
(3)步骤④的操作是___、过滤。得到的晶体依次用少量冰水、95%乙醇洗涤,用95%乙醇洗涤的目的是___。
(4)测定K3[Fe(C2O4)3]·3H2O中铁的含量。
①称量mg样品于锥形瓶中,溶解后加稀H2SO4酸化,用cmol·L-1KMnO4溶液滴定至终点。滴定反应的氧化产物为___。滴定时,盛放高锰酸钾溶液的仪器是___(“酸式”或“碱式”)滴定管。
②向上述溶液中加入过量锌粉至将铁元素全部还原为Fe2+后,过滤、洗涤,将滤液及洗涤液全部收集到锥形瓶中。加稀H2SO4酸化,用cmol·L-1KMnO4溶液滴定至终点,消耗KMnO4溶液VmL。该样品中铁的质量分数的表达式为___。
-
草酸合铁(III)酸钾晶体[K3[Fe(C2O4)3]·3H2O]是制备负载型活性铁催化剂的主要原料。某科研团队以硫酸亚铁铵晶体[(NH4)2Fe(SO4)2·6H2O]为原料制备草酸合铁(III)酸钾晶体的具体流程如图:
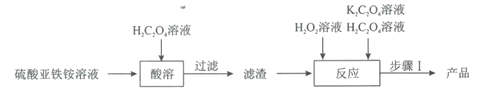
回答下列问题:
(1)配制100mL1.00mol·L-1的硫酸亚铁铵溶液。溶液配制过程中需用到的玻璃仪器除烧杯、玻璃棒、量筒外,还有___。在配制时需加入适量稀硫酸的目的是___。
(2)取12.5mL硫酸亚铁铵溶液于烧杯中,水浴加热至100℃,缓缓滴入饱和H2C2O4溶液,有黄色沉淀(FeC2O4·2H2O)生成,反应的离子方程式为___。
(3)在“酸溶”操作中,需保持溶液的pH为3.5,溶液中 =___。(H2C2O4的Ka1=10-1.25,Ka2=10-4.27)。
=___。(H2C2O4的Ka1=10-1.25,Ka2=10-4.27)。
(4)在“反应”中,先维持40℃水浴加热,滴加10mL6%H2O2溶液,一段时间后,再微沸2min;然后冷却,继续交替滴加H2C2O4和K2C2O4溶液直至溶液呈亮绿色。维持40℃水浴加热使最终所得产品产率最高的原因是__,溶液微沸的目的是__。
(5)经“步骤I”结晶、抽滤、洗涤、避光干燥,最终得到产品5.45g,产品的产率为____(保留1位小数)。
(6)草酸合铁(I)酸钾晶体为光敏配合物,应避光保存,光照时会发生光化学分解反应生成草酸钾和草酸亚铁,同时有气体生成,反应的化学方程式为___。
-
以下物质的制备原理错误的是
A.无水氯化镁的制备:MgCl2·6H2O MgCl2+ 6H2O
MgCl2+ 6H2O
B.钴的制备:3Co3O4+8Al 9Co+4Al2O3
9Co+4Al2O3
C.烧碱的制备:2NaCl+2H2O 2NaOH +H2↑+ Cl2↑
2NaOH +H2↑+ Cl2↑
D.漂粉精的制备: 2Ca(OH)2 + 2Cl2→Ca(ClO)2+CaCl2+2H2O
-
以下物质的制备原理错误的是
A.无水氯化镁的制备 :MgCl2·6H2O MgCl2+ 6H2O
MgCl2+ 6H2O
B.钴的制备:3Co3O4+8Al 9Co+4Al2O3
9Co+4Al2O3
C.烧碱的制备:2NaCl+2H2O 2NaOH +H2↑+ Cl2↑
2NaOH +H2↑+ Cl2↑
D.漂粉精的制备: 2Ca(OH) 2 + 2Cl2 Ca(ClO) 2 +CaCl2+2H2O
Ca(ClO) 2 +CaCl2+2H2O
-
高铁酸钾(K2FeO4)是一种常用的水处理剂。工业制备高铁酸钾的离子方程式为:3C1O-+10OH-+2Fe3+═2FeO42-+3C1-+5H2O。下列相关叙述不合理的是( )
A.K2FeO4中铁元素的化合价是+6
B.制得1molK2FeO4转移3mole-
C.Fe3+的氧化性强于FeO42-的氧化性
D.氧化产物和还原产物物质的量之比为2:3
ZnFe2(C2O4)3·6H2O↓……………(a)
ZnFe2O4+2CO2↑+4CO↑+6H2O ……………(b)