-
(15分)无水硫酸铜在强热下会发生分解反应:

用下图所示装置(夹持仪器已略去),根据D管在反应前后的质量差计算出分解了的无水硫酸铜的质量。

实验步骤:
①称量反应前D管的质量。
②连接好装置,关闭K,加热硬质玻璃管A一段时间后,停止加热。
③待硬质玻璃管A冷却后,打开K,通入一段时间的已除去二氧化碳等酸性气体的空气。
④再称量D管,得其反应前后的质量差为m。
回答下列问题:
(1) 2SO3(g)  2SO2(g) + O2(g) 该反应的平衡常数表达式为K=________________________。
2SO2(g) + O2(g) 该反应的平衡常数表达式为K=________________________。
(2) B管中除温度明显升高外,还可看到的现象是________________________,而温度明显升高的主要原因是________________________;B管中发生的有关离子方程式是________________________。
(3)步骤③中通一段时间已除去二氧化碳等酸性气体的空气的目的是________________________。
(4)按上述方法实验,假设B、C、D对气体的吸收均完全,并忽略空气中CO2的影响,能否根据m计算出分解了的无水CuSO4的质量?(任选其一回答)
①如果能,则分解的无水CuSO4的质量为________________________(用m表示)。
②如果不能,则原因是________________________。为了能测得分解了的无水硫酸铜的质量,你的简单实验方案是________________________。
-
(13分)无水硫酸铜在强热下会发生分解反应:
CuSO4  CuO + SO3↑ 2SO3
CuO + SO3↑ 2SO3  2SO2↑+ O2↑
2SO2↑+ O2↑
用下图所示装置(夹持仪器已略去),根据D管在反应前后的质量差计算出分解了的无水硫酸铜的质量。
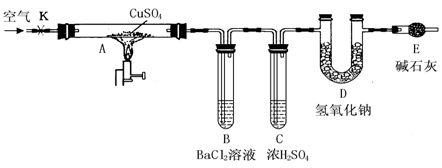
实验步骤:
①称量反应前D管的质量。
②连接好装置,关闭K,加热硬质玻璃管A一段时间后,停止加热。
③待硬质玻璃管A冷却后,打开K,通入一段时间的已除去二氧化碳等酸性气体的空气。
④再称量D管,得其反应前后的质量差为m。
回答下列问题:
(1) 2SO3(g)  2SO2(g) + O2(g) 该反应的平衡常数表达式为K=________________________。
2SO2(g) + O2(g) 该反应的平衡常数表达式为K=________________________。
(2) B管中除温度明显升高外,还可看到的现象是________________________,而温度明显升高的主要原因是________________________;B管中发生反应的有关离子方程式是________________________。
(3)仪器E的作用是________________________。
(4)按上述方法实验,假设B、C、D对气体的吸收均完全,并忽略空气中CO2的影响,能否根据m计算出分解了的无水CuSO4的质量?(任选其一回答)
①如果能,则分解的无水CuSO4的质量为________________________(用m表示)。
②如果不能,则原因是________________________。为了能测得分解了的无水硫酸铜的质量,你的简单实验方案是________________________。
-
(13分)无水硫酸铜在强热下会发生分解反应:
CuSO4  CuO + SO3↑ 2SO3
CuO + SO3↑ 2SO3  2SO2↑+ O2↑
2SO2↑+ O2↑
用下图所示装置(夹持仪器已略去),根据D管在反应前后的质量差计算出分解了的无水硫酸铜的质量。

实验步骤:
①称量反应前D管的质量。
②连接好装置,关闭K,加热硬质玻璃管A一段时间后,停止加热。
③待硬质玻璃管A冷却后,打开K,通入一段时间的已除去二氧化碳等酸性气体的空气。
④再称量D管,得其反应前后的质量差为m。
回答下列问题:
(1) 2SO3(g)  2SO2(g) + O2(g) 该反应的平衡常数表达式为K=________________________。
2SO2(g) + O2(g) 该反应的平衡常数表达式为K=________________________。
(2) B管中除温度明显升高外,还可看到的现象是________________________,而温度明显升高的主要原因是________________________;B管中发生反应的有关离子方程式是________________________。
(3)仪器E的作用是________________________。
(4)按上述方法实验,假设B、C、D对气体的吸收均完全,并忽略空气中CO2的影响,能否根据m计算出分解了的无水CuSO4的质量?(任选其一回答)
①如果能,则分解的无水CuSO4的质量为________________________(用m表示)。
②如果不能,则原因是________________________。为了能测得分解了的无水硫酸铜的质量,你的简单实验方案是________________________。
-
无水硫酸铜在强热下会发生分解反应:
CuSO4  CuO + SO3↑ 2SO3
CuO + SO3↑ 2SO3  2SO2↑+ O2↑
2SO2↑+ O2↑
用下图所示装置(夹持仪器已略去),根据D管在反应前后的质量差计算出分解了的无水硫酸铜的质量。

实验步骤:
①称量反应前D管的质量。
②连接好装置,关闭K,加热硬质玻璃管A一段时间后,停止加热。
③待硬质玻璃管A冷却后,打开K,通入一段时间的已除去二氧化碳等酸性气体的空气。
④再称量D管,得其反应前后的质量差为m。
回答下列问题:
(1)反应2SO3(g)  2SO2(g) + O2(g) 的平衡常数表达式为K=________。
2SO2(g) + O2(g) 的平衡常数表达式为K=________。
(2)B管中除温度明显升高外,还可看到的现象是________,而温度明显升高的主要原因是________;B管中发生反应的有关离子方程式是________。
(3)仪器E的作用是________。
(4)按上述方法实验,假设B、C、D对气体的吸收均完全,并忽略空气中CO2的影响,能否根据m计算出分解了的无水CuSO4的质量?(任选其一回答)
①如果能,则分解的无水CuSO4的质量为________(用m表示)。
②如果不能,则原因是________。为了能测得分解了的无水硫酸铜的质量,你的简单实验方案是________。
-
(15分)某化学研究小组探究无水三草酸合铁酸钾K3[Fe(C2O4)3]受热分解的产物,并对所得气体产物和固体产物进行验证,按下图装置进行实验(夹持仪器已略去)。
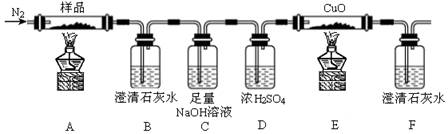
(1)连接好装置后,加入药品前,应该进行的实验操作是________________(填操作名称)。
(2)实验开始时缓缓通入氮气,过一段时间以后,加热反应管A和E ,待反应完全后,停止加热,仍继续通氮气,直到反应管冷却。停止加热前是否需要先断开A、B的连接处和E、F的连接处?为什么?_______________________________________________________________。
(3)实验中观察到B中澄清石灰水变浑浊,则说明气体产物中有________(写化学式)。
能证明分解产物中有CO气体生成的实验现象是________。
(4)该小组同学查阅资料后得知,固体产物中不存在+3价Fe元素,而盐类物质只有K2CO3。
① 验证固体产物中钾元素存在的方法是,现象是________。
② 研究小组为探究铁元素的存在形式,取A中充分反应后所得固体于试管中,加入足量蒸馏水,过滤、洗涤、干燥得到黑色粉末,取4.4g黑色粉末溶于足量稀硝酸中,收集到标准状况下NO气体1.12L通过计算判断黑色粉末的成分为________(写化学式)。写出黑色粉末溶于足量稀硝酸发生反应的离子方程式________。
-
某学习小组探究氨的还原性及检验产物的性质,按下图装置进行实验(夹持仪器已略去).将B处的Cr2O3加热至红热,再鼓入空气,已知:无水CaCl2可吸收氨气和水 回答下列问题:
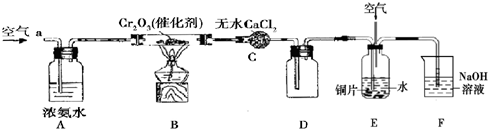
(1)B中发生反应的化学方程式是________.
(2)证明氨气发生了催化氧化的现象是________,发生反应的方程式是________.
(3)E中铜发生反应的离子方程式是________.
(4)E中缓缓通入空气的目的是________.
(5)氨作为燃料电池燃气时发生的总反应为4NH3+3O2=2N2+6H2O,该燃料电池以KOH溶液为电解质溶液,负极反应式是________.
-
由一种短周期金属元素和一种非金属元素组成的化合物X可与水发生复分解反应。某校兴趣小组用如图装置(夹持装置略去)对其进行探究实验。
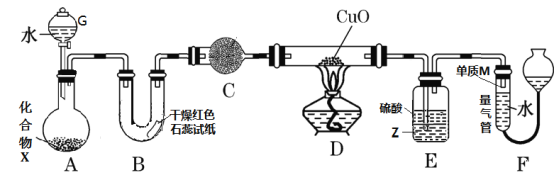
(1)仪器G的名称是_____________________,B中红色石蕊试纸变蓝,则单质M的电子式为___________________。
(2)化合物X中金属元素和非金属元素质量比为69:14,写出X与水反应的化学方程式:_________________________________。
(3)C中的试剂名称为___________________________。
(4)实验时,装置D中硬质玻璃管内的现象为_________________________。
(5)裝置E中试剂Z为___________(填化学式),装置E的作用是_________________。
(6)若不通过E、F两装置,请设计实验方案证明D中发生了反应(不通过观察D
中固体颜色发生变化)________________________________________ 。
(7)若装置A中固体样品含有杂质(杂质不参与反应),某同学通过测定F中单质M在标准状况下的体积和固体样品的质量,以确定固体样品中X的质量分数,判断该方案是否可行,并说明原因:_________________________________________________________________________________________。
-
由一种短周期金属元素和一种非金属元素组成的化合物X可与水发生复分解反应。某校兴趣小组用如图装置(夹持装置略去)对其进行探究实验。
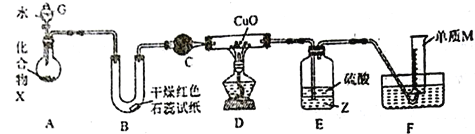
(1)仪器G的名称是_____________________,B中红色石蕊试纸变蓝,则单质M的电子式为___________________。
(2)化合物X中含组成单质M的元素质量分数为16.9%,写出X与水反应的化学方程式:_____________________________。
(3)C中的试剂名称为___________________________。
(4)实验时,装置D中硬质玻璃管内的现象为_________________________。
(5)裝置E中试剂Z为___________(填化学式),装置E的作用是_________________________。
(6)若不通过E、F两装置,请设计实验方案证明D中发生了反应(不通过观察D中固体颜色发生变化):__________________________________________________。
(7)若装置A中固体样品含有杂质(杂质不参与反应),某同学通过测定F中单质M在标准状况下的体积和固体样品的质量,以确定固体样品中X的质量分数,判断该方案是否可行,并说明原因:__________________________________________________。
-
(10分)为测定乙炔的相对分子质量,某小组利用下图所示装置进行试验(夹持仪器已略去,气密性已检验)。

(1)小组查阅资料得出:乙炔能与硫酸酸化的KMnO4反应生成Mn2+和CO2,该反应的化学方程式是________。
(2)在装置A中使用饱和食盐水而不直接滴加水的原因________。
(3)B中的CuSO4溶液用于除去乙炔中混有的H2S、PH3、AsH3等气体,CuSO4溶液除H2S气体的反应类型是________(基本反应)。
(4)实验前D中含有x mol KMnO4的酸性溶液,实验时向D中通入一定量的乙炔直至KMnO4酸性溶液恰好完全褪色,实验完毕后装置D及E的总质量共增重y g,通过计算求出所测乙炔的相对分子质量(用含字母x、y的代数式表示):__________(不写计算过程)。
(5)若该小组的实验原理及所有操作都正确,下列因素中,对所测乙炔相对分子质量的值不会产生影响的是________。
A.将装置A中产生的混合气体直接通入D中的KMnO4酸性溶液
B.将E装置(盛有碱石灰的干燥管)换成盛有浓硫酸的洗气瓶
C.通入过量纯净的乙炔气体于KMnO4酸性溶液时,有部分乙炔未被氧化而逸出
(6)另一活动小组的同学认为上述实验装置仍存在不足,则改进的措施是______________。
-
无水CuSO4在一定条件下发生如下反应:

有人设计通过实验测定反应生成的SO3、SO2和O2,并经过计算确定该条件下分解反应方程式各物质的化学计量数,实验所需仪器装置如图所示。

实验测得数据及有关结果如下:
①准确称量无水CuSO4 6.0g。
②测出量筒中水的体积后,折算成排水的气体在标准状况下的体积为280ml。
③干燥管中的质量在实验结束时增加了3.2g。
④实验结束时,装置F中的溶液变成Na2SO4溶液(不含其他杂质)。
请回答如下问题:
已知气体从左向右的流向,上述仪器装置接口的连接顺序是a →ji→f e →c d →h g→ b
(1)装置F的作用是_____________________,装置D的作用是_______________________。
(2)首先应计算的物质是______________。
通过计算推断,该条件下反应的化学方程式是_____________________________。
(3);(填序号)____________。

2SO2(g) + O2(g) 该反应的平衡常数表达式为K=________________________。









