-
在一个体积为5 L的真空密闭容器中加入1.25 mol CaCO3,发生反应CaCO3 (s) CaO(s) +CO2(g),测得平衡时二氧化碳的物质的量浓度随温度的变化关系如图所示:
CaO(s) +CO2(g),测得平衡时二氧化碳的物质的量浓度随温度的变化关系如图所示:
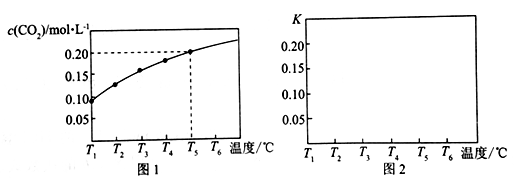
请按要求回答下列问题:
(1)该反应正反应为__________热反应(填“吸”或“放”),温度为T5℃时,该反应耗时40s达到平衡,则T5℃时,该反应的平均反应速率为________________。
(2)T2℃时,该反应已经达到平衡,下列措施中能使该反应的平衡常数K值变大的是_______________(选填编号)。
a.减小压强 b.减少CaO的量 c.加入CaCO3 d.升高温度
(3)请在如图中画出平衡常数K随温度的变化曲线_______________。
(4)在T5℃下,维持温度和容器体积不变,向上述平衡体系中再充入1molN2,则最后平衡时容器中的CaCO3的质量为________g。
-
在密闭容器中加入CaSO4和CO,在一定温度下,发生反应:CaSO4(s)+CO(g)  CaO(s)+SO2(g)+CO2(g) ΔH=+218.4 kJ·mol-1
CaO(s)+SO2(g)+CO2(g) ΔH=+218.4 kJ·mol-1
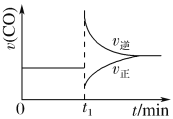
CO的反应速率随时间变化如图所示。下列说法正确的是( )
A.该反应是吸热反应,升高温度,正反应速率增大,逆反应速率减小
B.CaO是固态,不能用CaO表示反应的快慢
C.图示中t1时改变的条件可能是减小c(CO),同时增大c(SO2)
D.图示中t1时改变的条件可能是增大压强
-
一定条件下,在体积为VL的密闭容器中,发生反应mA+nB=pC,t秒末,A减少了1.0mol,B减少了1.25mol,C增加了0.5mol,则m:n:p为( )
A.2:5:4
B.4:5:2
C.1:3:2
D.1:4:5
-
在一个固定体积的密闭容器中加入2mol A,发生可逆反应:2A(g)
 2B(g)+C(g).该反应达到平衡的标志是( )
2B(g)+C(g).该反应达到平衡的标志是( )
A.容器内压强是开始时的1.5倍
B.容器内A、B、C物质的量浓度之比为2:2:1
C.单位时间消耗0.2molA同时生成0.1molC
D.容器内各物质的浓度不随时间变化
-
在一个固定体积的密闭容器中加入2mol A,发生可逆反应2A(g)  2B(g)+C(g)。该反应达到平衡的标志是( )
2B(g)+C(g)。该反应达到平衡的标志是( )
A.容器内压强是开始时的1.5倍
B.容器内A、B、C物质的量浓度之比为2∶2∶1
C.单位时间消耗0.2molA同时生成0.1molC
D.容器内各物质的浓度不随时间变化
-
在一个固定体积的密闭容器中加入2mol A,发生可逆反应2A(g)  2B(g)+C(g)。该反应达到平衡的标志是
2B(g)+C(g)。该反应达到平衡的标志是
A.容器内压强是开始时的1.5
B.容器内A、B、C物质的量浓度之比为2∶2∶1
C.单位时间消耗0.2molA,同时生成0.1molC
D.容器内各物质的浓度不随时间变化
-
在一个固定体积的密闭容器中加入2mol A,发生可逆反应:
2A(g)  2B(g)+C(g)。该反应达到平衡的标志是
2B(g)+C(g)。该反应达到平衡的标志是
A.容器内压强是开始时的1.5倍
B.容器内A、B、C物质的量浓度之比为2∶2∶1
C.单位时间消耗0.2molA同时生成0.1molC
D.容器内各物质的浓度不随时间变化
-
一定条件下,在体积为VL的密闭容器中,发生反应mA+nB=pC,t秒末,A减少了
1.0mol,B减少了1.25mol,C增加了0.5mol,则m: n:p为
A.2:5:4 B.4:5:2 C.1:3:2 D.1:4:5
-
在真空密闭容器中盛有1mol PCl5发生反应PCl5(气)⇌PCl3(气)+Cl2(气)达平衡后,PCl5所占体积分数为a%,若在同一温度和同一容器中,最初投入的是3mol PCl5,反应达平衡,PCl5体积分数为b%,则a b关系正确的是( )
A.a大于b
B.a小于b
C.a等于b
D.无法比较
-
在体积均为1.0L的恒容密闭容器中加入足量的相同的碳粉,再分别加入0.1 mol CO2和0.2 mol CO2,在不同温度下反应CO2 (g)+C(s)  2CO(g)达到平衡,平衡时CO2的物质的量浓度c(CO2)随温度的变化如图所示(图中I、II、III点均处于曲线上)。下列说法正确的是
2CO(g)达到平衡,平衡时CO2的物质的量浓度c(CO2)随温度的变化如图所示(图中I、II、III点均处于曲线上)。下列说法正确的是

A. 反应CO2(g)+c(s) 2CO(g) △H<0
2CO(g) △H<0
B. 体系的总压强P总:P总(状态Ⅱ) 2P总(状态III)
2P总(状态III)
C. 体系中c(CO):6c(CO,状态I)<c(CO,状态II)
D. 从状态I到状态III的升温过程中,每一时刻,正逆反应速率:υ逆>υ正
CaO(s) +CO2(g),测得平衡时二氧化碳的物质的量浓度随温度的变化关系如图所示:


