-
电石中的碳化钙和水能完全反应:CaC2+2H2O=C2H2↑+Ca(OH)2使反应产生的气体排水,测量排出水的体积,可计算出标准状况下乙炔的体积,从而可测定电石中碳化钙的含量。
(1)若用下列仪器和导管组装实验装置
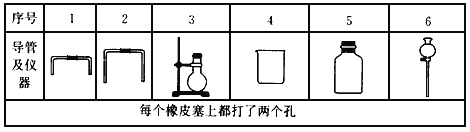
如果所制气体流向从左向右时,上述仪器和导管从左到右直接连接的顺序(填各仪器、导管的序号)是:____接____接____接____接____接____。
(2)仪器连接好后,进行实验时,有下列操作(每项操作只进行一次):
①称取一定量电石,置于仪器3中,塞紧橡皮塞。
②检查装置的气密性。
③在仪器6和5中注入适量水。
④待仪器3恢复到室温时,量取仪器4中水的体积(导管2中的水忽略不计)。
⑤慢慢开启仪器6的活塞,使水逐滴滴下,至不产生气体时,关闭活塞。
正确的操作顺序(用操作编号填写)是__________________。
(3)若实验产生的气体有难闻气味,且测定结果偏大,这是因为电石中含有___________杂质。
(4)若实验时称取的电石1.60g,测量排出水的体积后,折算成标准状况乙炔的体积为448mL,此电石中碳化钙的质量分数是_________%。
-
电石的主要成分为CaC2,易与水反应生成C2H2,故C2H2俗称电石气。某同学设计如下方案测定电石中CaC2的纯度(杂质不参加反应)。

实验原理:CaC2 +2H2O==Ca(OH)2+C2H2 ↑
通过测定生成的气体的体积(标准状况),可确定样品中CaC2的含量。
实验步骤:
①称取样品1.2g;
②把1.2g样品放入气密性良好的气体发生装置,如图所示;
③向样品中滴入水,至不再产生气泡,用量筒排水集气,量筒内液面在360mL处恰与水槽内液面相平;
④作为反应器的烧瓶中有24mL液体。
请回答下列问题:
(1)上述实验所用的玻璃仪器有导管、水槽 、、________、________。
(2)若实验前有1000 mL、500 mL、250 mL的量筒备用,则应选用________ mL的量筒。
(3)生成气体体积是 ________________ mL,为保证生成气体体积的准确性,读取量筒刻度时应注意的问题是________ 。
(4)若将C2H2通入KMnO4溶液中,KMnO4溶液的紫红色会变浅,反应的化学方程式为□KMnO4+□C2H2+□H2SO4——□K2SO4+□MnSO4+□CO2+□________。若该实验生成的 C2H2完全被KMnO4溶液氧化,至少需0.1 mol·L-1的KMnO4溶液________mL。
(5)通过以上数据计算,可得样品中CaC2的纯度为 。
-
(15分)电石的主要成分为CaC2,易与水反应生成C2H2,故C2H2俗称电石气。某同学设计如下方案测定电石中CaC2的纯度(杂质不参加反应)。
实验原理:CaC2+2H2O=Ca(OH)2+C2H2↑
通过测定生成的气体的体积(标准状况),可确定样品中CaC2的含量。
实验步骤:
①取样品1.2g;
②把1.2 g样品放入气密性良好的气体发生装置,如图所示;
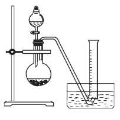
③向样品中滴入水,至不再产生气泡,用量筒排水集气,量筒内液面在360mL处恰与水槽内液面相平
④作为反应器的烧瓶中有24 mL液体。
请回答下列问题:
(1)上述实验所用的玻璃仪器有导管、水槽、 、 、 。
(2)若实验前有1000 mL、500 mL、250 mL的量筒备用,则应选用 mL的量筒。
(3)生成气体体积是 mL,为保证生成气体体积的准确性,读取量筒刻度时应注意的问题是 。
(4)若将C2H2通入KMnO4溶液中,KMnO4溶液的紫红色会变浅,配平并完成化学方程式
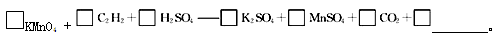
若该实验生成的C2H2完全被KMnO4溶液氧化,至少需0.1 mol • L-1的KMnO4溶液 mL。
(5)通过以上数据计算,可得样品中CaC2的纯度为 。
-
现有含CaO杂质的CaC2试样.某研究性学习小组的同学拟用以下三种方案测定CaC2试样的纯度(固体电石--CaC2与水可快速反应生成难溶于水的C2H2,反应方程式为:CaC2+2H2O→Ca(OH)2+C2H2↑).请填写下列空白:
Ⅰ、第一种方案:请从图中选用适当的装置,设计一个实验,测定CaC2试样的纯度.
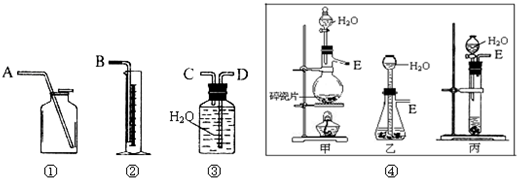
(1)制取C2H2最好选④中的______.所选用装置的连接顺序是(填各接口A~E的顺序):______.
(2)若实验时称取的试样为1.4g,产生的乙炔在标准状况下的体积为448mL,此试样中CaC2的质量分数为______.
Ⅱ、第二种方案:根据试样和水在锥形瓶中反应前后质量的变化,测定CaC2的质量分数.先称取试样1.6g、锥形瓶和水的质量为195.0g,再将试样加入锥形瓶中,反应过程中每隔相同时间测得的数据如下表:
| 读数次数 | 质量/g |
锥形瓶十水十试样 | 第1次 | 196.4 |
| 第2次 | 196.2 |
| 第3次 | 196.1 |
| 第4次 | 196.0 |
| 第5次 | 196.0 |
(3)计算CaC2的质量分数时,必需用的数据是______.不必作第6次读数的原因是______.
Ⅲ、第三种方案:称取一定质量的试样(1.6g),操作流程如下:

(4)操作Ⅱ的名称是______.
(5)要测定CaC2试样的纯度,还需知道的数据是______.
(6)在转移溶液时,如溶液转移不完全,则CaC2质量分数的测定结果______(填“偏大”、“偏小”或“不变”).
-
气体A(C2H2) 是无色、难溶于水的气体,实验室常用CaC2(块状固体)和水在常温下反应制备:CaC2+2H2O→Ca(OH)2(微溶)+C2H2↑。下列有关实验室制备A的叙述不正确的是( )
A.用如图所示装置 可以制A B.制A肯定可以用启普发生器
可以制A B.制A肯定可以用启普发生器
C.用排水法收集到的A较纯 D.用排空气法收集到的A密度偏小
-
大多金属碳化物能与水剧烈反应,生成相应氢氧化物和气态烃,如:Na4C+4H2O→4NaOH+CH4↑, MgC2+2H2O→Mg(OH)2+C2H2↑
现有CaC2与某常见金属碳化物A的混合物,与足量盐酸反应,得一澄清溶液,并有大量气体产生,将气体通过碱石灰干燥除杂后,测其体积为V1,将所得气体充分燃烧,生成的CO2的体积为V2,相同条件下,V1:V2=5:7:向澄清溶液中逐渐加入足量Na2CO3溶液后,再继续加入NaOH溶液,沉淀物质的量变化如下图所示,试回答下列问题:
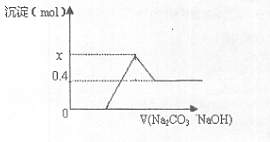
(1)已知A中的金属元素是短周期元素,则该元素是:(写元素符号),写出CaC2与浓盐酸反应的化学方程式:;
(2)根据Vl:V2=5:7,可算出混合烃中平均每Imol烃分子含有____mol C,由此可知气态混合烃中含有乙炔和________,
(3)A的化学式为________;
(4)原混合物中CaC2的物质的量为mol, A的质量为________g。
-
Ⅰ.现有含CaO杂质的CaC2试样。设计以下实验,测定CaC2试样的纯度。(反应方程式为:CaC2+2H2O→Ca(OH)2+C2H2↑),请从下图中选用适当的装置,完成该实验。
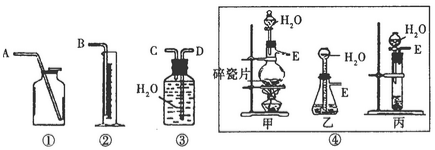
(1)制取C2H2最好选④中的_________装置(填“甲”“乙”或“丙”),所选用装置的连接顺序是_________________。(填各接口A~E的顺序)
(2)若实验时称取的试样为1.4 g,产生的乙炔在标准状况下的体积为448 mL,此试样中CaC2的质量分数为____________。(保留3位有效数字)
Ⅱ.某同学在实验室从如图标签的试剂瓶中取少许钠进行燃烧实验,实验后发现还有少许黑色固体生成。从反应物及实验操作猜测:

该黑色物质可能为炭与另一种氧化物组成的混合物。根据题意和图示回答下面问题:
(1)装置图⑤中A的名称_______________。
(2)此氧化物可能是___________或___________(写化学式)。
(3)对黑色固体物质的组成作如图⑥所示探究

①实验I加入盐酸溶液的目的是________________。
②仅通过实验Ⅱ,用最简步骤能快速确定黑色氧化物的组成,请完善该设计。(限选试剂:稀盐酸、KSCN溶液、10%H2O2溶液)

-
I、现有含CaO杂质的CaC2试样。设计以下实验,测定CaC2试样的纯度。(反应方程式为:CaC2+2H2O→Ca(OH)2+C2H2↑),请从下图中选用适当的装置,完成该实验。
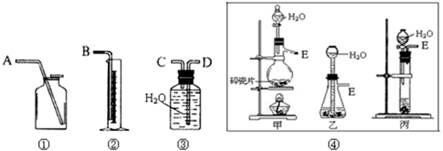
(1)制取C2H2最好选④中的 装置(填“甲”“乙”或“丙”),所选用装置的连接顺序是 (填各接口A~E的顺序)。
(2)若实验时称取的试样为1.4g,产生的乙炔在标准状况下的体积为448mL,此试样中CaC2的质量分数为 。(保留3为有效数字)

II、某同学在实验室从如图标签的试剂瓶中取少许钠进行燃烧实验,实验后 发现还有少许黑色固体生成。从反应物及实验操作猜测:
该黑色物质可能为碳与另一种氧化物组成的混合物。
根据题意和图示回答下面问题:
(1)装置图⑤中A的名称 。
(2)此氧化物可能是 或 (写化学式)。
(3)对黑色固体物质的组成作如图⑥所示研究

①实验I中加入盐酸溶液的目的是 。
②仅通过实验II,用最简步骤能快速确定黑色氧化物的组成,请完善该设计。(限选试剂:稀盐酸、KSCN溶液、10%H2O2溶液)
| 实验操作 | 预期现象与结论 | 相关离子方程式 |
| 取少量实验I中的澄清溶液,加入试剂 | | |
-
下图是制备和研究乙炔的性质实验装置图。下列说法不正确的是
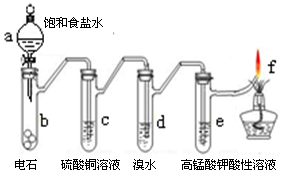
A. 制备乙炔的反应原理是CaC2+2H2O  Ca(OH) 2+C2H2↑
Ca(OH) 2+C2H2↑
B. c的作用是除去影响后续实验的杂质
C. d中的有机产物与AgNO3溶液混合能产生沉淀
D. e中的现象说明乙炔能被高锰酸钾酸性溶液氧化
-
下图是制备和研究乙炔性质的实验装置图。下列说法不正确的是
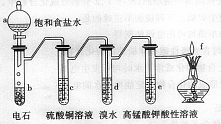
A.制备乙炔的反应原理是CaC2+2H2O→Ca(OH)2+C2H2↑
B.c的作用是除去影响后续实验的杂质
C.d中的有机产物与AgNO3溶液混合能产生沉淀
D.e中的现象说明乙炔能被高锰酸钾酸性溶液氧化



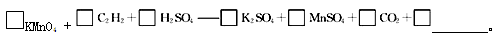


 可以制A B.制A肯定可以用启普发生器
可以制A B.制A肯定可以用启普发生器








