(6分)
(1)在微生物作用的条件下,NH4+经过两步反应被氧化成NO3—。两步反应的能量变化示意图如下:
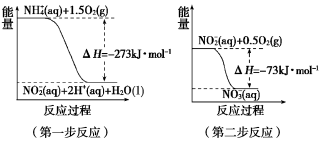
1 mol NH4+ (aq) 全部氧化成NO3—(aq)的热化学方程式是_______________。
(2)、电解NO制备 NH4NO3,其工作原理如图所示,
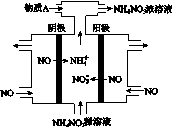
写出该电解池的电极反应式
阳极: __________________________ 阴极:________________________________
高三化学填空题中等难度题
(6分)
(1)在微生物作用的条件下,NH4+经过两步反应被氧化成NO3—。两步反应的能量变化示意图如下:

1 mol NH4+ (aq) 全部氧化成NO3—(aq)的热化学方程式是_______________。
(2)、电解NO制备 NH4NO3,其工作原理如图所示,

写出该电解池的电极反应式
阳极: __________________________ 阴极:________________________________
高三化学填空题中等难度题
在微生物作用的条件下,NH4+经过两步反应被氧化成NO3-。这两步的能量变化示意图如下:
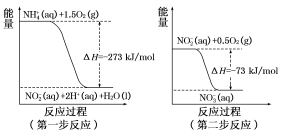
(1)第二步反应是 反应(选填“放热”或“吸热”),判断依据是 。
(2)1 mol NH4+ (aq)全部氧化成NO2- (aq)的热化学方程式是 。
高三化学填空题中等难度题查看答案及解析
(6分)
(1)在微生物作用的条件下,NH4+经过两步反应被氧化成NO3—。两步反应的能量变化示意图如下:

1 mol NH4+ (aq) 全部氧化成NO3—(aq)的热化学方程式是_______________。
(2)、电解NO制备 NH4NO3,其工作原理如图所示,

写出该电解池的电极反应式
阳极: __________________________ 阴极:________________________________
高三化学填空题中等难度题查看答案及解析
(I)某氮肥厂氨氮废水中的氮元素多以NH4+和NH3·H2O的形式存在。在微生物作用下,NH4+经过两步反应被氧化成NO3-,两步反应的能量变化示意图如下:

(1)1molNH4+(aq)全部氧化成NO3-(aq)的热化学方程式是________。
(2)在一定条件下,向废水中加入CH3OH,将HNO3还原成N2,若该反应消耗32gCH3OH转移6mol电子,则参加反应的还原剂和氧化剂的物质的量之比是________。
(Ⅱ)超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层。科学家正在研究利用催化技术将尾气中的NO和CO转变成CO2和N2,化学方程式如下:
2NO+2CO2CO2+N2 △H
某温度下用气体传感器测得不同的时间的NO和CO浓度如下表:
| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| C(NO)(×10-4mol·L-1) | 10.0 | 4.50 | 2.50 | 1.50 | 1.00 | 1.00 |
| C(CO)(×10-3mol·L-1) | 3.60 | 3.05 | 2.85 | 2.75 | 2.70 | 2.70 |
请回答下列问题(均不考虑温度变化对催化剂催化效率的影响):
(1)在上述条件下反应能够自发进行,则反应的△H________0(填写“>”、“<”、“=”)
(2)前2s内的平均反应速率v(N2)=________;
(3)在该温度下,反应的平衡常数K=________(只写出计算结果);
(4)某同学设计了三组实验,分别验证温度、催化剂比表面积对化学反应速率的影响规律,部分实验条件如下表:
| 实验编号 | T/℃ | NO初始浓度/mol·L-1 | CO初始浓度/mol·L-1 | 催化剂的比表面积/m2·g-1 |
| I | 280 | 1.20×10-3 | 5.80×10-3 | 82 |
| II | 280 | 1.20×10-3 | 5.80×10-3 | 124 |
| III | 350 | 1.20×10-3 | 5.80×10-3 | 124 |
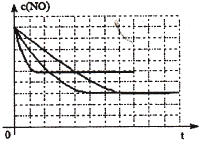
该同学画出了表中三个实验条件下,混合气体中NO浓度随时间变化的趋势曲线图,请在图上标明各条曲线的实验编号;
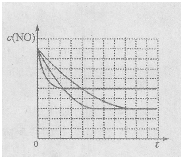
(5)有人认为:催化剂比表面积增大,会提高NO和CO的反应效率,从而使污染物NO和CO的转化率提高。请用化学基本理论对此观点进行评价:________。
高三化学填空题中等难度题查看答案及解析
(I某氮肥厂氨氮废水中的氮元素多以NH4+和NH3·H2O的形式存在。在微生物作用下,NH4+经过两步反应被氧化成NO3-,两步反应的能量变化示意图如下:

(1)1 mo1NH4+(aq)全部氧化成NO3-(aq)的热化学方程式是 _________。
(2)在一定条件下,向废水中加入CH3OH,将HNO3还原成 N2,若该反应消耗32gCH3OH转移6mol电子,则参加反应的还原剂和氧化剂的物质的量之比是_________。
(B)超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层。科学家正在研究利用催化技术
将尾气中的NO和CO转变成CO2和N2,化学方程式如下:2NO十2CO2CO2+ N2 △H
某温度下用气体传感器测得不同的时间的NO和CO浓度如下表:
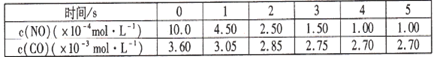
请回答下列问题(均不考虑温度变化对催化剂催化效率的影响):
(1)在上述条件下反应能够自发进行,则反应的△H________0(填写“>”、“<”、“=”)
(2)在该温度下,反应的平衡常数K=________(只写出计算结果);
(3)某同学设计了三组实验,分别验证温度、催化剂比表面积对化学反应速率的影响规律,
部分实验条件如下表:

该同学画出了表中三个实验条件下,混合气体中NO浓度随时间变化的趋势曲线图,请在图上标明各条曲线的实验编号;
高三化学填空题极难题查看答案及解析
(1)在微生物作用的条件下,NH经过两步反应被氧化成NO3-。两步反应的能量变化示意图如下:
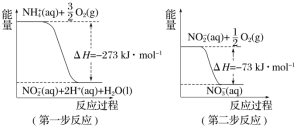
①第一步反应是_______(填“放热”或“吸热”)反应,判断依据是_______________。
②1 mol NH (aq)全部氧化成NO3-(aq)的热化学方程式是_________________________。
(2)已知红磷比白磷稳定,则反应P4(白磷,s)+5O2(g)===2P2O5(s) ΔH1;4P(红磷,s)+5O2(g)===2P2O5(s) ΔH2;ΔH1和ΔH2的关系是ΔH1________ΔH2(填“>”、“<”或“=”)。
(3)在298 K、101 kPa时,已知:2H2O(g)===O2(g)+2H2(g) ΔH1;Cl2(g)+H2(g)===2HCl(g) ΔH2;2Cl2(g)+2H2O(g)===4HCl(g)+O2(g) ΔH3
则ΔH3与ΔH1和ΔH2之间的关系正确的是________。
A.ΔH3=ΔH1+2ΔH2 B.ΔH3=ΔH1+ΔH2 C.ΔH3=ΔH1-2ΔH2 D.ΔH3=ΔH1-ΔH2
(4)已知:2CO(g)+O2(g)===2CO2(g) ΔH=-566 kJ·mol-1①,Na2O2(s)+CO2(g)===Na2CO3(s)+1/2O2(g) ΔH=-226 kJ·mol-1,②,则CO(g)与Na2O2(s)反应放出509 kJ热量时,电子转移数目为_______________。
(5)已知H2(g)+Br2(l)===2HBr(g) ΔH=-72 kJ·mol-1,蒸发1 mol Br2(l)需要吸收的能量为30 kJ,其他相关数据如下表:
| 物质 | H2(g) | Br2(g) | HBr(g) |
| 1 mol分子中的化学键断裂时需要吸收的能量(kJ) | 436 | 200 | a |
则表中a=________。
高三化学解答题困难题查看答案及解析
氨氮废水中的氮元素多以NH4+和NH3·H2O的形式存在,在一定条件下,NH4+经过两步反应被氧化成NO3¯,两步反应的能量变化示意图如下:
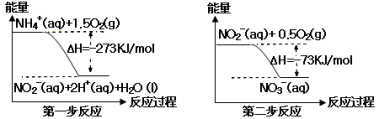
下列说法合理的是:
A.该反应的催化剂是NO2¯
B.升高温度,两步反应速率均加快,有利于NH4+ 转化成NO3¯
C.在第一步反应中,当溶液中水的电离程度不变时,该反应即达平衡状态
D.1 mol NH4+在第一步反应中与1 mol NO2-在第二步反应中失电子数之比为1:3
高三化学选择题极难题查看答案及解析
氨氮废水中的氮元素多以NH4+和NH3·H2O的形式存在,在一定条件下,NH4+经过两步反应被氧化成NO3¯,两步反应的能量变化示意图如下:

下列说法合理的是
A.该反应的催化剂是NO2¯
B.升高温度,两步反应速率均加快,有利于NH4+ 转化成NO3¯
C.在第一步反应中,当溶液中水的电离程度不变时,该反应即达平衡状态
D.1 mol NH4+在第一步反应中与1 mol NO2-在第二步反应中失电子数之比为1: 3
高三化学选择题简单题查看答案及解析
某反应池中,发生“生物硝化过程”,利用O2将NH4+氧化成NO3-,如果不考虑过程中硝化细菌的增殖,其净反应如下式所示:
1、完成上述反应的离子方程式并配平,将系数填入方框中,并标出电子的转移方向和数目。
2、反应中,还原剂是________,被还原的元素是。
3、将铵态氮中的lmg氮转化成硝酸根中的氮,需氧气 ________mg。(精确到0.01)
4、取100mL完全反应以后的溶液,加入19.2g铜粉及一定量的稀硫酸,恰好完全反应(假设还原产物全部是NO气体),则原溶液中NH4+的浓度为________mol/L。(假设反应前后溶液的体积不变)
高三化学填空题中等难度题查看答案及解析
在好氧菌和厌氧菌作用下,废液中NH4+能转化为N2(g)和H2O (l),示意图如下:
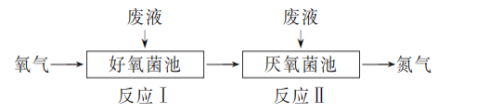
反应Ⅰ:NH4+(aq)+2O2(g)===NO3-(aq)+2H+(aq)+H2O (l) ΔH1=a kJ·mol-1
反应Ⅱ:5NH4+(aq)+3NO3-(aq)===4N2(g)+9H2O(l)+2H+(aq) ΔH2=b kJ·mol-1
下列说法正确的是
A. 两池发生的反应中,氮元素只被氧化
B. 两池中投放的废液体积相等时,NH4+能完全转化为N2
C. 常温常压下,反应Ⅱ中生成22.4 L N2转移的电子数为3.75×6.02×1023
D. 4NH4+(aq)+3O2(g)===2N2(g)+4H+(aq)+6H2O(l) ΔH=1/2(3a+b) kJ·mol-1
高三化学单选题中等难度题查看答案及解析
在好氧菌和厌氧菌作用下,废液中NH4+能转化为N2(g)和H2O (l),示意图如下:

反应Ⅰ:NH4+(aq)+2O2(g)===NO3-(aq)+2H+(aq)+H2O (l) ΔH1=a kJ·mol-1
反应Ⅱ:5NH4+(aq)+3NO3-(aq)===4N2(g)+9H2O(l)+2H+(aq) ΔH2=b kJ·mol-1
下列说法正确的是
A. 两池发生的反应中,氮元素只被氧化
B. 两池中投放的废液体积相等时,NH4+能完全转化为N2
C. 常温常压下,反应Ⅱ中生成22.4 L N2转移的电子数为3.75×6.02×1023
D. 4NH4+(aq)+3O2(g)===2N2(g)+4H+(aq)+6H2O(l) ΔH=1/2(3a+b) kJ·mol-1
高三化学单选题中等难度题查看答案及解析