-
阅读下表中短周期主族元素的相关信息。
元素
相关信息
A
A的单质能与冷水剧烈反应,得到强喊性溶液
B
B的原子最外层电子数是其内层电子数的3倍
C
在第三周期元素中,C的简单离子半径最小
D
A、B、D组成的36电子的化合物X是家用消毒剂的主要成分
E
所有有机物中都含有E元素
(1) E在元素周期表中的位置是_____________________。
(2) X的化学式为____________________
(3) A、B、C三种元素形成的简单离子半径由大到小的顺序为________________ (用离子符号表示)。
(4)A的单质在真空高压下能与由元素D、E组成的化合物ED4反应生成两种固体物质,其中一种是自然界中硬度最大的物质,此反应在科学上有“稻草变黄金”的美称。写出该反应的化学方程式:____________。
高二化学推断题中等难度题查看答案及解析
-
X、Y、Z、W为周期表中前20号元素中的四种,原子序数依次增大,W、Y为金属元素,X原子的最外层电子数是次外层电子数的3倍,Y、Z位于同周期,Z单质是一种良好的半导体.W能与冷水剧烈反应,Y、Z原子的最外层电子数之和与X、W原子的最外层电子数之和相等.下列说法正确的是( )
A.原子半径:W>Y>Z>X
B.气态氢化物的稳定性:X<Z
C.最高价氧化物对应水化物的碱性:Y>W
D.Y、Z的氧化物都有酸性和碱性高二化学选择题中等难度题查看答案及解析
-
下表是元素周期表中短周期的一部分。已知A元素原子的最外层电子数比其电子层数的3倍还多。下列关于表中六种元素的说法正确的是 ( )
A. X的单质在空气中可以燃烧
B. X、Y、Z三种元素中Y元素形成的单核阴离子半径最大
C. 最高价氧化物对应的水化物酸性最强的是A元素
D. A单质通入NaZ溶液中,根据反应现象可证明A、Z非金属性的相对强弱
高二化学单选题简单题查看答案及解析
-
下表是元素周期表中短周期的一部分。已知A元素原子的最外层电子数比其电子层数的3倍还多。下列关于表中六种元素的说法正确的是 ( )
A. X的单质在空气中可以燃烧
B. X、Y、Z三种元素中Y元素形成的单核阴离子半径最大
C. 最高价氧化物对应的水化物酸性最强的是A元素
D. A单质通入NaZ溶液中,根据反应现象可证明A、Z非金属性的相对强弱
高二化学单选题简单题查看答案及解析
-
下表是元素周期表中短周期的一部分。已知A元素原子的最外层电子数比其电子层数的3倍还多。下列关于表中六种元素的说法正确的是 ( )
A. X的单质在空气中可以燃烧
B. X、Y、Z三种元素中Y元素形成的单核阴离子半径最大
C. 最高价氧化物对应的水化物酸性最强的是A元素
D. A单质通入NaZ溶液中,根据反应现象可证明A、Z非金属性的相对强弱
高二化学单选题简单题查看答案及解析
-
A、B、C、D均为短周期主族元素,它们的原子序数依次增大,已知相关信息如下表所示:
元素代号
元素的原子结构或性质
A
原子最外层电子数是次外层电子数的3倍
B
单质燃烧时火焰呈黄色
C
氧化物为两性氧化物
D
原子最外层有7个电子
(1)A的元素符号为____________,D元素位于元素周期表中第________周期第____________族。
(2)C的最高价氧化物对应水化物的化学式为____________。
(3)B的单质与水反应的化学方程式为____________________。
高二化学推断题简单题查看答案及解析
-
有U、V、W、X四种前三周期元素,原子序数依次增大,其相关信息如下表:
元素编号
相关信息
U
所处的周期数、族序数分别与其原子序数相等
V
外层电子数是最内层电子数的两倍
W
单质中有三对共用电子对
X
是地壳中含量最多的元素
请回答下列问题:
(1)U、V两种元素组成的一种化合物甲是重要的化工原料,常把它的产量作为衡量石油化工发展水平的标志,则甲分子的空间构型为________。
(2)写出W单质的结构式 ___________,其化学键为________性共价键:W最简单气态氢化物的电子式为___________,分子的空间构型是___________,其化学键为___________性共价键。
(3)X在周期表中的位置是_______,该主族元素的气态氢化物中,沸点最低的是__________(填化学式)
(4)乙和丙分别是V和X的某种氢化物,这两种氢化物分子中含有有18个电子。乙和丙的化学式分别是________、________。
高二化学推断题中等难度题查看答案及解析
-
A、B、C、D是原子序数依次增大的四种短周期主族元素,其相关信息如下表所示
元素代号
元素相关信息
A
原子核内无中子,核外只有1个电子
B
其单质是空气中含量最多的气体
C
最外层电子数是电子层数的3倍
D
短周期中原子半径最大的元素
试回答下列问题:
(1)写出下列元素名称:A________, C________
(2)B在元素周期表中的位置:第____周期,第_____族。
(3)B、C两种元素的气态氢化物的稳定性强弱为:_____>______(填化学式)。
(4)A、C、D三种元素可以形成离子化合物,该化合物的电子式为_____________。
(5)写出C与D形成的淡黄色化合物的用途(填一种即可)___________________。
高二化学推断题简单题查看答案及解析
-
现有部分前36号元素的性质或原子结构如下表
元素编号
元素性质或原子结构
R
基态原子的最外层有3个未成对电子,次外层有2个电子
S
单质能与水剧烈反应,所得溶液呈弱酸性
T
基态原子3d轨道上有1个电子
X
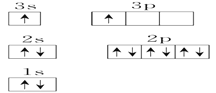
(1)R元素的第一电离能要大于其同周期相邻的元素,原因是____________。
(2)S元素的化合价是否有正价?_______,原因是_________,最外层电子排布式为____________。
(3)T元素的原子N能层上电子数为______,其原子结构示意图为_________。
(4)X的核外电子排布图违背了__________。用X单质、碱金属盐及碱土金属盐等可以做成焰火。燃放时,焰火发出五颜六色的光,请用原子结构的知识解释发光的原因:________________。
高二化学综合题中等难度题查看答案及解析
-
现有部分前36号元素的性质或原子结构如下表
元素编号
元素性质或原子结构
R
基态原子的最外层有3个未成对电子,次外层有2个电子
S
单质能与水剧烈反应,所得溶液呈弱酸性
T
基态原子3d轨道上有1个电子
X
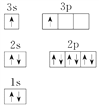
(1)R元素的第一电离能要大于其同周期相邻的元素,原因是________________________________________________________。
(2)S元素的化合价是否有正价?__________,原因是__________________________________,最外层电子排布式为________________________。
(3)T元素的原子N能层上电子数为__________,其原子结构示意图为__________。
(4)X的核外电子排布图违背了__________。用X单质、碱金属盐及碱土金属盐等可以做成焰火。燃放时,焰火发出五颜六色的光,请用原子结构的知识解释发光的原因:____________________________________________________________________。
【答案】 氮原子2p轨道半充满,能量低,稳定 否 F的电负性最大,只能得电子 2s22p5 2
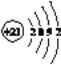 能量最低原理 电子从能量较高的轨道跃迁到能量较低的轨道时,以光的形式释放能量
能量最低原理 电子从能量较高的轨道跃迁到能量较低的轨道时,以光的形式释放能量【解析】试题分析:R元素的基态原子最外层有3个未成对电子,次外层有2个电子,R是N元素;S元素的单质能与水剧烈反应,所得溶液呈弱酸性,S是F元素;T元素的基态原子3d轨道上有1个电子,T是21号元素Sc; X元素的原子核外有12个电子,X是Mg元素。
解析:根据以上分析,(1)R是N元素,氮原子2p轨道半充满,能量低,稳定,所以第一电离能要大于其同周期相邻的O元素。
(2)元素F的电负性最大,只能得电子,所以F元素没有正价;F元素的最外层电子排布式为2s22p5。
(3)Sc原子的核外电子排布式是1s22s22p63s23p63d14s2,所以N能层上电子数为2,其原子结构示意图为
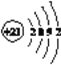 。(4)根据能量最低原理,Mg原子最外层2个电子应排布在3s轨道上,所以核外电子排布图违背了能量最低原理。电子从能量较高的轨道跃迁到能量较低的轨道时,以光的形式释放能量,所以燃放焰火时,焰火发出五颜六色的光。
。(4)根据能量最低原理,Mg原子最外层2个电子应排布在3s轨道上,所以核外电子排布图违背了能量最低原理。电子从能量较高的轨道跃迁到能量较低的轨道时,以光的形式释放能量,所以燃放焰火时,焰火发出五颜六色的光。【题型】综合题
【结束】
20现有部分短周期元素的性质或原子结构如下表:
元素编号
元素性质或原子结构
T
单质能与水剧烈反应,所得溶液呈弱酸性
X
L层p电子数比s电子数多2个
Y
第三周期元素的简单离子中半径最小
Z
L层有三个未成对电子
(1)写出元素X的离子结构示意图__________。
(2)写出Y元素最高价氧化物的水化物分别与HCl、NaOH溶液反应的离子方程式_______________________、_________________________。
(3)写出Z与Y的电子排布式______________、________________。
(4)元素T与氯元素相比,非金属性较强的是__________(用元素符号表示),下列表述中能证明这一事实的是__________。
A.气态氢化物的挥发性和稳定性
B.单质分子中的键能
C.两元素的电负性
D.含氧酸的酸性
E.氢化物中X—H键的键长(X代表T和Cl两种元素)
F.两单质在自然界中的存在形式
(5)探寻物质的性质差异性是学习的重要方法之一。T、X、Y、Z四种元素的单质中化学性质明显不同于其他三种单质的是__________(填元素符号),理由是________________________________________________。
高二化学综合题中等难度题查看答案及解析