-
I、工业合成氨反应为:N2(g)+3H2(g) 2NH3(g),对其研究如下:
2NH3(g),对其研究如下:
(1)已知H-H键能为436kJ·mol-1,N-H键能为391 kJ·mol-1,N≡N键的键能是945.6 kJ·mol-1,则上述反应的△H=_________。
(2)在773K时,分别将2molN2和6molH2充入一个固定容积为1L的密闭容器中,随着反应的进行,气体混合物中n(H2)、n(NH3)与反应时间t的关系如下表:
| t/min | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
| n(H2)/mol | 6.00 | 4.50 | 3.60 | 3.30 | 3.03 | 3.00 | 3.00 |
| n(NH3)/mol | 0 | 1.00 | 1.60 | 1.80 | 1.98 | 2.00 | 2.00 |
①该温度下,若向同容积的另一容器中投入的N2、H2、NH3浓度分别为3mol/L,3mol/L、3mol/L,此时v正_________v逆(填“大于”、“小于”或“等于”)
②由上述表中的实验数据计算得到“浓度~时间”的关系可用下图中的曲线表示,表示c(N2)~t的曲线是__________。在此温度下,若起始充入4molN2和12molH2,反应刚达到平衡时,表示c(H2)的曲线上相应的点为___________。

Ⅱ.NH3与NO2是常见的氮的化合物,研究它们的综合利用有重要意义。
(1)NO2产生的环境问题有___________(填两种)。
(2)热电厂通常用NH3消除燃煤烟气中NO2,该反应化学方程式____________。
(3)氨气与氯化氢气体混合的现象及该反应的用途是______________。
(4)若将少量氨气与过量氯气混合,则生成一种酸性气体和另一种化合物A,A中所有原子均满足8电子稳定结构,试写出A的电子式___________。
III.向SO2的饱和溶液中加入BaCl2溶液无明显现象,得混合溶液M。
(1)若将下列各组物质分别加入溶液M中,均可产生沉淀。其中原理相同、沉淀相同的是__________
a.氨水、NaOH溶液 b.氯水、FeCl3溶液
c.H2S溶液、氯水 d.硫酸、溴水
(2)若向溶液M中加入CaCO3粉末,则产生亚硫酸钡沉淀,请用化学反应原理予以解释(用离子方程式结合必要的文字)_________________________
-
已知H—H键能为436 KJ/mol,H—N键能为391KJ/mol,根据化学方程式:N2 + 3H2 = 2NH3 ΔH=—92.4 KJ/mol,则N≡N键的键能是
A.431 KJ/mol B.946 KJ/mol C.649 KJ/mol D.869 KJ/mol
-
已知H-H键的键能为436kJ· mol-1,H-N键的键能为391 kJ· mol-1,根据热化学方程式:N2(g)+3H2(g)  2NH3(g) △H=-92.4 kJ· mol-1,可知N≡N键的键能是
2NH3(g) △H=-92.4 kJ· mol-1,可知N≡N键的键能是
A.431 kJ· mol-1 B.649 kJ· mol-1 C.945.6 kJ· mol-1 D.896 kJ· mol-1
-
有关键能数据如表所示:
| 化学键 | N≡N | H—H | H—N |
| 键能/kJ·mol-1 | x | 436 | 391 |
已知N2(g)+3H2(g)=2NH3(g) ΔH=-92.4 kJ/mol。则x的值为( )
A.945.6 B.649 C.431 D.869
-
合成氯是人类研究的重要课题,目前工业合成氨的原理为:
N2(g)+3H2(g)  2NH3(g) ΔH=-93.0kJ/mol
2NH3(g) ΔH=-93.0kJ/mol
(1)某温度下,在2 L密闭容器中发生上述反应,测得数据如下
| 时间/h 物质的量/mol | 0 | 1 | 2 | 3 | 4 |
| N2 | 2.0 | 1.83 | 1.7 | 1.6 | 1.6 |
| H2 | 6.0 | 5.49 | 5.1 | 4.8 | 4.8 |
| NH3 | 0 | 0.34 | 0.6 | 0.8 | 0.8 |
①0~2 h内,v(N2)= 。
②平衡时,H2的转化率为____;该温度下,反应2NH3(g)  N2(g)+3H2(g)的平衡常数K= 。
N2(g)+3H2(g)的平衡常数K= 。
③若保持温度和体积不变,起始投入的N2、H2、NH3的物质的量分别为a mol、b mol、c mol,达到平衡后,NH3比的浓度与上表中相同的为 (填选项字母)。
A.a=l、b=3.c=0 B.a=4、b=12、c=0
C.a=0、b=0.c=4 D.a=l、b=3、c=2
(2)另据报道,常温、常压下,N2在掺有少量氧化铁的二氧化钛催化剂表面能与水发生反应,生成NH3和O2。已知:H2的燃烧热ΔH=-286kJ/mol,则陪制NH3反应的热化学方程式为 。
(3)采用高质子导电性的SCY陶瓷(能传递H'),通过电解法也可合成氨,原理为:
N2(g)+3H2(g)  2NH3(g)。在电解法合成氨的过程申,应将N2不断地通入 ___极,该电极反应式为 。
2NH3(g)。在电解法合成氨的过程申,应将N2不断地通入 ___极,该电极反应式为 。
-
工业上合成氨是在一定条件下进行如下反应:N2(g)+3H2(g)⇌2NH3(g),其部分工艺流程如下:
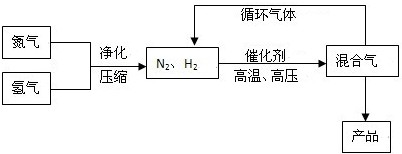
回答下列问题:
(1)已知:N2(g)+O2(g)=2NO(g);△H=180.5kJ/mol
4NH3(g)+5O2(g)=4NO(g)+6H2O(g);△H=-905kJ/mol
2H2(g)+O2(g)=2H2O(g);△H=-483.6kJ/mol
则N2(g)+3H2(g)⇌2NH3(g)的△H=______.
(2)如果工业上,在一定温度下,将1.5molN2 气体和6molH2 气体通入到体积为1升的密闭容器中.当反应达到平衡时,容器内气体的压强为起始时的80%,则氮气的转化率为______.该反应的平衡常数表达式为______,改变下列条件,能使平衡向正反应方向进行且平衡常数不变的是______
①增大压强 ②增大反应物的浓度 ③使用催化剂 ④降低温度
(3)可以用氯气来检验输送氨气的管道是否漏气,如果漏气则会有白烟(成份为氯化铵)生成.该反应的化学方程式为:______.
(4)假如该厂生产的氨水的pH=a,加入相同体积的盐酸时,溶液呈中性,则此盐酸的pH______14-a(填“大于”“小于”或“等于”)
-
某小组同学研究合成氨反应及氨水的性质如下:
(1)已知:N2(g)+3H2(g)=2NH3(g) △H =-92.4 kJ/mol
2H2(g)+O2(g)=2H2O(g) △H =-483.6kJ/mol
则氨气完全燃烧生成氮气和水蒸气的热化学方程式__________________________。
(2)如图是合成氨反应平衡混合气中NH3的体积分数随温度或压强变化的曲线,图中L(L1、L2)、X分别代表温度或压强。其中X代表的是_______________(填“温度”或“压强”),判断L1、L2的大小关系:L1______L2(填“<”或“>”)。

(3)已知:在硫酸铜溶液中加入浓氨水,首先析出蓝色的碱式硫酸铜沉淀,氨水过量时此沉淀溶解,得到深蓝色的四氨合铜(Ⅱ)络离子,发生的离子反应如下:
a.2Cu2++ 2NH3·H2O+ SO42-=== 2NH4+ + Cu2(OH)2SO4↓
b.Cu2(OH)2SO4 + 8 NH3 2[Cu(NH3)4]2++SO42-+2 OH-
2[Cu(NH3)4]2++SO42-+2 OH-
某小组设计如下实验:

①试管ⅰ中反应的离子方程式_______________________________________。
②试管ⅱ中的深蓝色晶体是[Cu(NH3)4]SO4·H2O,该实验现象反映出该晶体的性质是______。
③请结合方程式解释试管ⅲ加入少量NaOH后产生蓝色沉淀和气体的原因_______。
-
(10分)工业上合成氨是在一定条件下进行如下反应:
N2(g)+3H2(g) 2NH3(g)回答下列问题:
2NH3(g)回答下列问题:
(1)已知:N2(g)+O2(g)=2NO(g);△H=+180.5kJ/mol
4NH3(g)+5O2(g)=4NO(g)+6H2O(g); △H=-905kJ/mol
2H2(g)+O2(g)=2H2O(g); △H=-483.6kJ/mol
则N2(g)+3H2(g) 2NH3(g)的△H=_______________。
2NH3(g)的△H=_______________。
(2)(NH4)2SO3和NH4HSO4是两种化工原料。
①对于(NH4)2SO3溶液,某同学写出了如下的正确关系式:
2[c( )+c(
)+c( )+c(H2SO3)]=c(
)+c(H2SO3)]=c( )+c(NH3·H2O)
)+c(NH3·H2O)
该同学的依据是:_________________________________________
⑦写出NH4HSO4溶液中离子浓度由大到小的顺序:______________________。
(3)甲烷——空气燃料电池是一种碱性燃料电池,电解质溶液是20%-30%的KOH溶液。现用甲烷——空气燃料电池进行下图所示实验(其中a、b均为碳棒):

①Zn片上发生的电极反应式:_____________________。
②a电极的电极反应式_______________________________。
-
合成氨工业对国民经济和社会发展具有重要的意义,其原理是:
N2(g)+3H2(g)⇌2NH3(g) △H=-92.4KJ/mol,
(1)已知合成氨反应在某温度下2L的密闭容器中进行,测得数据如下表:
| 不同时间各物质的物质的量/mol |
| 0min | 1min | 2min | 3min | 4min |
| N2 | 1.50 | n1 | 1.20 | n3 | 1.00 |
| H2 | 4.50 | 4.20 | 3.60 | n4 | 3.00 |
| NH3 | 0.00 | 0.20 | n2 | 1.00 | 1.00 |
| | | | | |
根据表中数据计算:
①0 min~1 min内N2的平均反应速率为_____________
②该条件下反应的平衡常数k=________(保留两位小数)
③反应达到平衡后,若往平衡体系中再加入N2、H2、NH3各1mol,化学平衡向___________(填“正向”、“逆向”或“不移动”),该反应的平衡常数k___________(填“变大”“减小”或“不变”)
④能表明该反应达到平衡状态的是__________(选填序号)
A.N2的转化率等于NH3的产率
B.混合气体的平均相对分子质量不变
C.v(N2)与v(H2)的比值不变
D.混合气体的密度不变
(2)室温下向10mL0.3mol/LNaOH溶液中加入0.3mol/L的一元酸HA溶液pH的变化曲线如图,下列说法正确的是__________。
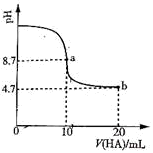
A.a点所示溶液中c(Na+)>c(A—)>c(H+)>c(HA)
B.a、b两点所示溶液中水的电离程度相同
C.b点所示溶液中c(A-)>c(HA)
D.pH=7时,c(Na+)= c(A-)+ c(HA)
E.b点所示溶液中c(HA)+c(A-)=0.2mol/L
-
已知H-H键键能为436kJ/mol,H-N键键能为391kJ/mol,根据化学方程式:N2+3H2
 2NH3,反应1mol N2时放出92.4kJ的热量,则N≡N键键能是( )
2NH3,反应1mol N2时放出92.4kJ的热量,则N≡N键键能是( )
A.431kJ/mol
B.945.6kJ/mol
C.649kJ/mol
D.869kJ/mol
2NH3(g),对其研究如下:





