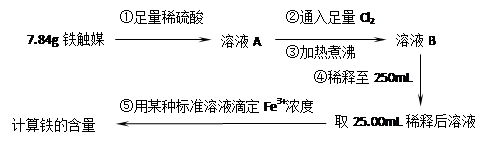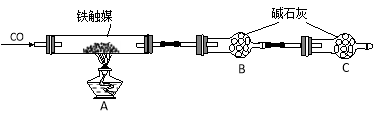-
铁触媒(铁的氧化物)是硫酸工业的催化剂。某同学设计了以下两种方案研究铁触媒的组成。
方案一:用下列装置测定铁触媒的含铁量,确定其组成。
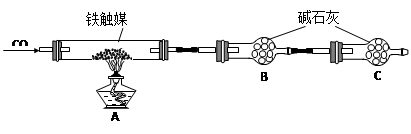
方案二:用下列实验方法测定铁触媒的含铁量,确定其组成。
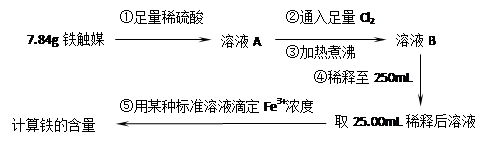
(1)步骤④中用到的玻璃仪器有烧杯、玻璃棒、胶头滴管和 ________ 。
(2)因为通入Cl2不足量,“溶液B”中还含有________会影响测定结果。
(3)因为通入Cl2过量且加热煮沸不充分,“溶液B”中可能含有Cl2。请设计实验方案检验Cl2,完成下列实验报告。
限选试剂:0.1mol·L-1酸性KMnO4溶液、紫色石蕊试液、品红稀溶液、淀粉-KI溶液、0.1moL·L-1KSCN溶液
(4)“干燥管C”的作用是。
(5)称取15.2g铁触媒进行上述实验。充分反应后,测得“干燥管B”增重11.0g,则该铁触媒的化学式可表示为________。
-
铁触媒(铁的某氧化物)是工业合成氨的催化剂。某同学设计了以下两种方案研究铁触媒的组成。
方案一:用下列流程测定铁触媒的含铁量,确定其组成。
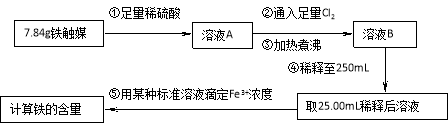
(1)步骤④后面需用 (填仪器名称)取25.00mL稀释后溶液。
(2)因为通入Cl2不足量,“溶液B”中还含有 会影响测定结果。
(3)因为通入Cl2过量且加热煮沸不充分,“溶液B”中可能含有Cl2。请设计实验方案检验Cl2,完成下列实验报告。限选试剂:0.1mol·L-1酸性KMnO4溶液、紫色石蕊试液、品红稀溶液、淀粉-KI溶液、0.1moL·L-1KSCN溶液
方案二:用下列实验方法测定铁触媒的含铁量,确定其组成。
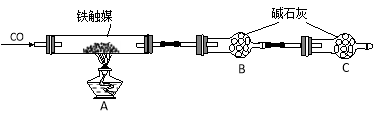
(4)“干燥管C”的作用是 。
(5)称取15.2g铁触媒进行上述实验。充分反应后,测得“干燥管B”增重11.0g,则该铁触媒的化学式可表示为 。(相对原子质量:C-12 O-16 Fe-56)
-
(16分)铁触媒(铁的某氧化物)是工业合成氨的催化剂。某同学设计了以下两种方案研究铁触媒的组成。
方案一:用下列流程测定铁触媒的含铁量,确定其组成。

(1)步骤④后面需用________(填仪器名称)取25.00mL稀释后溶液。
(2)因为通入Cl2不足量,“溶液B”中还含有________会影响测定结果。
(3)因为通入Cl2过量且加热煮沸不充分,“溶液B”中可能含有Cl2。请设计实验方案检验Cl2,完成下列实验报告。
限选试剂:0.1mol·L-1酸性KMnO4溶液、紫色石蕊试液、品红稀溶液、淀粉-KI溶液、0.1moL·L-1KSCN溶液
方案二:用下列实验方法测定铁触媒的含铁量,确定其组成。

(4)“干燥管C”的作用是________。
(5)称取15.2g铁触媒进行上述实验。充分反应后,测得“干燥管B”增重11.0g,则该铁触媒的化学式可表示为________。(相对原子质量:C-12 O-16 Fe-56)
-
铁触媒(铁的氧化物)是合成氨工业的催化剂。某同学设计了以下两种方案研究铁触媒的组成。
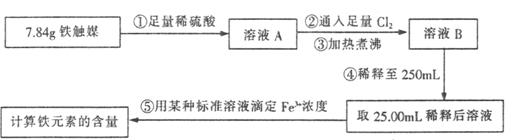
方案一:用下列实验方法测定铁触媒的含铁量,确定其组成。
(1)步骤④中用到的玻璃仪器有烧杯、玻璃棒、胶头滴管和________。
(2)若通入Cl2不足量,溶液B中还含有会影响测定结果。
(3) 若通入Cl2过量且加热煮沸不充分,溶液B中可能含有Cl2。请设计实验方案检验Cl2,完成下列实验报告。
限选试剂:0.1 mol L-1酸性KMnO4溶液、紫色石蕊试液、淀粉-KI溶液、0.1 mol L-1 KSCN溶液、 品红稀溶液
| 实验操作 | 实验现象与结论 |
| 取适量溶液B于试管中,滴加________,振荡 ,放置一段时间后,观察现象。 | 若溶液________,则溶液B中含Cl2; 若溶液________,则溶液B中不含Cl2。 |
方案二 :用下列装置测定铁触媒的含铁量,确定其组成。

(4)干燥管C的作用是________。
(5)称取15.2g铁触媒进行上述实验。充分反应后,测得干燥管B增重ll.0g,则该铁触媒的化学式可表示为________。
-
铁及其化合物在生活、生产中有着广泛的应用。
Ⅰ.铁触媒(+2价铁和+3价铁组成的氧化物)是工业合成氨的催化剂。某学习小组用下列流程测定铁触媒的含铁量。根据题意回答相关问题:
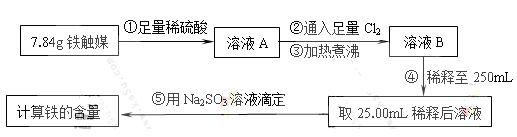
(1)步骤①中需用1.50 mol·L-1的硫酸100mL,若用18.4mol·L-1的浓硫酸来配制,则需要用量筒量取浓硫酸________mL
(2)步骤②通入Cl2的目的是________(用离子方程式表示)
(3)步骤④后需用________(填仪器名称)取25.00mL稀释后溶液。
(4)步骤⑤消耗0.10mol·L-1的Na2SO3溶液25.00mL,则铁触媒中铁的质量分数为。
Ⅱ.目前的研究表明,铁的某些含氧酸盐可用于工业废水、废气的处理。
(1)用K2FeO4处理中性废水时与水反应生成氢氧化铁胶体,并放出无色无味的气体和其它物质,写出反应的离子反应方程式________,处理废水时既利用K2FeO4强氧化性,又利用生成氢氧化铁胶体的 作用。
(2)MFe2O4可以与氢气反应制备新型纳米材料氧缺位铁酸盐MFe2Ox (3<x<4),其中M表示+2价的金属元素,常温下,MFe2Ox能使工业废气中的SO2转化为S,达到回收硫、净化空气目的,转化过程表示如下:

则可以判断x________y,氧化性:MFe2Oy________SO2(填“>”、“<”或“=”)
-
(11分)某研究性学习小组的同学为在实验室再现二氧化硫催化氧化的过程,并制取少量三氧化硫晶体,设计了如图所示的装置。已知三氧化硫遇水生成硫酸并放出大量热,容易形成酸雾,工业上常用浓硫酸吸收三氧化硫。
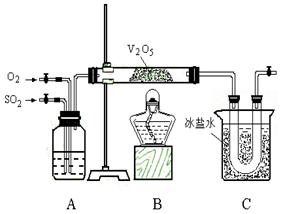
试回答:
(1)已知6.4 g 二氧化硫被氧气氧化成气态三氧化硫,放出9.83 kJ热量。反应的热化学方程式为____________________________________________________;
(2)A装置可用来观察二氧化硫和氧气的进气量。实验时使A中氧气导管冒出的气泡与二氧化硫导管冒出的气泡速率相近,其目的是___________________________;
(3)检查完装置的气密性且加入药品后,开始进行实验。此时首先应该进行的操作是________________________________。
(4)C装置用来收集三氧化硫,若用a g铜跟足量浓硫酸反应制二氧化硫,实验结束时得到b g 三氧化硫,该实验中二氧化硫的转化率不小于_________________;
(5)为了减轻实验对环境的污染,请你设计尾气处理装置,绘出装置图:
__________________________________________________________________。
-
二氧化硫的催化氧化是工业上生产硫酸的主要反应,反应如下:
I:2SO2(g)+O2(g) 2SO3(g) △H1=-197.7kJ·mol-1 K1(浓度平衡常数)
2SO3(g) △H1=-197.7kJ·mol-1 K1(浓度平衡常数)
为研究该反应,某同学设计了以下三种已装固体V2O3催化剂的密闭容器装置

(1)在初始体积与温度相同的条件下,甲、乙、丙中均按2 mol SO2、1molO2投料,达平衡时,三个容器中SO2的转化率从大到小的顺序为___________(用“甲、乙、丙”表示)。
(2)在容器丙中,0.1MPa条件下,在不同温度或不同投料方式下研究上述反应得到数据如下表:
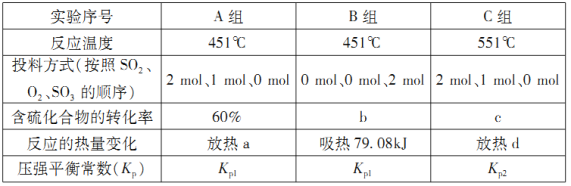
①表中:a=___________;b=___________。
②已知用平衡分压(分压=总压×物质的量分数)代替平衡浓度计算,得到的平衡常数即为压强平衡常数,则Kp1=___________;Kp1___________Kp2(填“>”、“<”或“=”)。
③若按0.4 mol SO2、0.4molO2、0.4 mol SO3进行投料,则反应开始时v正(SO2)_______v逆(SO2)(填“>”、“<”或“=”)。
(3)将上述固体催化剂V2O5换成NO2气体同样可以对该反应起到催化作用,此催化过程如下:
Ⅱ:SO2(g)+NO2(g) SO3(g)+NO(g) △H2 K2(浓度平衡常数)
SO3(g)+NO(g) △H2 K2(浓度平衡常数)
Ⅲ:2NO(g)+O2(g) 2NO2(g) △H3=-114.1kJ·mol-1 K3(浓度平衡常数)
2NO2(g) △H3=-114.1kJ·mol-1 K3(浓度平衡常数)
△H2=___________;K3=___________(用含有K1、K2的表达式表示)。
-
现有含CaO杂质的CaC2试样。某研究性学习小组的同学拟用以下三种方案测定CaC2试样的纯度。请填写下列空白:
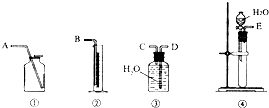
(1)第一种方案:请从下图中选用适当的装置,设计一个实验,测定CaC2试样的纯度。
所选用装置的连接顺序为(填各接口的字母):________。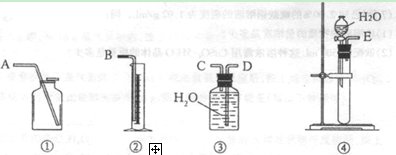
(2)第二种方案:根据试样和水在锥形瓶中反应前后质量的变化,测定CaC2的质量分数。先称取试样1.50g,并称量锥形瓶和水的质量为195.00g,再将试样加入锥形瓶中,反应过程中每隔相同时间测得的数据如下表。
| 读数次数 | 质量/g |
| 锥形瓶+水+试样 | 第1次 | 196.30 |
| 第2次 | 196.15 |
| 第3次 | 196.05 |
| 第4次 | 196.00 |
| 第5次 | 196.00 |
①计算CaC2的质量分数时,不必作第6次读数的原因是:________。
②此试样中CaC2的质量分数为________。(保留2位有效数字)
(3)第三种方案:称取一定质量的试样(1.60g),操作流程如下:
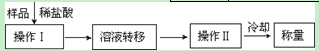
①操作Ⅱ的名称是________。
②在转移溶液时,如溶液转移不完全,则CaC2质量分数的测定结果________ (填“偏大”、“偏小”或“不变”)。
-
现有含CaO杂质的CaC2试样.某研究性学习小组的同学拟用以下三种方案测定CaC2试样的纯度.请填写下列空白:
(1)第一种方案:请从下图中选用适当的装置,设计一个实验,测定CaC2试样的纯度.所选用装置的连接顺序应是(填各接口的字母):______.
| 读数次数 | 质量/g |
| 锥形瓶+水+试样 | 第1次 | 196.30 |
| 第2次 | 196.15 |
| 第3次 | 196.05 |
| 第4次 | 196.00 |
| 第5次 | 196.00 |
(2)第二种方案:根据试样和水在锥形瓶中反应前后质量的变化,测定CaC2的质量分数.先称取试样1.50g、锥形瓶和水的质量为195.00g,再将试样加入锥形瓶中,反应过程中每隔相同时间测得的数据如右表:
计算CaC2的质量分数时,必需用的数据是______.不必作第6次读数的原因是______.此试样中CaC2的质量分数为______.
(3)第三种方案:称取一定质量的试样(1.60g),操作流程如下:
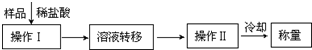
①操作Ⅱ的名称是______.
②还需直接测定的物理量是______.
③在转移溶液时,如溶液转移不完全,则CaC2质量分数的测定结果______(填“偏大”、“偏小”或“不变”).
④请指出该实验方案的2个不足之处______
⑤请改进这个实验方案,至少解决其中1个不足之处______.
-
实验室为测定某工业纯碱(假设仅含 NaHCO3 杂质)中 Na2CO3 的质量分数,设计了以下四 中实验方案:
方案一:样品 稀硫酸 测定生成二氧化碳的质量。采用下图装置完成实验。
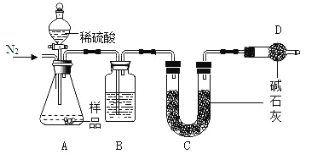
(1) B 中盛放的物质是_________。若把分液漏斗中的稀硫酸换成盐酸,在其他操作正确的情况下,测定 的 Na2CO3 的质量分数_____(填“偏大”、“偏小”或“无影响”),解释原因_____。
方案二:样品 加热 测定剩余固体的质量,坩埚的质量为 m0,样品和坩埚的质量为 m1,反应结束后坩埚及剩余固体的质量为 m2。
(2)移动坩埚的仪器是_____;实验时需要重复“ 加热、冷却、称量” 操作多次,其目的是________________;样品中碳酸钠的质量为____________g(用 m0、m1、m2 表示)。
方案三:样品溶液 氢氧化钙溶液 测定沉淀质量
(3)实验步骤为:①称量样品的质量②加水溶解③加氢氧化钙溶液,沉淀④过滤(其余步骤省略)。在过 滤前,需要检验是否沉淀完全,其操作是____________________。如果步骤③中使用 CaCl2 溶液代替氢氧 化钙溶液作沉淀剂,在其他操作正确的情况下,测得的结果______ (填“偏大”、“偏小”或“无影响”)。