-
(14分)亚铁是血红蛋白的重要组成部分,起着向人体组织传送O2的作用,人如果缺铁就可能出现缺铁性贫。下面是一种补铁药品说明书中的部分内容:该药品为无水碱式盐,含Fe2+34%~36%,是薄衣片,与VC(维生素C)同服可增加本品吸收。某同学设计实验对其中的铁成分进行了验证。请一起完成实验:
第一步:查阅资料得知,双氧水可以氧化SCN—生成N2、CO2、和SO42—,也可以将Fe2+ 氧化成 Fe3+。
第二步:向去掉糖衣、研磨好的药品中加稀盐酸,出现淡绿色混浊液,说明有________存在(填离子符号)。
第三步:往上述溶液中滴入几滴KSCN溶液出现浅红色,说明溶液中有少量Fe3+存在。该离子存在的原因可能是(填序号):________
①药品中的铁本来就以Fe3+的形式存在:②在制药过程中生成少量Fe3+;
②本实验过程中有少量Fe3+生成。
第四步:将第三步所得溶液分成两份,分别装在A、B两个试管中。
第五步:向A试管的溶液中加入少量稀硫酸,再慢慢滴入过量的H2O2溶液,溶液的红色先变深,之后红色逐渐褪去。
红色变深的原因是(用离子方程式表示)________红色又逐渐褪去的原因可能是
设计实验证明你的推测________
第六步:向B试管的溶液中加入一片VC,片刻后溶液红色也褪去,说明VC有________性。怎样理解药品说明书中所述“与VC(维生素C)同服可增加本品吸收”这句话?
________。
高一化学实验题简单题查看答案及解析
-
治疗缺铁性贫血的常见方法是服用补铁药物,常采用更易被吸收的亚铁盐。“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物。该药品不溶于水,但能溶于人体中的胃酸。某同学为了检测“速力菲”药片中二价铁元素,设计并实施了如下实验:

试回答下列问题:
(1)试剂1是______________,试剂2是__________________。
(2)该同学预测加入试剂2后,溶液应依然为浅绿色,但这与实际现象不符,请用离子方程式解释实际现象的合理性:_________________,_______________。
(3)用离子反应方程式解释加入新制氯水后溶液变血红色的原因:______________________________________________。
(4)补铁药物的说明书中通常会有“与VC同服可增加本品吸收”的内容,向淡红色溶液中加入VC,片刻后溶液红色褪去,试从氧化还原角度解释补铁药物与VC同服的优点:___________________________________________________________。
高一化学综合题中等难度题查看答案及解析
-
铁是人体必需的微量元素,治疗缺铁性贫血的常见方法是服用补铁药物。“速力菲”(主要成分: 琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物(见图)。该药品不溶于水但能溶于人体中的胃酸(主要成分:稀盐酸),服用时同维生素 C一起服用效果会更好。某学习小组为了检测“速力菲”药片中Fe2+的存在,设计并进行了如下实验:

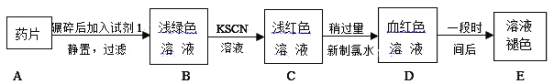
(1)试剂1是_____________。
(2)取少量B溶液于试管中,向其滴加NaOH溶液。最初观察到白色沉淀,一会灰变为灰绿色,最终变为红褐色,沉淀颜色变化的原因是_________________(用化学方程式表示)。
(3)B溶液中加入KSCN溶液后,溶液中也产生了红色,其可能的原因是____________。
(4)有同学提出由C到D 用双氧水代替新制氯水效果会更好原因是____,写出用双氧水实现由C到D转变的离子方程式________。
(5)在上述实验中,同学们发现血红色溶液放置一段时间后,溶液的颜色会逐渐褪去。为了进一步探究溶液褪色的原因,甲、乙两位同学首先对此进行了猜想:
编号
猜想
甲
溶液中的+3价Fe又被还原成+2价铁
乙
溶液中的SCN-被过量的新制氯水氧化
①你认为甲同学的猜想合理吗______?(填“合理”或“不合理”)请说明理由_______。
②基于乙同学的猜想,请设计一个简单的实验加以验证____________________________。
(6)“速力菲”药品为什么要与维生素 C一起用效果会更好原因是_______。
高一化学实验题中等难度题查看答案及解析
-
铁是人体必需的微量元素,治疗缺铁性贫血的常见方法是服用补铁药物。“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物。该药品不溶于水但能溶于人体中的胃酸。某同学为了检测“速力菲”药片中Fe2+的存在,设计并进行了如下实验:
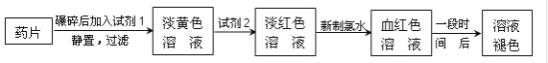
试回答下列问题:
(1)试剂1是__,试剂2是__,加入新制氯水后溶液中发生的离子反应方程式是__、_____。
(2)加入试剂2后溶液中颜色由淡黄色转变为淡红色是因为__,写出+2价Fe在空气中转化为+3价Fe的化学方程式__。
(3)该同学猜想红色溶液变为无色溶液的原因是溶液中的+3价铁被还原为+2价铁,你认为该同学的猜想合理吗?__。若你认为合理,请说明理由(若你认为不合理,该空不作答);若你认为不合理请提出你的猜想并设计一个简单的实验加以验证(若你认为合理,该空不作答)___。
高一化学实验题中等难度题查看答案及解析
-
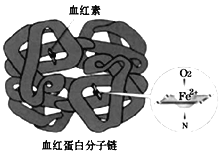
铁是人体必需的微量元素,在肺部,血红蛋白中血红素的Fe2+与O2结合,把O2送到各个组织器官。铁摄入不足可能引起缺铁性贫血。黑木耳中含有比较丰富的铁元素,某研学小组测定其含量。
(1)(铁元素的分离) 称量黑木耳,将之洗净切碎,用蒸馏水浸泡,但浸泡液中未能检测到铁元素。在坩埚中高温灼烧黑木耳,使之完全灰化。用酸充分浸泡溶解,过滤,滤液备用。
① 浸泡液检测不出铁元素的原因是____。
② 滤液中铁元素的存在形式是Fe2+、____。
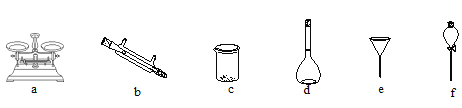
(2)(配制溶液) 将滤液配制成100 mL 溶液。实验时需要选择合适的仪器完成(铁元素的分离)、(配制溶液)2个实验,下列仪器不必使用的是____。
(3)(铁元素含量测定) 研学小组提出如下测量方案:
Ⅰ. 沉淀法:向溶液中加入足量NaOH溶液,搅拌使Fe(OH)2全部转化为Fe(OH)3然后过滤、洗涤沉淀、加热烘干、称量Fe(OH)3的质量进行分析。请指出该测量方案是否可行及其理由____。
Ⅱ. 比色法:流程示意如下:
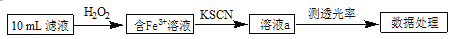
① 用离子方程式解释加入H2O2的目的是____。
② 溶液a的颜色是____。
③ 溶液颜色越深,光的透过能力越差,即透光率越小。若不加H2O2,测出黑木耳中铁元素的含量____(填“偏大”或“偏小”)。
(4)亚铁盐易被氧化,但在体内Fe2+参与O2的运输却不被氧化。蛋白质是一种既有亲水部分、又有疏水部分的大分子,为血红素提供了疏水环境。可见,氧化还原反应能否发生与___有关。
高一化学实验题中等难度题查看答案及解析
-
铁是人体必需的微量元素,在肺部,血红蛋白中血红素的Fe2+与O2结合,把O2送到各个组织器官。铁摄入不足可能引起缺铁性贫血。黑木耳中含有比较丰富的铁元素,某研学小组测定其含量。
(1)【铁元素的分离】 称量黑木耳,将之洗净切碎,用蒸馏水浸泡,但浸泡液中未能检测到铁元素。在坩埚中高温灼烧黑木耳,使之完全灰化。用酸充分溶解,过滤,滤液备用。
①浸泡液检测不出铁元素的原因是________。
②滤液中铁元素的存在形式是Fe2+、________。
(2)【配制溶液】 将滤液配制成100 mL 溶液。选择合适的仪器完成“铁元素的分离”、
“配制溶液”2个实验,下列仪器不必使用的是_______。

(3)【铁元素含量测定】 研学小组提出如下测量方案:
Ⅰ.沉淀法:向溶液中加入足量NaOH溶液,过滤、洗涤沉淀、加热烘干、称量。评价该测量方案是否可行________。
Ⅱ.比色法:流程示意如下:

① 用离子方程式解释加入H2O2的目的是________。
② 溶液a的颜色是________。
③ 溶液颜色越深,光的透过能力越差,即透光率越小。若不加H2O2,测出黑木耳中铁元素的含量________(填“偏大”或“偏小”)。
(4)亚铁盐易被氧化,但在体内Fe2+参与O2的运输却不被氧化。蛋白质是一种既有亲水部分、又有疏水部分的大分子,为血红素提供了疏水环境。
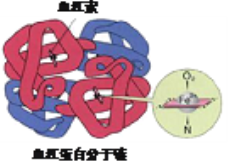
可见,氧化还原反应能否发生与_________有关。
高一化学实验题中等难度题查看答案及解析
-
铁是人体必需的微量元素,治疗缺铁性贫血的常见方法是服用补铁药物,“速力菲”(主要成分为的琥珀酸亚铁,即丁二酸亚铁)是市场上一种常用的补铁药物,它难溶于水,但在人体胃酸的作用下可以释放出Fe2+,从而被人体吸收。
(1)某同学为了检验其中的Fe2+,将药物研磨、水溶后过滤。
①如图是某学生的过滤操作示意图,其操作不规范的是___(填标号)
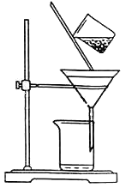
a.玻璃棒用作引流
b.漏斗末端颈尖未紧靠烧杯壁
c.将滤纸湿润,使其紧贴漏斗壁
d.滤纸边缘高出漏斗
e.用玻璃棒在漏斗中搅动以加快过滤速度
②取少量所得滤液,分别加入 K3Fe(CN)6溶液(一种检验Fe2+的试剂)和KSCN溶液(一种检验Fe3+的试剂),均未出现明显现象。其主要原因是___。
(2)取酸性环境下“速力菲”溶解过滤后的滤液敞口放置在空气中一段时间,然后滴入KSCN溶液,溶液立即呈现血红色说明有Fe3+生成,说明Fe2+___。
(3)医生通常会建议:与维生素C同时服用,能增强“速力菲”的补铁效果。此举是利用了维生素C的___。(填“氧化性”、“还原性”或“碱性”)
高一化学实验题中等难度题查看答案及解析
-
人体中含有铁元素,+2价的亚铁离子是血红蛋白(用于运输氧气)的重要组成成分。
(l)误服亚硝酸盐会使人中毒,是因为二价铁被 ___(填“氧化”或“还原”)成三价铁,此 时服用维生素C可缓解亚硝酸盐中毒,维生素C在此过程中是作____(填“氧化剂”或“还原剂”)。
(2)现有一瓶久置的FeSO4溶液,请设计实验检验其中是否含有Fe3+:___ 。Fe2+在空气中易发生氧化还原反应而变质,可加入____(填化学式)来防止其变质,而又不会使溶液中有新的杂质。
(3)高铁酸钾(K2FeO4)是水处理过程中使用的一种新型消毒剂。可在碱性条件下,用NaCIO氧化Fe(OH)3来制备,请配平反应方程式:____ClO—+____Fe(OH)3+____OH— =____FeO42—+_________+____Cl—。
(4)向制得的Na2FeO4溶液中加入适量的饱和KOH溶液会析出K2FeO4,写出该反应的化学方程式:____。
高一化学综合题中等难度题查看答案及解析
-
NaNO2(亚硝酸钠)常用作肉类食品的防腐剂,若添加过量,易导致人体中毒。亚硝酸盐经消化道吸收进入血液,使血液中的正常携氧的亚铁血红蛋白转化成三价铁血红蛋白,失去携氧能力引起组织缺氧,导致中毒。成人摄入0.2~0.5g就会引起中毒,摄入3g即可致死。
(1)NaNO2的毒性源于NaNO2具有________性。
(2)设计实验验证NaNO2确实具有该性质(已知: NaNO2与HI反应生成I2和NO),将离子方程式配平:
____NO2-+_____H+ + _____I -=_____I2 + _____NO↑ + _____
(3)请从两个不同的角度进一步预测NaNO2还可能具有的化学性质,并说明预测的依据(已知:HNO2是一种弱酸)。按照因为…所以…进行表述___________________;__________________。
(4)救治NaNO2中毒病人的方法是静脉注射亚甲蓝(一种有机物),其解毒原理是__________。
高一化学解答题中等难度题查看答案及解析
-
化学在药物的开发、合成和使用中起着至关重要的作用.
(1)下面是一种常见药品说明书的部分内容,请将其补充完整.
[药品名称]碳酸氢钠.
[其他名称]重碳酸钠、酸性碳酸钠、______.
[功效主治]适用于胃酸过多______、消化不良______及碱化尿液等;静脉给药用于酸中毒;外用滴耳软化耵聍.
[不良反应]对胃溃疡______的病人,中和胃酸时产生的气体会刺激溃疡面,甚至有胃穿孔的危险.其中的化学原理(用离子方程式表示)是______.
(2)胃舒平(复方氢氧化铝)也可以治疗胃酸过多,所依据的反应原理(用离子方程式表示)是______.氢氧化铝跟氢氧化钠溶液反应的离子方程式是______.
(3)硫酸亚铁缓释片可以补铁、防治贫血,但存放不当很容易变质,药片中的Fe2+被氧化生成Fe3+.若将药片配成溶液,需使用刚刚煮沸过又冷却的蒸馏水,原因是______.实验室检验Fe3+,除了可以用碱外,常用的试剂是(填化学式)______,现象______,则证明有Fe3+.高一化学解答题中等难度题查看答案及解析