-
CO2中的一个O原子被S原子代替后,即为羰基硫(OCS),羰基硫是一种有臭鸡蛋气味的无色气体,高温下分解为CO和S。下列有关说法正确的是
A.OCS中S的化合价为+4价
B.羰基硫分解时,CO是氧化产物
C.每有1mol OCS分解,能生成22.4LCO
D.OCS中含有共价键,属于非电解质
高三化学选择题中等难度题查看答案及解析
-
CO2中的一个O原子被S原子代替后,即为羰基硫(OCS),羰基硫是一种有臭鸡蛋气味的无色气体,高温下分解为CO和S。下列有关说法正确的是
A.OCS中S的化合价为+4价
B.羰基硫分解时,CO是氧化产物
C.每有1mol OCS分解,能生成22.4LCO
D.OCS中含有共价键,属于非电解质
高三化学选择题中等难度题查看答案及解析
-
羰基硫(OCS)是一种有臭鸡蛋气味的无色气体,分子结构与CO2相似,高温下分解为CO和S。下列有关说法正确的是( )
A.OCS、CO、CO2、S四种物质的晶体类型相同
B.OCS高温分解时,碳元素化合价升高
C.OCS分子中含有1个σ键和1个π键
D.22.4 L OCS中约含有3×6.02×1023个原子
高三化学选择题中等难度题查看答案及解析
-
(1)羰基硫(COS)在常温常压下为有臭鸡蛋气味的无色气体,广泛应用于农药、医药和其他化工生产中。在酸性溶液中可用H2O2氧化COS生成一种强酸(脱硫反应)该脱硫反应的化学方程式为________。
(2)已知:①COS(g)+H2(g)
H2S(g)+CO(g)△H1=+11kJ·mo-1;
②CO(g)+H2O(g)
H2(g)+CO2(g) △H2=-21kJ·mol-l;
③COS(g)+H2O(g)
H2S(g)+ CO2(g) △H3=________
(3)用活性a-Al2O3催化COS水解,反应为 COS(g)+H2O(g)
CO2(g)+H2S(g)在催化剂表面停留时间相同时,不同温度下COS的转化率如图所示。
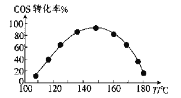
由图可知,COS的转化率在后期下降的原因可能是________ 。
(4)COS可由CO和H2S在一定条件下反应制得,在刚性容器中发生反应:CO(g)+H2S(g)=COS(g) + H2(g)△H<0。初始时各物质的物质的量浓度与平衡时CO的物质的量浓度数据如下表所示:
实验
温度/℃
起始时/ mol•L-1
平衡时/ mol•L-1
c(CO)
c(H2S)
c(COS)
c(H2)
c(CO)
Ⅰ
T1
20.0
20.0
0
0
16.0
Ⅱ
T2
10.0
10.0
0
0
7.0
Ⅲ
T3
7.0
8.0
2.0
4.5
①T1_____(填“大于”“小于”或“等于”)T2。
②实验I中,8 min反应达到平衡,则0〜8 min内v(COS)= _____mol•L-1,T
时,该反应的平衡常数为_____。
③实验Ⅲ中的反应应_____(填“正向”或“逆向”)移动。
(5)反应COS(g)+H2(g)=H2S(g)+CO(g)的平衡常数K与温度T的关系式为lgK=aT+b(a,b均为常数),请在如图所示的坐标系中用直线画出lgK与温度T的关系图像_____。
高三化学综合题中等难度题查看答案及解析
-
天然气的主要成分是甲烷,含有少量的羰基硫
、乙硫醇
等气体。
(1)组成羰基硫的元素中,原子半径最小的元素在周期表中的位置是 ______。
(2)乙硫醇有特殊气味,是天然气的臭味指示剂.乙硫醇可以看作是乙醇分子中羟基
被
取代,则乙硫醇的结构式为 ______。
(3)下列事实可用于比较C与S两种元素非金属性
原子得电子能力
相对强弱的是 ______ (填序号)。
a.沸点:
元素在周期表中的位置
酸性:
同温同浓度水溶液的pH:
(4)羰基硫水解及利用的过程如下
部分产物已略去
:
 溶液
溶液溶液
①常温下,在反应Ⅱ中,每吸收
气体放出热量a kJ,其热化学方程式为 ______。
②已知X溶液中硫元素的主要存在形式为
,则反应Ⅲ中生成该离子的离子方程式为 ______。
③如图是反应Ⅲ中,在不同反应温度下,反应时间与
产量的关系图
初始含量为
 请结合图象数据解释X溶液中除
请结合图象数据解释X溶液中除外,还有
、
的原因______。
高三化学综合题中等难度题查看答案及解析
-
下列化学用语正确的是( )
A.用电子式表示HCl的形成过程:
B.乙烯的分子式:CH2=CH2
C.羰基硫(OCS)的比例模型:
D.氯离子的结构示意图:
高三化学选择题简单题查看答案及解析
-
I.羰基硫(COS)可作为熏蒸剂,分子结构与CO2相似。回答下列问题:
(1)碳原子的核外电子排布式为____________;组成羰基硫的元素中,半径最大的原子其核外有_____种不同能量的电子。
(2)羰基硫为___(填“极性”或“非极性”)分子,羰基硫的电子式为_____________。
(3)解释稳定性CO2大于CS2的原因________________________________________。
II.密闭容器中,发生反应:CO(g)+H2S(g)
COS(g)+H2(g)
(4)已知逆反应速率随时间变化如图所示,则t0时改变的条件可能是_____________或________________。
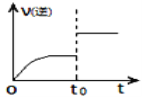
(5)该反应达到平衡后,其他条件不变,升高温度,H2S浓度增加,表明该反应是___(填“放”或“吸”)热反应,平衡常数K将____(填“增大”、“减小”或“不变”);若在反应体系中通入一定量SO2(g),判断平衡移动的方向并解释原因。 ________________________
高三化学综合题中等难度题查看答案及解析
-
最新研究表明生命起源于火山爆发,因为火山爆发产生的气体中含有1%的羰基硫(化学式为COS,CO就是羰基),已知羰基硫分子中所有原子最外层均满足8电子稳定结构,结合元素周期表知识,下列有关说法正确的是( )
A.羰基硫中O为-2价,C、S都是+1价
B.羰基硫分子中共含有3个原子核、16个电子
C.羰基硫的电子式为:········C········
D.羰基硫分子结构中只含有极性共价键
高三化学选择题中等难度题查看答案及解析
-
硫化氢是一种有臭鸡蛋气味的剧毒气体,在生产、生活及科研中均有重要应用。
(1)工业上采用高温热分解H2S的方法制取H2,在膜反应器中分离出H2,发生的反应为2H2S(g)
2H2(g)+S2(g)△H
已知:①H2S(g)
H2(8)+S(g)△H1
②2S(g)
S2(g)△H2
则△H=________(用含△H1、△H2的式子表示)。
(2)在容积2 L的恒容密闭容器中,控制不同温度进行H2S分【解析】
2H2S(g)2H2(g)+S2(g)。H2S的起始物质的量均为1mol,实验过程中测得H2S的转化率如图1所示。曲线a表示H2S的平衡转化率与温度的关系,曲线b表示不同温度下反应经过相同时间时H2S的转化率。
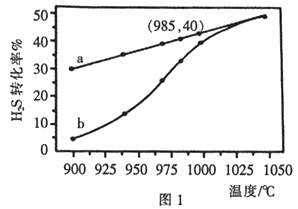
①反应2H2S (g)
2H2(g)+S2(g)是放热还是吸热,判断并说理由________。
②随着H2S分解温度的升高,曲线b向曲线a逐渐靠近,其原因是________ 。
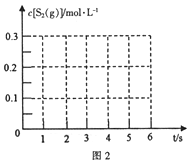
③在985℃时,该反应经过5 s达到平衡,则该反应的平衡常数为________。在图2中画出985℃时,0~6s 体系中S2(g)浓度随时间的变化曲线。___________________
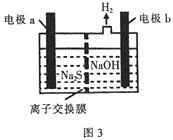
(3)工业上常用NaOH溶液吸收H2S废气,吸收后所得溶液进行电解(装置如图3所示),在阳极区可生成Sx2-,写出生成Sx2-离子的电极反应式:________。
高三化学综合题中等难度题查看答案及解析
-
研究表明生命起源于火山爆发,是因为火山爆发产生的气体中含有1%的羰基硫(COS),已知羰基硫分子中所有原子均满足八电子结构,结合周期表知识,有关说法不正确的是
A.羰基硫分子为非极性分子 B.羰基硫的电子式为:
C.羰基硫沸点比CO2高 D.羰基硫分子中三个原子处于同一直线上
高三化学选择题中等难度题查看答案及解析