-
选考[化学---选修2:化学与技术](15分)银、铜均属于重金属,从银铜合金废料中回收银并制备含铜化合物产品的工艺如图所示:
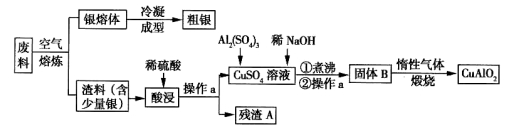
(1)熔炼时被氧化的元素是 ,酸浸时反应的离子方程式为 。为提高酸浸时铜元素的浸出率及浸出速率,酸浸前应对渣料进行处理,其处理方法是 。
(2)操作a是 ,固体B转化为CuAlO2的过程中,存在如下反应,请填写空白处:
CuO+ Al2O3 + ↑。
+ ↑。
(3)若残渣A中含有n mol Ag,将该残渣全部与足量的稀HNO3置于某容器中进行反应,写出反应的化学方程式 。为彻底消除污染,可将反应中产生的气体与V L(标准状况)空气混合通入水中,
则V至少为 L(设空气中氧气的体积分数为0.2)。
(4)已知2Cu+  Cu+Cu2+,试分析CuAlO2分别与足量盐酸、稀硝酸混合后,产生现象的异同点 。
Cu+Cu2+,试分析CuAlO2分别与足量盐酸、稀硝酸混合后,产生现象的异同点 。
(5)假设粗银中的杂质只有少量的铜,利用电化学方法对其进行精炼,则粗银应与电源的 极相连,当两个电极上质量变化值相差30.4g时,则两个电极上银质量的变化值相差 g。
-
[化学---选修2:化学与技术](15分)银、铜均属于重金属,从银铜合金废料中回收银并制备含铜化合物产品的工艺如图所示:
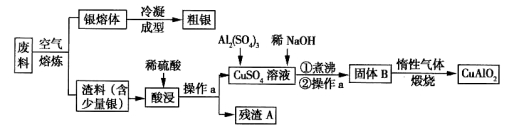
(1)熔炼时被氧化的元素是 ,酸浸时反应的离子方程式为 。为提高酸浸时铜元素的浸出率及浸出速率,酸浸前应对渣料进行处理,其处理方法是 。
(2)操作a是 ,固体B转化为CuAlO2的过程中,存在如下反应,请填写空白处:
CuO+ Al2O3 + ↑。
+ ↑。
(3)若残渣A中含有n mol Ag,将该残渣全部与足量的稀HNO3置于某容器中进行反应,写出反应的化学方程式 。为彻底消除污染,可将反应中产生的气体与V L(标准状况)空气混合通入水中,则V至少为 L(设空气中氧气的体积分数为0.2)。
(4)已知2Cu+ Cu+Cu2+,试分析CuAlO2分别与足量盐酸、稀硝酸混合后,产生现象的异同点 。
Cu+Cu2+,试分析CuAlO2分别与足量盐酸、稀硝酸混合后,产生现象的异同点 。
(5)假设粗银中的杂质只有少量的铜,利用电化学方法对其进行精炼,则粗银应与电源的 极相连,当两个电极上质量变化值相差30.4g时,则两个电极上银质量的变化值相差 g。
-
[化学---选修2:化学与技术](15分)银、铜均属于重金属,从银铜合金废料中回收银并制备含铜化合物产品的工艺如图所示:
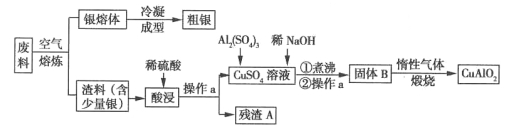
(1)熔炼时被氧化的元素是 ,酸浸时反应的离子方程式为 。为提高酸浸时铜元素的浸出率及浸出速率,酸浸前应对渣料进行处理,其处理方法是 。
(2)操作a是 ,固体B转化为CuAlO2的过程中,存在如下反应,请填写空白处:
CuO+ Al2O3 + ↑。
+ ↑。
(3)若残渣A中含有n mol Ag,将该残渣全部与足量的稀HNO3置于某容器中进行反应,写出反应的化学方程式 。为彻底消除污染,可将反应中产生的气体与V L(标准状况)空气混合通入水中,则V至少
为 L(设空气中氧气的体积分数为0.2)。
(4)已知2Cu+  Cu+Cu2+,试分析CuAlO2分别与足量盐酸、稀硝酸混合后,产生现象的异同点 。
Cu+Cu2+,试分析CuAlO2分别与足量盐酸、稀硝酸混合后,产生现象的异同点 。
(5)假设粗银中的杂质只有少量的铜,利用电化学方法对其进行精炼,则粗银应与电源的 极相连,当两个电极上质量变化值相差30.4 g时,则两个电极上银质量的变化值相差 g。
-
[化学—选修2:化学与技术](15分)银、铜均属于重金属,从银铜合金废料中回收银并制备含铜化合物产品的工艺如图所示:
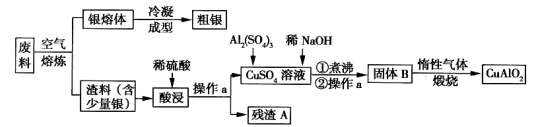
(1)熔炼时被氧化的元素是 ,酸浸时反应的离子方程式为 。为提高酸浸时铜元素的浸出率及浸出速率,酸浸前应对渣料进行处理,其处理方法是 。
(2)操作a是 ,固体B转化为CuAlO2的过程中,存在如下反应,请填写空白处:
CuO+ Al2O3 + ↑。
+ ↑。
(3)若残渣A中含有n mol Ag,将该残渣全部与足量的稀HNO3置于某容器中进行反应,写出反应的化学方程式 。为彻底消除污染,可将反应中产生的气体与V L(标准状况)空气混合通入水中,则V至少为 L(设空气中氧气的体积分数为0.2)。
(4)已知2Cu+  Cu+Cu2+,试分析CuAlO2分别与足量盐酸、稀硝酸混合后,产生现象的异同点 。
Cu+Cu2+,试分析CuAlO2分别与足量盐酸、稀硝酸混合后,产生现象的异同点 。
(5)假设粗银中的杂质只有少量的铜,利用电化学方法对其进行精炼,则粗银应与电源的 极相连,当两个电极上质量变化值相差30.4g时,则两个电极上银质量的变化值相差 g。
-
(12分)【化学—化学与技术】铜、银均属于重金属,从铜银合金废料中回收银并制备含铜化合物产品的工艺如图:

(1)酸浸时反应的离子方程式为________。为提高酸浸时铜元素的浸出率及浸出速率,酸浸前应对渣料进行处理,其处理方法是________。
(2)操作a是________。
(3)已知固体B中含有CuO和Al2O3,反应①的化学方程式为________。
(4)若残渣A中含有b mol Ag,将该残渣全部与足量的稀HNO3置于某容器中进行反应,写出反应的离子方程式_______,为消除污染,可将反应中产生的气体与VL(标准状况)空气混合通入水中,则V至少为________(设空气中氧的体积分数为0.2)。
-
I.银铜合金广泛用于航空工业。从切割废料中回收银并制备铜化工产品的工艺如下:

(注:Al(OH)3和Cu(OH)2开始分解的温度分别为450℃和80℃)
(1)固体混合物B的组成为 ;在生成固体B的过程中,需控制NaOH的加入量,若NaOH过量,则因过量引起的反应的离子方程式为 。
(2)完成煅烧过程中一个反应的化学方程式: 。
(3)若银铜合金中铜的质量分数为64%,理论上5.0kg废料中的铜可完全转化为CuAlO2,至少需要1.0mol·L-1的Al2(SO4)3溶液 L。
II.某同学用FeCl3溶液吸收H2S,得到单质硫;过滤后,再以石墨为电极,在一定条件下电解滤液。
(4)FeCl3与H2S反应的离子方程式为_______________________。
(5)电解池中H+在阴极放电产生H2,阳极的电极反应为____________________。
(6)综合分析实验II的两个反应,可知该实验有两个显著优点:
①H2S的原子利用率100%;
②____________________。
-
中国航空航天事业飞速发展,银铜合金广泛用于航空工业。从银铜合金切割废料中回收银并制备铜化工产品的工艺如下:
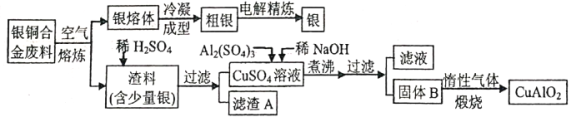
注:A1(OH)3和Cu(OH)2分解温度分别为450℃和80℃
(1)在电解精炼银时,阳极材料为___________。
(2)加快渣料(含少量银)溶于稀H2SO4速率的措施为___________(写出两种)。
(3)滤渣A与稀HNO3反应,产生的气体在空气中迅速变为红棕色,滤渣A与稀HNO3反应的离子方程式为______________________。
(4)过滤操作需要的玻璃仪器除烧杯外还有___________。
(5)固体混合物B的组成为___________;在生成固体B的过程中,需控制NaOH的加入量,若NaOH过量,则因过量引起的反应的离子方程式为___________。
(6)煅烧阶段通入惰性气体的原因___________。
-
中国航空航天事业飞速发展,银铜合金广泛用于航空工业。从银铜合金切割废料中回收银并制备铜化工产品的工艺如下:
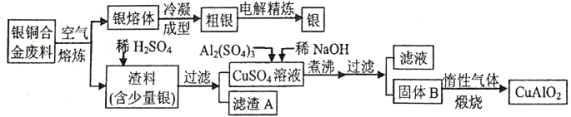
注:A1(OH)3和Cu(OH)2分解温度分别为450℃和80℃
(1)在电解精炼银时,阳极材料为___________。
(2)加快渣料(含少量银)溶于稀H2SO4速率的措施为___________(写出两种)。
(3)滤渣A与稀HNO3反应,产生的气体在空气中迅速变为红棕色,滤渣A与稀HNO3反应的离子方程式为______________________。
(4)过滤操作需要的玻璃仪器除烧杯外还有___________。
(5)固体混合物B的组成为___________;在生成固体B的过程中,需控制NaOH的加入量,若NaOH过量,则因过量引起的反应的离子方程式为___________。
(6)煅烧阶段通入惰性气体的原因___________。
-
中国航空航天事业飞速发展,银铜合金广泛用于航空工业。从银铜合金切割废料中回收银并制备铜化工产品的工艺如下:
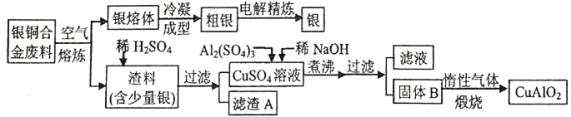
注:A1(OH)3和Cu(OH)2分解温度分别为450℃和80℃
(1)在电解精炼银时,阳极材料为___________。
(2)加快渣料(含少量银)溶于稀H2SO4速率的措施为___________(写出两种)。
(3)滤渣A与稀HNO3反应,产生的气体在空气中迅速变为红棕色,滤渣A与稀HNO3反应的离子方程式为______________________。
(4)过滤操作需要的玻璃仪器除烧杯外还有___________。
(5)固体混合物B的组成为___________;在生成固体B的过程中,需控制NaOH的加入量,若NaOH过量,则因过量引起的反应的离子方程式为___________。
(6)煅烧阶段通入惰性气体的原因___________。
-
从银铜合金废料中回收银并制备铜化工产品的工艺如下:
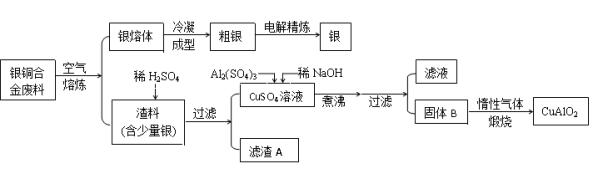
已知:①铝元素在溶液中的存在形态与溶液pH的关系如图所示。
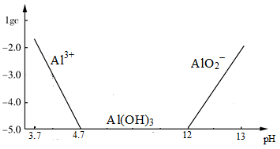
②室温时,Cu(OH)2的溶度积Ksp=2.0×10-20,当溶液中某种离子浓度小于1.0×10-5mol/L时,认为该离子沉淀完全, 。
。
③Al(OH)3和Cu(OH)2开始分解的温度分别为450℃和80℃。
请回答下列问题:
(1)电解精炼银时,粗银做 极(填“阴”或“阳”),电解质选用________溶液,阴极电极反应为 。
(2)在生成固体B的过程中,需控制NaOH的加入量,使溶液的pH范围在 ,若控制不当,使NaOH过量可能会引起的反应的离子方程式为 。
(3) 煅烧过程中发生多步反应,写出最终生成CuAlO2的反应的化学方程式: 。
(4)若银铜合金中铜的质量分数为64%,理论上1.0 kg废料中的铜可完全转化为CuAlO2,至少需要1.0 mol·L-1的Al2(SO4)3溶液 L。

+ ↑。
Cu+Cu2+,试分析CuAlO2分别与足量盐酸、稀硝酸混合后,产生现象的异同点 。









