下列有关说法正确的是( )
A.燃料电池工作时,燃料在负极被还原
B.氯碱工业采用的是以铜为电极,阳离子交换膜来电解饱和食盐水
C.有Mg、Al和NaOH溶液组成的原电池,其负极为铝,电极反应为Al-3e- = Al3+
D.二次电池充电时,电池负极连接到外接电源的负极
高二化学选择题简单题
下列有关说法正确的是( )
A.燃料电池工作时,燃料在负极被还原
B.氯碱工业采用的是以铜为电极,阳离子交换膜来电解饱和食盐水
C.有Mg、Al和NaOH溶液组成的原电池,其负极为铝,电极反应为Al-3e- = Al3+
D.二次电池充电时,电池负极连接到外接电源的负极
高二化学选择题简单题
下列有关说法正确的是( )
A.燃料电池工作时,燃料在负极被还原
B.氯碱工业采用的是以铜为电极,阳离子交换膜来电解饱和食盐水
C.有Mg、Al和NaOH溶液组成的原电池,其负极为铝,电极反应为Al-3e- = Al3+
D.二次电池充电时,电池负极连接到外接电源的负极
高二化学选择题简单题查看答案及解析
化学用语是学习化学的重要工具,下列用来表示物质变化的化学用语中,正确的是
A.氯碱工业中电解饱和食盐水时,阳极的电极反应为:2Cl--2e-=Cl2↑
B.氢氧燃料电池的负极反应:O2+2H2O+4e-=4OH-
C.粗铜精炼时,与电源正极相连的是纯铜,电极反应为:Cu-2e-=Cu2+
D.钢铁发生电化学腐蚀的正极反应:Fe-2e-=Fe2+
高二化学选择题中等难度题查看答案及解析
化学用语是学习化学的重要工具,下列用来表示物质变化的化学用语中,正确的是
A. 氯碱工业中电解饱和食盐水时,阳极的电极反应为:2Cl--2e-=Cl2↑
B. 氢氧燃料电池的负极反应:O2+2H2O+4e-=4OH-
C. 粗铜精炼时,与电源正极相连的是纯铜,电极反应为:Cu-2e-=Cu2+
D. 钢铁发生电化学腐蚀的正极反应:Fe-2e-=Fe2+
高二化学单选题中等难度题查看答案及解析
如图所示,某同学设计了一个燃料电池并探究氯碱工业原理和粗铜(含有少量锌、金、银等杂质)的精炼原理,其中乙装置中X为阳离子交换膜。回答下列问题:
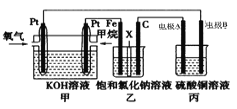
(1)甲烷燃料电池负极的电极反应式为_________。
(2)乙装置中阳离子通过X膜向________ 极(填“Fe”或“C”)移动;丙装置中粗铜为_______电极(填“A”或“B”)
(3)若在标况下,有2.24L氧气参与反应,则乙装置中右侧溶液________(填“增加”或“减少”)______g,丙装置中CuSO4浓度__________(填“增加”、“减少” 或“不变”)。
高二化学填空题中等难度题查看答案及解析
如图所示,某同学设计了一个燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜.下列有关说法正确的是( )
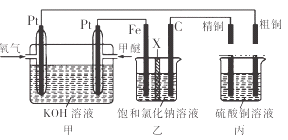
A. 反应一段时间后,乙装置中生成的氢氧化钠在铁极区
B. 乙装置中铁电极为阴极,电极反应式为Fe﹣2e ﹣=Fe2+
C. 通入氧气的一极为正极,发生的电极反应为O2﹣4e ﹣+2H2O═4OH﹣
D. 反应一段时间后,丙装置中硫酸铜溶液浓度保持不变
高二化学单选题困难题查看答案及解析
如图所示,某同学设计了一个燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。下列有关说法正确的是( )

A.反应一段时间后,乙装置中生成的氢氧化钠在铁极区
B.乙装置中铁电极为阴极,电极反应式为Fe-2e-=Fe2+
C.甲中通入氧气的一极为阳极,发生的电极反应为O2+4e-+2H2O=4OH-
D.反应一段时间后,丙装置中硫酸铜溶液浓度保持不变
高二化学单选题中等难度题查看答案及解析
如图所示,某同学设计了一个燃料电池并探究氯碱工业原理和粗铜(含有少量锌、金、银等杂质)的精炼原理,其中乙装置中X为阳离子交换膜。回答下列问题:
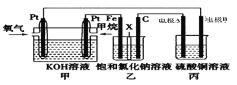
(1)甲烷燃料电池负极的电极反应式为_____________________。
(2)乙装置中阳离子通过X膜向________ 极(填“Fe”或“C”)移动,写出乙装置中的石墨电极上的电极方程式____________________________________。
(3)若在标况下,有2.24L氧气参与反应,则乙装置中右侧溶液________(填“增加”或“减少”)______g,丙装置中CuSO4浓度__________(填“增加”、“减少” 或“不变”);若将乙装置两侧溶液混合,常温下加水稀释至体积为4 L,则此时溶液液的pH=____。
高二化学综合题困难题查看答案及解析
如下图所示,某同学设计了一个燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。下列有关说法正确的是
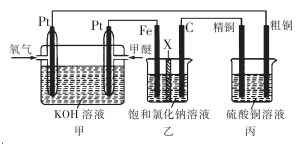
A. 反应一段时间后,乙装置中生成的氢氧化钠在铁极区
B. 乙装置中铁电极为阴极,电极反应式为Fe - 2e-=Fe2+
C. 通入氧气的一极为正极,发生的电极反应为O2-4e-+2H2O -4OH -
D. 反应一段时间后,丙装置中硫酸铜溶液浓度保持不变
高二化学选择题困难题查看答案及解析
如图所示,某同学设计一个燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜.根据要求回答相关问题:

(1)甲烷燃料电池的负极反应式______.
(2)石墨电极(C)的电极反应式为______.
(3)如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,硫酸铜溶液浓度将______(填“增大”“减小”或“不变”).
(4)若在标准状况下,有2.24L氧气参加反应,则乙装置中铁电极上生成标况下气体的的体积为______;丙装置中阴极析出铜的质量为______.
高二化学综合题中等难度题查看答案及解析
如图1所示,某同学设计了一个燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙烧杯中X为阳离子交换膜。请按要求回答相关问题:
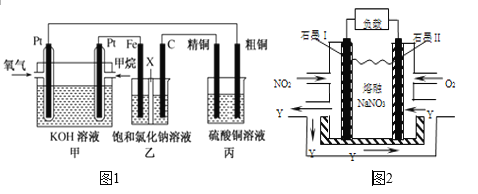
(1)甲烷燃料电池负极电极反应式是___________;正极电极反应式是___________________
(2)石墨(C)为__________极,其电极反应式为____________________________;乙中总反应的离子方程式为__________________________________________________
(3)若在标准状况下,有2.24 L氧气参加反应,则丙装置中阴极析出铜的质量为_________g ;
(4)若将甲装置中的甲烷换成甲醇(CH3OH),KOH溶液换成稀硫酸,则负极电极反应式为___________,消耗等量氧气时,需要甲烷与甲醇的物质的量之比为_________。
(5)NO2、O2和熔融NaNO3可制作燃料电池,其原理见图2,该电池在使用过程中石墨I电极上生成氧化物Y,其电极反应式为________________________________
高二化学综合题困难题查看答案及解析