A.
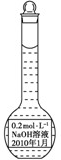
B.

C.

D.

高三化学选择题中等难度题




高三化学选择题中等难度题




高三化学选择题中等难度题查看答案及解析
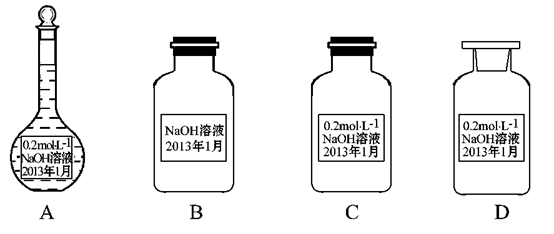
某实验小组配制了0.2 mol·L-1的NaOH的溶液备用,下列保存方法正确的是( )
高三化学选择题中等难度题查看答案及解析
(12分)某研究性学习小组利用手持技术探究强碱和不同的酸中和反应的过程如下:
(1)实验步骤:
①分别配制浓度均为0.1mol·L-1的NaOH、HC1、CH3 C00H、H3PO4溶液备用。配制过程中用到的玻璃仪器有烧杯、容量瓶、玻璃棒、细口瓶、____、____。
②在锥形瓶中加入10mL0.1 mol.L-1的HC1,在25.00mL____(填“酸式”、“碱式”)滴定管中加入0.1 mol.L-1的NaOH,连接数据采集器和pH传感器。
③向锥形瓶中滴入NaOH,接近估算的NaOH用量附近时,减慢滴加速度,等读数稳定后,再滴下一滴NaOH。
④存储计算机绘制的pH变化图。用0.1 mol·L-1的CH3 C00H、H3 P04溶液代替HC1重复上述②~④的操作。
(2)结果分析:20℃时NaOH分别滴定HC1、CH3 C00H、H3 P04的pH变化曲线如下。
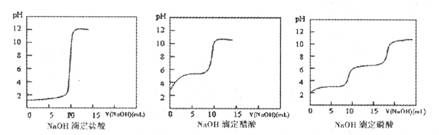
根据上述曲线回答下列问题:
①20℃时,三种酸从强到弱的顺序是________;
②滴定开始后醋酸曲线变化比盐酸快的原因是________;
③醋酸恰好中和时pH≈8的原因是________ ;
④你认为前述的步骤中,NaOH滴定磷酸是否可行?________(填“可行”、“不可行”)。
高三化学填空题简单题查看答案及解析
下列关于实验原理或操作的叙述,正确的是( )
A.实验室欲用480 mL 0.2 mol·L-1 H2SO4溶液,可用500 mL容量瓶配制
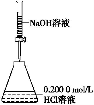
B.用如图所示装置测定NaOH溶液的浓度
C.铜与浓硫酸反应时,用蘸有浓溴水的棉花放在导管口吸收多余的气体
D.用pH试纸测得新制氯水的pH为4
高三化学选择题中等难度题查看答案及解析
实验是解决化学问题的基本途径,下列有关实验的叙述不正确的是
A.240 mL 0.2 mol·L-1的NaOH溶液配制:需要使用天平、烧杯、250 mL容量瓶等仪器
B.除去Cu粉中的CuO,可向混合物中滴加适量稀硫酸再过滤
C.为增强氯水的漂白性,向其中加入碳酸钙
D.为使0.5mol/L的NaNO3溶液物质的量浓度变为1mol/L,可将原溶液加热蒸发掉50克水
高三化学选择题中等难度题查看答案及解析
Ⅰ。一定物质的量浓度溶液的配制和酸碱中和滴定是中学化学中两个典型的定量实验。某研究性学习小组在实验室中配制1mol/L的稀硫酸标准溶液,然后用其滴定某未知浓度的NaOH溶液。下列有关说法中正确的是______________(答案可能不唯一)
A、实验中所用到的滴定管、容量瓶,在使用前均需要检漏;
B、如果实验中需用60mL 的稀硫酸标准溶液,配制时应选用100mL容量瓶;
C、容量瓶中含有少量蒸馏水,会导致所配标准溶液的浓度偏小;
D、酸式滴定管用蒸馏水洗涤后,即装入标准浓度的稀硫酸,则测得的NaOH溶液的浓度将偏大;
E、用甲基橙作指示剂,滴定终点时,溶液颜色从橙色变为红色;
F、配制溶液和中和滴定的两个实验中,若在最后一次读数均俯视读数,则导致实验结果都偏大。
Ⅱ . 现用如图所示的装置制取较多量的饱和氯水并测定饱和氯水的pH。
回答有关问题:
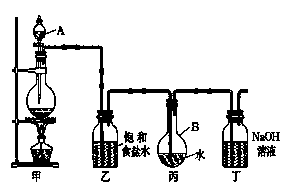
(1)写出有关化学方程式。
装置甲:____________________________________ ;
装置丁:__________________________________。
(2)证明氯水已饱和的现象是 。
(3)制取结束时,装置丙的液体中含有的微粒是 (用微粒符号表示 );
(4)若撤去装置乙,直接将装置甲和丙相连。这样做对实验测定结果的影响是:________。
测定饱和氯水的pH方法是_______________________________________________。
Ⅲ.实验设计:证明NaOH固体在空气中放置部分变质
_______________________________________________________________
_______________________________________________________________________
高三化学实验题中等难度题查看答案及解析
某项目小组同学发现某一种胃药片的止酸剂为碳酸钙,为了测定其中止酸剂的质量特制定了如下操作步骤:
①配制0.2mol·L-1的HCl溶液和0.2mol·L-1的NaOH溶液;②每次取一粒(药片质量均相同)0.2g的此胃药片,磨碎后放入锥形瓶中再加入20mL蒸馏水;③以酚酞作指示剂,用0.2mol·L-1的NaOH溶液滴定,需用去VmL达滴定终点;④加入25mL0.2mol·L-1的HCl溶液。
(1)写出全部实验过程的操作步骤的顺序:__。
(2)如图所示的仪器中配制0.2mol·L-1的HCl溶液和0.2mol·L-1NaOH溶液肯定不需要的仪器是__(填序号),配制上述溶液还需用到的玻璃仪器是__(填仪器名称)。
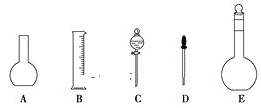
(3)配制上述溶液应选用的容量瓶的规格分别为__(填字母)。
A.50mL、50mL B.100mL、100mL
C.100mL、150mL D.250mL、250mL
(4)配制过程中,下列情况会使配制结果偏高的是__(填序号)。
A.洗净后容量瓶内还残留蒸馏水未烘干
B.量取浓盐酸时,仰视刻度线观察液面
C.定容时,仰视刻度线
D.定容后,加盖倒转摇匀后,发现液面低于刻度线又加水至刻度线
高三化学实验题中等难度题查看答案及解析
第三研究性学习小组发现某一种胃药片的制酸剂为碳酸钙,为了测定其中制酸剂的质量特制定了如下操作步骤:
①配制0.2 mol·L-1的HCl溶液和0.2 mol·L-1的NaOH溶液;②每次取一粒(药片质量均相同)0.2 g的此胃药片,磨碎后放入锥形瓶中再加入20 mL蒸馏水;③以酚酞作指示剂,用0.2 mol·L-1的NaOH溶液滴定,需用去V mL达滴定终点;④加入25 mL 0.2 mol·L-1的HCl溶液。
(1)写出全部实验过程的操作步骤的顺序:____________。
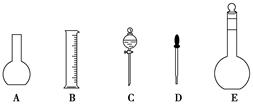
(2)上图所示的仪器中配制0.2 mol·L-1的HCl溶液和0.2 mol·L-1NaOH溶液肯定不需要的仪器是________(填序号),配制上述溶液还需用到的玻璃仪器是________(填仪器名称)。
(3)配制上述溶液应选用的容量瓶的规格分别为________(填字母)。
A.50 mL、50 mL B.100 mL、100 mL
C.100 mL、150 mL D.250 mL、250 mL
(4)写出相关的化学反应方程式:
________________________________________________________________________。
(5)做2次平行实验后,则每粒胃药片中含碳酸钙的质量表达式为________________g。
高三化学填空题中等难度题查看答案及解析
下列实验数据记录和实验方法正确的是
A.用天平称取4.0g NaOH固体,用100mL量筒配制1.00 mol·L-1的NaOH溶液
B.使用25mL碱式滴定管(内装有标准NaOH溶液),滴定未知浓度的盐酸,用去NaOH溶液22.32mL
C.使用pH试纸测得新制氯水的pH为4
D.常温常压下,收集500mLNO2气体,则NO2气体的物质的量为(0.5/22.4)mol
高三化学选择题中等难度题查看答案及解析
实验室需要0.2 mol·L-1NaOH溶液480 mL和0.5 mol·L-1硫酸溶液500 mL。根据这两种溶液的配制情况回答下列问题:
(1)如图所示的仪器中配制溶液肯定不需要的是________(填序号),配制上述溶液还需用到的玻璃仪器是________(填仪器名称)。
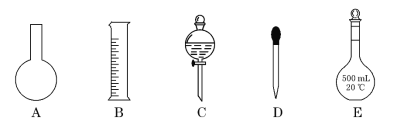
(2)下列有关容量瓶使用方法的操作中,错误的是_______。
A.使用容量瓶之前应检查它是否漏水
B.容量瓶用蒸馏水洗净后,再用待配溶液润洗
C.定容时,将蒸馏水小心倒入容量瓶中直至与刻度线齐平
D.配制溶液时,如果试样是液体,用量筒量取试样后直接倒入容量瓶中定容
E.盖好瓶塞,用食指顶住瓶塞,另一只手托住瓶底,把容量瓶反复上下颠倒,摇匀
(3)在配制NaOH溶液时:
①根据计算用托盘天平称取NaOH的质量为________g;
②若NaOH溶液在转移至容量瓶时,洒落了少许,则所得溶液浓度________(填“>”“<”或“=”)0.2 mol·L-1;
③若NaOH固体溶解后立即移入容量瓶→洗烧杯→洗涤液移入容量瓶→定容,则所得溶液浓度________(填“>”“<”或“=”)0.2 mol·L-1。
(4)在配制硫酸溶液时:
①所需质量分数为98%、密度为1.84 g·cm-3的浓硫酸的体积为________(计算结果保留一位小数)mL;
②如果实验室有15 mL、20 mL、50 mL量筒,应选用______mL量筒最好;
③配制过程中需先在烧杯中将浓硫酸进行稀释,稀释时操作方法是___________________________________________________________________________。
高三化学填空题中等难度题查看答案及解析