已知25℃时CH3COOH的电离常数K=1.6×10-5。该温度下向20ml 0.01mol·L-1 CH3COOH溶液中逐滴加入0.01mol·L-1 KOH溶液,其pH变化曲线如图所示(忽略温度变化),下列有关叙述正确的是

A. a点溶液中c(H+)为4.0×10-5mol/L
B. c点溶液中的离子浓度大小顺序为c(K+)>c(CH3COO->c(H+)=c(OH-)
C. V=200
D. a、b、c三点中水的电离程度最大的是c点
高三化学选择题中等难度题
已知25℃时CH3COOH的电离常数K=1.6×10-5。该温度下向20ml 0.01mol·L-1 CH3COOH溶液中逐滴加入0.01mol·L-1 KOH溶液,其pH变化曲线如图所示(忽略温度变化),下列有关叙述正确的是

A. a点溶液中c(H+)为4.0×10-5mol/L
B. c点溶液中的离子浓度大小顺序为c(K+)>c(CH3COO->c(H+)=c(OH-)
C. V=200
D. a、b、c三点中水的电离程度最大的是c点
高三化学选择题中等难度题
已知某温度下CH3COOH的电离常数K=1.6×10-5。该温度下向20 mL 0.01 mol/L CH3COOH溶液中逐滴加入0.01 mol/L KOH溶液,其pH变化曲线如图所示(忽略温度变化)。请回答下列有关问题:

(1)a点溶液中c(H+)为 。
(2)b点溶液中离子浓度大小顺序为 或 或 。c点溶液中的离子浓度大小顺序为 。
(3)a、b、c三点中水的电离程度最大的是 ,滴定过程中宜选用 作指示剂。
高三化学选择题中等难度题查看答案及解析
已知25℃时CH3COOH的电离常数K=1.6×10-5。该温度下向20ml 0.01mol·L-1 CH3COOH溶液中逐滴加入0.01mol·L-1 KOH溶液,其pH变化曲线如图所示(忽略温度变化),下列有关叙述正确的是

A. a点溶液中c(H+)为4.0×10-5mol/L
B. c点溶液中的离子浓度大小顺序为c(K+)>c(CH3COO->c(H+)=c(OH-)
C. V=200
D. a、b、c三点中水的电离程度最大的是c点
高三化学选择题中等难度题查看答案及解析
(6分)已知某温度下CH3COOH的电离常数K=1.6×10-5。该温度下向20mL0.01mol/LCH3COOH溶液中逐滴加入0.01mol/L KOH溶液,其pH变化曲线如下图所示(忽略温度变化)。请回答下列有关问题:
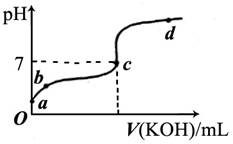
(1)a点溶液中c(H+)为________。
(2)b点溶液中离子浓度的大小顺序可能有________种情况。
(3)a、b、c三点中水的电离程度最大的是________。
高三化学填空题简单题查看答案及解析
已知25℃时醋酸的电离常数为1.6×10-5,该温度下向20 mL 0.01 mol·L-1醋酸溶液中不断滴入0.01 mol·L−1 NaOH(aq),溶液pH变化如图所示。此过程溶液中离子浓度的关系错误的是
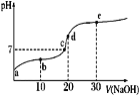
A. a点溶液的c(H+)=4×10-4mol·L-1
B. 水电离程度:e>d>c>b>a
C. b点:2c(Na+)=c(CH3COO-)+c(CH3COOH)
D. d点:c(OH-)=c(CH3COOH)+c(H+)
高三化学单选题中等难度题查看答案及解析
已知25℃时醋酸的电离常数为1.6×10-5,该温度下向20 mL 0.01 mol·L-1醋酸溶液中不断滴入0.01 mol·L−1 NaOH(aq),溶液pH变化如图所示。此过程溶液中离子浓度的关系错误的是
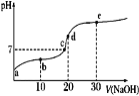
A.a点溶液的c(H+)=4×10-4mol·L-1
B.水电离程度:e>d>c>b>a
C.b点:2c(Na+)=c(CH3COO-)+c(CH3COOH)
D.d点:c(OH-)=c(CH3COOH)+c(H+)
高三化学单选题中等难度题查看答案及解析
已知25℃时醋酸的电离常数为1.6×10-5,该温度下向20 mL 0.01 mol·L-1醋酸溶液中不断滴入0.01 mol·L−1 NaOH(aq),溶液pH变化如图所示。此过程溶液中离子浓度的关系错误的是
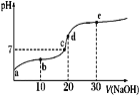
A.a点溶液的c(H+)=4×10-4mol·L-1
B.水电离程度:e>d>c>b>a
C.b点:2c(Na+)=c(CH3COO-)+c(CH3COOH)
D.d点:c(OH-)=c(CH3COOH)+c(H+)
高三化学单选题中等难度题查看答案及解析
已知25℃时醋酸的电离常数为1.6×10-5,该温度下向20 mL 0.01 mol·L-1醋酸溶液中不断滴入0.01 mol·L−1 NaOH(aq),溶液pH变化如图所示。此过程溶液中离子浓度的关系错误的是
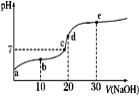
A.a点溶液的c(H+)=4×10-4mol·L-1
B.水电离程度:e>d>c>b>a
C.b点:2c(Na+)=c(CH3COO-)+c(CH3COOH)
D.d点:c(OH-)=c(CH3COOH)+c(H+)
高三化学单选题中等难度题查看答案及解析
已知常温时CH3COOH的电离平衡常数Ka=1.75×10−5,NH3·H2O的电离平衡常数Kb=1.75×10−5。常温时,向10 mL浓度均为0.01mol·L−1的NaOH和氨水混合溶液中,逐滴加入0.01mol·L−1的 CH3COOH 溶液,混合溶液的pH与加入CH3COOH的体积V之间的变化曲线如图所示,下列有关说法正确的是
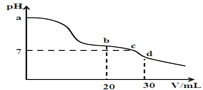
A. a 点溶液的pH<12
B. b 点时水的电离程度最大
C. c 点处的微粒间存在:c(CH3COO−)=c(NH4+)+c(NH3·H2O)
D. d 点处的微粒间存在:c(CH3COO−)>c(H+)>c(Na+)>c(NH4+)>c(OH−)
高三化学单选题困难题查看答案及解析
已知常温时CH3COOH的电离平衡常数Ka=1.75×10−5,NH3·H2O的电离平衡常数Kb=1.75×10−5。常温时,向10 mL浓度均为0.01mol·L−1的NaOH和氨水混合溶液中,逐滴加入0.01mol·L−1的 CH3COOH 溶液,混合溶液的pH与加入CH3COOH的体积V之间的变化曲线如图所示,下列有关说法正确的是

A. a 点溶液的pH<12
B. b 点时水的电离程度最大
C. c 点处的微粒间存在:c(CH3COO−)=c(NH4+)+c(NH3·H2O)
D. d 点处的微粒间存在:c(CH3COO−)>c(H+)>c(Na+)>c(NH4+)>c(OH−)
高三化学单选题困难题查看答案及解析
已知常温下CH3COOH和NH3·H2O的电离常数相等,现向10mL浓度为0.01mol/L的氨水溶液中滴加相同浓度的CH3COOH溶液,在滴加过程中溶液的pH与所加醋酸的体积关系如图所示。下列说法错误的是
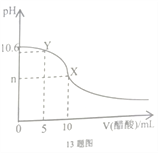
A. n=7
B. 水的电离程度先增大再减小
C. 常温下,0.01mol/L的氨水溶液中NH3·H2O的电离度为3.98%
D. Y点溶液中c(NH3·H2O)+(OH-)=c(CH3COO-)+c(H+)
高三化学单选题中等难度题查看答案及解析