-
五种不同元素X、Y、Z、D、E、F的信息如下:
元素
有关信息
X
元素主要常见化合价为-2和-1价,原子半径为0.074 nm。
Y
所在主族序数与所在周期序数之差为4。
Z
原子半径为0.102 nm,核外最外层电子数是其电子层数的2倍,其气态氢化物与Y单质发生反应生成淡黄色固体。
D
最高价氧化物对应的水化物,能电离出离子数、电子数都相等的阴、阳离子。
E
单质是生活中常见金属,其制品在潮湿空气中易被腐蚀或损坏。
F
元素所在的主族序数等于周期序数。
请回答下列问题:
(1)Z在周期表中的位置_________,D的最高价氧化物对应水化物的电子式为__________
(2)X单质与D单质反应生成的D2X2能和H2O反应,写出其离子方程式为 。
(3)E元素与Y元素可形成EY2和EY3两种化合物,向淀粉碘化钾溶液滴加几滴EY3的浓溶液,原无色溶液可变为紫色,其原因是 (用离子方程式表示)。
(4)E单质在发生吸氧腐蚀时的正极反应方程式
(5)F的一种复盐常用作净水剂,用离子方程式表示其净水原理
高三化学填空题中等难度题查看答案及解析
-
元素周期表是学习化学的重要工具,它隐含许多信息和规律。下表所列是五种短周期元素的原子半径及主要化合价:
元素代号 A B C D E
原子半径/nm 0.16 0.143 0.102 0.089 0.074
主要化合价 +2 +3 +6,-2 +2 -2
(1)在下表中标出上述五种元素在元素周期表中的对应位置(用元素符号)。
(2)在下表中标明通常寻找催化剂材料的区域(用斜线阴影)。

(3)A、B、E三种元素各自形成简单离子,其中半径最大的为________(填离子符号)。
(4)证明B元素的单质与A元素的单质在化学性质上有明显不同的离子方程式为:________________________。
(5)周期表中有些处于对角(左上→右下)位置的元素,它们的单质及其化合物的性质存在“对角线相似”的现象,请写出D的氧化物与强碱溶液反应的离子方程式:________________________。
高三化学填空题困难题查看答案及解析
-
元素周期表是学习化学的重要工具,它隐含许多信息和规律。下表所列是五种短周期元素的原子半径及主要化合价:
元素代号 A B C D E
原子半径/nm 0.16 0.143 0.102 0.089 0.074
主要化合价 +2 +3 +6,-2 +2 -2
(1)在下表中标出上述五种元素在元素周期表中的对应位置(用元素符号)。
(2)在下表中标明通常寻找催化剂材料的区域(用斜线阴影)。

(3)A、B、E三种元素各自形成简单离子,其中半径最大的为________(填离子符号)。
(4)证明B元素的单质与A元素的单质在化学性质上有明显不同的离子方程式为:________________________。
(5)周期表中有些处于对角(左上→右下)位置的元素,它们的单质及其化合物的性质存在“对角线相似”的现象,请写出D的氧化物与强碱溶液反应的离子方程式:________________________。
高三化学填空题简单题查看答案及解析
-
元素周期表隐含着许多信息和规律。以下所涉及的元素均为中学化学中常见的短周期元素,其原子半径及主要化合价列表如下,其中R2Q2用于呼吸面具或潜水艇中作为氧气来源。下列说法正确的是
元素代号
M
R
Q
T
X
Y
Z
原子半径/nm
0.037
0.186
0.074
0.102
0.150
0.160
0.099
主要化合价
+1
+1
-2
+6 -2
+3
+2
-1
A.T、Z的氧化物对应水化物的酸性T<Z B.R、X、Y的单质失去电子能力最强的是X
C.X与Z形成的是共价化合物 D.M、Q、Z都在第2周期
高三化学单选题中等难度题查看答案及解析
-
元素周期表隐含着许多信息和规律。以下所涉及的元素均为中学化学中常见的短周期元素,其原子半径及主要化合价列表如下,其中R2Q2用于呼吸面具或潜水艇中作为氧气来源。

下列说法正确的是
A. T、Z的最高价氧化物对应水化物的酸性T<Z
B. R、X、Y的单质失去电子能力最强的是X
C. M与Q形成的是离子化合物
D. M、Q、Z都在第2周期
高三化学单选题简单题查看答案及解析
-
元素周期表隐含着许多信息和规律。以下所涉及的元素均为中学化学中常见的短周期元素,其原子半径及主要化合价列表如下,其中R2Q2用于呼吸面具或潜水艇中作为氧气来源。
元素代号
M
R
Q
T
X
Y
Z
原子半径/nm
0.037
0.186
0.074
0.102
0.150
0.160
0.099
主要化合价
+1
+1
-2
-2、+4、+6
+3
+2
-1
下列说法正确的是
A. T、Z的最高价氧化物对应水化物的酸性T<Z
B. R、X、Y的单质失去电子能力最强的是X
C. M与Q形成的是离子化合物
D. M、Q、Z都在第2周期
高三化学单选题中等难度题查看答案及解析
-
(12分)有关元素X、Y、Z、D、E的信息如下
元素
有关信息
X
元素主要化合价为—2,原子半径为0.074nm
Y
所在主族序数与所在周期序数之差为4
Z
原子半径为0.102nm,核外最外层电子数是其电子层数的2倍,其单质在X的单质中燃烧,产生的气体通入品红中,品红褪色。
D
最高价氧化物对应的水化物,是强电解质,能电离出电子数相等的阴、阳离子
E
单质是生活中常见金属,其制品在潮湿空气中易被腐蚀或损坏
请回答下列问题:
(1)X的一种氢化物可用于实验室制取X的单质,其反应的化学方程式为________。
(2)E元素与Y元素可形成EY2和EY3两种化合物,下列说法正确的是(填序号)________。
①保存EY2溶液时,需向溶液加入少量E单质
②通常实验室配制EY3溶液时,直接用水溶解EY3固体即可
③EY2只能通过置换反应生成,EY3只能通过化合反应生成
④铜片、碳棒和EY3溶液组成原电池,电子由铜片沿导线流向碳棒
(3)用电子式表示D2Z的形成过程:________,D2Z水溶液显________性
用离子方程式表示其原因________
(4)2009年3月,墨西哥、美国等多国连接暴发甲型H1N1型流感,防控专家表示,含Y消毒剂和过氧化物可防甲型H1N1流感。YO2是目前国际上公认的第四代高效、无毒的广谱消毒剂,它可由KYO3在H2ZO4存在下与D2ZO3反应制得。请写出反应的离子方程式:________。
(5)将一定量的Y单质通入一定浓度的苛性钾溶液中,两者恰好完全反应(已知反应过程放热),生成物中
有三种含Y元素的离子,其中两种离子的物质的量(n)与反应时间(t)的变化示意图如右图所示。
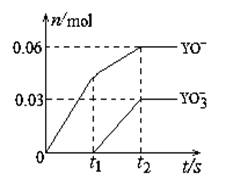
该苛性钾溶液中KOH的质量是g,该反应中转移电子的物质的量是mol。
高三化学填空题中等难度题查看答案及解析
-
有关元素X、Y、Z、D、E的信息如下
用化学用语答下列问题:元素 有关信息 X 元素主要化合价为-2,原子半径为0.074nm Y 所有主族序数与所在周期序数之差为4 Z 原子半径为0.102nm,其单质在X的单质中燃烧,发出明亮的蓝紫色火焰 D 最高价氧化物既能溶于强酸又能溶于强碱 E 单质是生活中常见金属,其制品在潮湿空气中易被腐蚀或损坏
(1)E在元素周期表中的位置为________;Z的氢化物电子式为________
(2)沸点:硒化氢________X的氢化物(填“>”或“<”).
X、Y、D形成的简单离子的半径由大到小为________.
(3)X的一种氢化物可用于实验室制取X的单质,其反应的化学方程式为________,D的最高价氧化物溶于强碱的离子方程式为________.
(4)E元素与Y元素可形成EY2和 EY3两种化合物,下列说法正确的是(填序号)________.
①保存EY2溶液时,需向溶液加入少量E单质
②EY2、E2Y3均能通过化合反应生成
③铜片、碳棒和EY3溶液组成原电池,电子由铜片沿导线流向碳棒
④向煮沸的NaoH溶液中滴加几滴饱和EY3溶液,可以制得胶体
(5)右图所示物质均为常见化合物,其中甲为上述五种元素中的两种组成,乙在常温下为液态,工业上常用电解戊冶炼金属,则甲与乙发生反应的化学方程式________.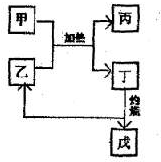
高三化学填空题中等难度题查看答案及解析
-
有关元素X、Y、Z、D、E的信息如下:
(1)画出Y的离子结构示意图______;元素 有关信息 X 元素主要化合价为-2,原子半径为0.074nm Y 所在主族序数与所在周期序数之差为4 Z 原子半径为0.102nm,其单质在X的单质中燃烧,发出明亮的蓝紫色火焰 D 最高价氧化物对应的水化物,能按1:1电离出电子数相等的阴、阳离子 E 其单质有多种同素异形体,一种为自然界中硬度最大
(2)写出D的最高价氧化物的水化物电离出的阴离子的电子式______;
(3)D2ZX3的溶液与Y的单质可能发生反应,其反应的离子方程式为______;
(4)用化学符号表示D2EX3的水溶液中各离子的浓度关系(列等式)______;
(5)已知ZX2与X2可发生反应:2ZX2(g)+X2(g)⇌2ZX3(g)△H<0;
当反应达到平衡时不断改变条件(不改变ZX2、X2、ZX3的量),反应速率随时间的变化如图:
其中表示平衡混合物中ZX3含量最高的一段时间是______;如t~t1平衡常数为K1,t2~t3平衡常数为K2,则K1______K2
(填“大于”、“等于”或“小于”).高三化学解答题中等难度题查看答案及解析
-
有关元素X、Y、Z、D、E的信息如下
请回答下列问题:元素 有关信息 X 元素主要化合价为-2,原子半径为0.074nm Y 所在主族序数与所在周期序数之差为4 Z 原子半径为0.102nm,其单质在X的单质中燃烧,发出明亮的蓝紫色火焰 D 最高价氧化物对应的水化物,能电离出电子数相等的阴、阳离子 E 单质是生活中常见金属,其制品在潮湿空气中易被腐蚀或损坏
(1)X的一种氢化物可用于实验室制取X的单质,其反应的化学方程式为______ 2H2O+O2↑高三化学解答题中等难度题查看答案及解析