-
(15分)对叔丁基苯酚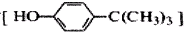 工业用途广泛,可用于生产油溶性酚醛树脂、稳定剂和香料等。实验室以苯酚、叔丁基氯[(CH3)3CCl]等为原料制备对叔丁基苯酚。实验步骤如下:反应物和产物的相关数据列表如下:
工业用途广泛,可用于生产油溶性酚醛树脂、稳定剂和香料等。实验室以苯酚、叔丁基氯[(CH3)3CCl]等为原料制备对叔丁基苯酚。实验步骤如下:反应物和产物的相关数据列表如下:
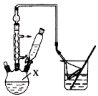
步骤l:组装仪器,用量筒量取2.2 mL叔丁基氯(过量),称取1.6 g苯酚,搅拌使苯酚完全溶解,并装入滴液漏斗。
步骤2:向X中加入少量无水AlCl3固体作催化剂,打开滴液漏斗旋塞,迅速有气体放出。
步骤3:反应缓和后,向X中加入8 mL水和1 mL浓盐酸,即有白色固体析出。
步骤4:抽滤得到白色固体,洗涤,得到粗产物,用石油醚重结晶,得对叔丁基苯酚1.8 g。
(1)仪器X的名称为 。
(2)步骤2中发生主要反应的化学方程式为 。该反应过于激烈,放出大量热,常使实验的产率降低,可能的原因是 。
(3)图中倒扣漏斗的作用是 。苯酚有腐蚀性,能使蛋白质变性,若其溶液沾到皮肤上可用 洗涤。
(4)在取用苯酚时发现苯酚冻结在试剂瓶中,可采取的措施为____ 。
(5)下列仪器在使用前必须检查是否漏液的是 (填选项字母)。
A.量筒
B.容量瓶
C.滴定管
D.分液漏斗
E.长颈漏斗
(6)本实验中,对叔丁基苯酚的产率为 。(请保留三位有效数字)
-
对叔丁基苯酚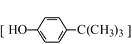 可用于生产油溶性酚醛树脂等。实验室以苯酚、叔丁基氯[(CH3)3CCl]等为原料制备对叔丁基苯酚的实验步骤如下:
可用于生产油溶性酚醛树脂等。实验室以苯酚、叔丁基氯[(CH3)3CCl]等为原料制备对叔丁基苯酚的实验步骤如下:
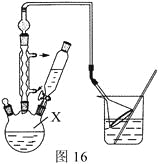
步骤1:按图16组装仪器,在X中加入2.2 mL叔丁基氯(过量)和1.41 g苯酚,搅拌使苯酚完全溶解。
步骤2:向X中加入无水AlCl3固体作催化剂,不断搅拌,有气体放出。
步骤3:反应缓和后,向X中加入8 mL水和1 mL浓盐酸,即有白色固体析出。
步骤4:抽滤得到白色固体,洗涤,用石油醚重结晶,得对叔丁基苯酚1.8 g。
(1)仪器X的名称为________。
(2)步骤2中发生主要反应的化学方程式为________。若该反应过于激烈,可采取的一种措施为________。
(3)图16中倒扣漏斗的作用是________。
(4)实验结束后,对产品进行光谱鉴定结果如下。其中属于红外光谱的谱图是________(填字母)。
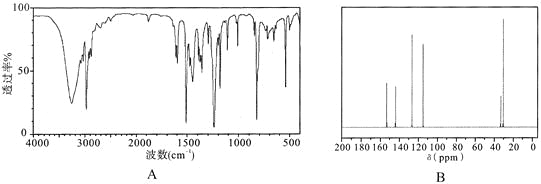
(5)本实验中,对叔丁基苯酚的产率为________。
-
对叔丁基苯酚 可用于生产油溶性酚醛树脂等。实验室以苯酚、叔丁基氯[(CH3)3CCl]等为原料制备对叔丁基苯酚的实验步骤如下:
可用于生产油溶性酚醛树脂等。实验室以苯酚、叔丁基氯[(CH3)3CCl]等为原料制备对叔丁基苯酚的实验步骤如下:
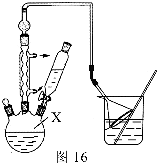
步骤1:按图16组装仪器,在X中加入2.2 mL叔丁基氯(过量)和1.41 g苯酚,搅拌使苯酚完全溶解。
步骤2:向X中加入无水AlCl3固体作催化剂,不断搅拌,有气体放出。
步骤3:反应缓和后,向X中加入8 mL水和1 mL浓盐酸,即有白色固体析出。
步骤4:抽滤得到白色固体,洗涤,用石油醚重结晶,得对叔丁基苯酚1.8 g。
(1)仪器X的名称为 。
(2)步骤2中发生主要反应的化学方程式为 。若该反应过于激烈,可采取的一种措施为 。
(3)图16中倒扣漏斗的作用是 。
(4)实验结束后,对产品进行光谱鉴定结果如下。其中属于红外光谱的谱图是 (填字母)。
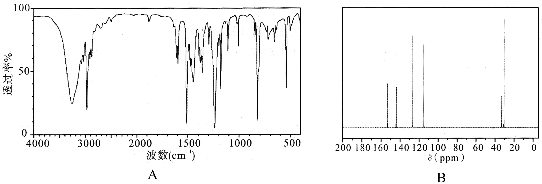
(5)本实验中,对叔丁基苯酚的产率为 。
-
叔丁基氯 与碱溶 液经两步反应 得到叔丁基醇,反应 (CH3)3CCl+OH-→(CH3)3COH+Cl-的能量与反应进程如图所示:
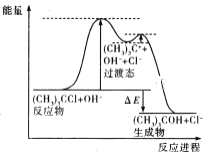
下列说法正确的是
A. 该反应为吸热反应
B. (CH3)3C+比(CH3)3 CCl 稳定
C. 第一步反应一定比第二步反应快
D. 增大碱的浓度和升高温度均可加快反应速率
-
叔丁基氯与碱溶液经两步反应得到叔丁基醇,反应(CH3)3CCl+OH-→ (CH3)3COH+Cl-的能量与反应进程如图所示:
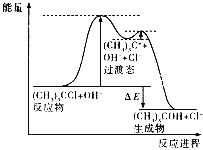
下列说法正确的是
A. 该反应为吸热反应
B. (CH3)3C+比(CH3)3 CCl稳定
C. 第一步反应一定比第二步反应快
D. 增大碱的浓度和升高温度均可加快反应速率
-
异丁烯[CH2=C(CH3)2]是重要的化工原料。
已知:
(1)异丁烯和苯酚在一定条件下反应生成对叔丁基酚( ),该反应属于_________反应(填“反应类型”).
),该反应属于_________反应(填“反应类型”).
(2)对叔丁基酚和甲醛在催化剂作用下可生成油溶性聚合物,写出该反应的化学方程式________________。
(3)写出符合下列条件的对叔丁基酚的所有同分异构体的结构简式________________________________。
①含相同官能团;②不属于酚类;③苯环上的一溴代物只有一种。
(4)已知由异丁烯的一种同分异构体A,经过一系列变化可合成物质,其合成路线如图:

①条件1为_____________;
②写出结构简式:A_____________;B____________。
(5)异丁烯可二聚生成CH2=C(CH3)CH2C(CH3)3,写出该二聚物的名称__________。异丁烯二聚时,还会生成其他的二聚烯烃类产物,写出其中一种链状烯烃的结构简式________________________________。
-
物质的用途错误的是
A.草酸可用于提炼稀有金属 B.苯酚可用于制造酚醛树脂
C.浓硫酸可用于实验室制取HCl(g) D.氯化铵溶液可用于除去金属表面油污
-
邻苯二甲酸丁基月桂酯是一种淡黄色透明油状液体,密度约0.97g/cm3,常用作聚氯乙烯等树脂的增塑剂。工业上生产原理和工艺流程如下:
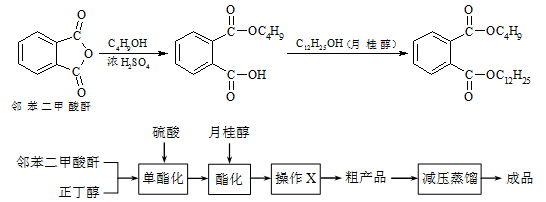
有关物质的物理性质见下表:
| 化合物 | 溶解性 | 熔点 | 沸点 |
| 邻苯二甲酸酐 | 微溶于冷水、乙醚,易溶于热苯、乙醇、乙酸 | 131.6℃ | 295℃ |
| 正丁醇 | 微溶于水,溶于乙醇、醚、多数有机溶剂 | -88.9℃ | 117.5℃ |
| 月桂醇 | 不溶于水,溶于醇、醚 | 24 | 259℃ |
| 邻苯二甲酸丁基月桂酯 | 不溶于水,溶于多数有机溶剂 | 不祥 | 202~210℃ |
某实验小组的同学模拟工业生产的工艺流程,用右图所示装置制取少量邻苯二甲酸丁基月桂酯,图中夹持和加热装置已略去。主要操作步骤如下:

①向三颈烧瓶内加入30 g 邻苯二甲酸酐、16 g 正丁醇以及少量浓硫酸。
②搅拌,升温至105 ℃,持续搅拌反应1小时。
③冷却至室温,加入40 g 月桂醇,升温至160 ℃,搅拌、保温至反应结束。
④冷却至室温,将反应混合物倒出。
⑤通过工艺流程中的操作X,得到粗产品。
请回答下列问题:
(1)仪器C的名称___________。冷凝管中冷水应从___________进。
(2)步骤③中判断反应已结束的方法是___________。
(3)步骤⑤中操作X可除去少量未反应的邻苯二甲酸酐及正丁醇,操作X包括___________。
(4)工艺流程中减压蒸馏的目的是___________。
(5)实验结果表明步骤②、③产率都比较高,原因是___________。
-
铁是人类较早使用的金属之一,铁及其化合物在现代社会各个领域仍有广泛的应用。
I.氧化物—Fe2O3:用工业FeCl3粗品(含Ca、Mn、Cu等杂质离子)制取高纯铁红,实验室常用萃取剂X(甲基异丁基甲酮)萃取法制取高纯铁红的主要实验步骤如下:

已知:HCl(浓) + FeCl3 HFeCl4 。试回答下列问题:
HFeCl4 。试回答下列问题:
(1)用萃取剂X萃取,该步骤中:
① Ca2+、Mn2+、Cu2+等杂质离子主要在__________(填“水”或“有机”)相。
② 若实验时共用萃取剂X 150mL,萃取率最高的方法是__________(填字母)。
a.一次性萃取,150mL b.分2次萃取,每次75mL c.分3次萃取,每次50mL
(2)用高纯水反萃取,萃取后水相中铁的存在形式是________________(写化学式);反萃取能发生的原因是___________________。
(3)所得草酸铁沉淀需用冰水洗涤,其目的一是洗去沉淀表面吸附的杂质离子,二是________________。
(4)测定产品中铁的含量需经酸溶、还原为Fe2+,然后在酸性条件下用标准K2Cr2O7溶液滴定,已知铬的还原产物为Cr3+,写出该滴定反应的离子方程式 ___________________。
II.含氧酸盐—铁酸铜(CuFe2O4)是很有前景的热化学分解水制氢的材料,CuFe2O4在制氢过程中可以循环使用。在热化学循环分解水制氢的过程中,铁酸铜(CuFe2O4)先要煅烧成氧缺位体(CuFe2O4-a),氧缺位值(a)越大,活性越高,制氢越容易。
(5)根据以上提示,写出氧缺位体与水常温下反应制氢的化学方程式____________。
(6)课外小组将铁酸铜样品在N2的气氛中充分煅烧,得氧缺位体的质量为原质量的96.6%,则氧缺位值(a)=__________。(结果保留小数点后2位)
-
铁是人类较早使用的金属之一,铁及其化合物在现代社会各个领域仍有广泛的应用。
I.氧化物—Fe2O3:用工业FeCl3粗品(含Ca、Mn、Cu等杂质离子)制取高纯铁红,实验室常用萃取剂X(甲基异丁基甲酮)萃取法制取高纯铁红的主要实验步骤如下:
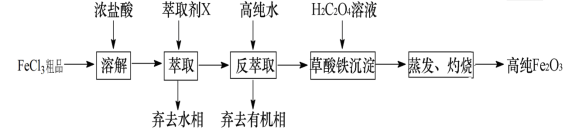
已知:HCl(浓) + FeCl3 HFeCl4 。试回答下列问题:
HFeCl4 。试回答下列问题:
(1)用萃取剂X萃取,该步骤中:
① Ca2+、Mn2+、Cu2+等杂质离子主要在__________(填“水”或“有机”)相。
② 若实验时共用萃取剂X 150mL,萃取率最高的方法是__________(填字母)。
a.一次性萃取,150mL b.分2次萃取,每次75mL c.分3次萃取,每次50mL
(2)用高纯水反萃取,萃取后水相中铁的存在形式是________________(写化学式);反萃取能发生的原因是___________________。
(3)所得草酸铁沉淀需用冰水洗涤,其目的一是洗去沉淀表面吸附的杂质离子,二是________________。
(4)测定产品中铁的含量需经酸溶、还原为Fe2+,然后在酸性条件下用标准K2Cr2O7溶液滴定,已知铬的还原产物为Cr3+,写出该滴定反应的离子方程式 ___________________。
II.含氧酸盐—铁酸铜(CuFe2O4)是很有前景的热化学分解水制氢的材料,CuFe2O4在制氢过程中可以循环使用。在热化学循环分解水制氢的过程中,铁酸铜(CuFe2O4)先要煅烧成氧缺位体(CuFe2O4-a),氧缺位值(a)越大,活性越高,制氢越容易。
(5)根据以上提示,写出氧缺位体与水常温下反应制氢的化学方程式____________。
(6)课外小组将铁酸铜样品在N2的气氛中充分煅烧,得氧缺位体的质量为原质量的96.6%,则氧缺位值(a)=__________。(结果保留小数点后2位)
 工业用途广泛,可用于生产油溶性酚醛树脂、稳定剂和香料等。实验室以苯酚、叔丁基氯[(CH3)3CCl]等为原料制备对叔丁基苯酚。实验步骤如下:反应物和产物的相关数据列表如下:
工业用途广泛,可用于生产油溶性酚醛树脂、稳定剂和香料等。实验室以苯酚、叔丁基氯[(CH3)3CCl]等为原料制备对叔丁基苯酚。实验步骤如下:反应物和产物的相关数据列表如下:
 可用于生产油溶性酚醛树脂等。实验室以苯酚、叔丁基氯[(CH3)3CCl]等为原料制备对叔丁基苯酚的实验步骤如下:
可用于生产油溶性酚醛树脂等。实验室以苯酚、叔丁基氯[(CH3)3CCl]等为原料制备对叔丁基苯酚的实验步骤如下:








