-
东汉成书的《神农本草经》有“石胆化铁为铜”(石胆是硫酸铜)的记载。这一方法开创了人类文明史上湿法冶金的先河。其中涉及的化学反应类型是
A. 化合反应 B. 分解反应 C. 置换反应 D. 复分解反应
高一化学单选题简单题查看答案及解析
-
(8分)中华民族在世界冶金史上曾谱写过辉煌的篇章,早在两千多年前的西汉时期就有“曾青得铁则化为铜”的记载,这种方法是现代湿法冶金的先驱.硫酸铜溶液遇到金属铁时,铁与硫酸铜发生置换反应能生成金属铜,该反应的化学方程式为Fe+CuSO4=Cu+FeSO4.
其中被还原的元素是________,被氧化的元素是________,氧化剂是________,还原剂是________,氧化产物是________,还原产物是________,每得到128克铜时,转移电子数目为________。
高一化学填空题简单题查看答案及解析
-
中华民族在世界冶金史上曾谱写过辉煌的篇章,早在两千多年前的西汉时期就有“曾青得铁则化为铜”的记载,这种方法是现代湿法冶金的先驱.硫酸铜溶液遇到金属铁时,铁与硫酸铜发生置换反应能生成金属铜,该反应的化学方程式为Fe+CuSO4=Cu+FeSO4.其中被还原的元素是________,被氧化的元素是________,氧化剂是________,还原剂是________,氧化产物是________,还原产物是________,每得到128克铜时,转移电子数目为________.
高一化学填空题中等难度题查看答案及解析
-
人们发现氧化铁硫杆菌能促使黄铁矿(FeS2)氧化成硫酸铁和硫酸,氧化铁硫杆菌能把矿物中的硫或硫化物氧化成硫酸,而硫酸和硫酸铁能将某些矿石中的金属元素转化成金属硫酸盐,从而开辟了“细菌冶金”的先河。氧化铁硫杆菌的活动过程如图所示,其中a过程发生的反应为4FeS2+15O2+2H2O
2Fe2(SO4)3+2H2SO4。则下列说法错误的是
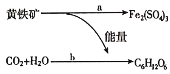
A.a过程中释放能量
B.细菌在反应a过程中起了催化剂的作用
C.b过程类似于植物的光合作用,细菌将能量储存在C6H12O6中
D.有些细菌可直接把含铅、汞等重金属的矿石溶解,得到重金属离子的溶液
高一化学单选题中等难度题查看答案及解析
-
磷酸亚铁锂(LiFePO4)电池是新能源汽车的动力电池之一。采用湿法冶金工艺回收废旧硫酸亚铁锂电池正极片中的金属,其流程如下:
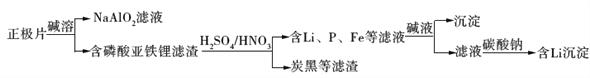
下列叙述错误的是
A. 合理处理废旧电池有利于保护环境和资源再利用
B. 从“正极片”中可回收的金属元素有Al、Fe、Li
C. “沉淀”反应的金属离子为Fe3+
D. 上述流程中可用硫酸钠代替碳酸钠
高一化学单选题中等难度题查看答案及解析
-
磷酸亚铁锂(LiFePO4)电池是新能源汽车的动力电池之一。采用湿法冶金工艺回收废旧硫酸亚铁锂电池正极片中的金属,其流程如下:
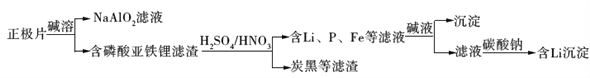
下列叙述错误的是
A. 合理处理废旧电池有利于保护环境和资源再利用
B. 从“正极片”中可回收的金属元素有Al、Fe、Li
C. “沉淀”反应的金属离子为Fe3+
D. 上述流程中可用硫酸钠代替碳酸钠
高一化学单选题中等难度题查看答案及解析
-
盐酸广泛应用在稀有金属的湿法冶金、漂染工业、金属加工、无机药品及有机药物的生产等领域中。HCl 极易溶于水,工业上用 HCl 气体溶于水的方法制取盐酸。
(1)用 12.0mol/L 浓盐酸配置 230mL 0.3mol/L 的稀盐酸,需要量取浓盐酸的体积为___mL;
(2)溶液稀释过程中需要的玻璃仪器有烧杯、玻璃棒、量筒、____________、___________;
(3)溶液稀释过程中有以下操作:
a.量取浓盐酸和一定体积的水,在烧杯中稀释
b.计算所需浓盐酸的体积
c.上下颠倒摇匀
d.加蒸馏水至刻度线 1-2cm 地方,改用胶头滴管加蒸馏水至凹液面与刻度线相切
e.将稀释液转移入容量瓶,洗涤烧杯和玻璃棒,并将洗涤液转移入容量瓶,振荡
以上正确的操作顺序为____________________________________________(填序号);
(4)实验过程中的以下操作会导致最终所配溶液浓度(填“偏大”、“偏小”或“不变”)
a.量取浓盐酸时俯视:______________________;
b.量取浓盐酸后,清洗了量筒并将洗涤液转移入容量瓶:______________________;
c.实验前,容量瓶中有少量残留蒸馏水:______________________;
(5)标准状况,1L 水中通入 aL HCl 气体,忽略盐酸溶液中 HCl 的挥发,得到的盐酸溶液密度为 b g/mL,物质的量浓度为 ______________________mol/L。
高一化学实验题中等难度题查看答案及解析
-
海水是镁资源的贮存库,从海水中提取MgCl2用于制取金属镁以被广泛的应用于工业生产,其中制取镁的方法是
A.热分解法 B.用CO还原 C.电解法 D.湿法冶金
高一化学单选题简单题查看答案及解析
-
盐酸广泛应用在稀有金属的湿法冶金、漂染工业、金属加工、无机药品及有机药物的生产等领域中。HCl极易溶于水,工业上用HCl气体溶于水的方法制取盐酸。
(1)用密度为1.2g/mL,质量分数为36.5%的浓盐酸配制250mL3mol/L的稀盐酸,需要用量筒量取浓盐酸的体积为__mL。
(2)溶液配制中需要的玻璃仪器有烧杯、玻璃棒、量筒、__、__。
(3)实验过程中,下列操作会导致最终所配溶液浓度偏高的是__。
A.量取浓盐酸时俯视刻度线
B.实验前,容量瓶中有少量残留蒸馏水
C.定容时俯视刻度线
D.转移时,未洗涤烧杯和玻璃棒
高一化学实验题中等难度题查看答案及解析
-
盐酸广泛应用在稀有金属的湿法冶金、漂染工业、金属加工、无机药品及有机药物的生产等领域中。HCl极易溶于水,工业上用HCl气体溶于水的方法制取盐酸。
(1)用密度为1.2g/mL,质量分数为36.5%的浓盐酸配制250mL3mol/L的稀盐酸,需要用量筒量取浓盐酸的体积为__mL。
(2)溶液配制中需要的玻璃仪器有烧杯、玻璃棒、量筒、__、__。
(3)实验过程中,下列操作会导致最终所配溶液浓度偏高的是__。
A.量取浓盐酸时俯视刻度线
B.实验前,容量瓶中有少量残留蒸馏水
C.定容时俯视刻度线
D.转移时,未洗涤烧杯和玻璃棒
高一化学实验题中等难度题查看答案及解析