-
(8分)增加反应物浓度可以加快化学反应速率。已知:反应Na2S2O3+H2SO4=Na2SO4+SO2+S↓+H2O出现浑浊的快慢与浓度有关。现有0.1mol/L的Na2S2O3溶液和0.1mol/L的H2SO4溶液和蒸馏水;实验用品有:烧杯、试管、量筒、胶头滴管、秒表等,请设计一个实验通过较明显的实验事实证明上述结论(说明实验操作、现象及结论)。
高二化学实验题简单题查看答案及解析
-
已知:Na2S2O3+H2SO4===Na2SO4+SO2↑+S↓+H2O,下列各组实验中,反应速率最快的是
组号
反应
温度/℃Na2S2O3
H2SO4
H2O
体积/ mL
浓度/ mol·L-1
体积/ mL
浓度/ mol·L-1
体积/ mL
A
10
5
0.2
5
0.1
10
B
10
5
0.1
5
0.1
10
C
30
5
0.1
5
0.1
10
D
30
5
0.2
5
0.2
10
A. A B. B C. C D. D
高二化学单选题中等难度题查看答案及解析
-
已知:Na2S2O3+H2SO4===Na2SO4+SO2↑+S↓+H2O,下列各组实验中,反应速率最快的是
组号
反应
温度/℃
Na2S2O3
H2SO4
H2O
体积/ mL
浓度/ mol·L-1
体积/ mL
浓度/ mol·L-1
体积/ mL
A
10
5
0.2
5
0.1
10
B
10
5
0.1
5
0.1
10
C
30
5
0.1
5
0.1
10
D
30
5
0.2
5
0.2
10
高二化学选择题中等难度题查看答案及解析
-
已知:Na2S2O3+H2SO4=Na2SO4+SO2↑+S↓+H2O,下列各组实验中,反应速率最快的是
组号 反应温
度/℃ Na2S2O3 H2SO4 H2O体积/mL
体积/mL 浓度/mol·L-1 体积/mL 浓度/mol·L-1
A 10 5 0.2 5 0.1 10
B 10 5 0.1 5 0.1 10
C 30 5 0.1 5 0.1 10
D 30 5 0.2 5 0.2 10
高二化学选择题中等难度题查看答案及解析
-
Ⅰ.已知:Na2S2O3+H2SO4==Na2SO4+SO2↑+S
↓+H2O。某同学探究影响硫代硫酸钠与稀硫酸反应速率的因素时,设计了如下系列实验:
实验序号
反应温度
Na2S2O3浓度[
稀硫酸
H2O
V/mL
c/(mol/L)
V/mL
c/(mol/L)
V/mL
①
20
10.0
0.10
10.0
0.50
0
②
40
V1
0.10
V2
0.50
V3
③
20
V4
0.10
4.0
0.50
V5
(1)该实验①、②可探究 对反应速率的影响,因此V1、V2和V3分别是 、 、 。
(2)实验①、③可探究 对反应速率的影响,因此V4、V5分别是 、 。
Ⅱ.二氧化氮在加热条件下能够分解成一氧化氮和氧气。该反应进行到45秒时,达到平衡(NO2浓度约为0.0125mol/L)。如图中的曲线表示二氧化氮分解反应在前25秒内的反应进程。
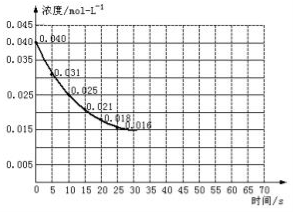
(3)前20秒内氧气的平均生成速率 mol/(L·s)
(4)在某温度下达到平衡时的平衡常数表达式是 。
(5)在某温度下达到平衡后,不改变其它条件,向该容器中再加入少量的NO2,平衡移动的方向是 ,NO2的平衡转化率 68.75%(填“>”、“<”或“=”),NO的体积百分含量 (填“增大”、“减小”或“不变”)。
(6)若在反应开始时加入催化剂(其他条件都不变),反应经过20秒达到平衡,请在图上用虚线画出加催化剂后反应0~70s的曲线。
高二化学填空题困难题查看答案及解析
-
已知反应Na2S2O3+H2SO4=Na2SO4+S↓+SO2+H2O,下列各组实验中最先出现浑浊的是
组号
温度
Na2S2O3
H2SO4
H2O
体积
浓度
体积
浓度
体积
A
0℃
10mL
0.1 mol/L
10mL
0.1 mol/L
0mL
B
10℃
5mL
0.1 mol/L
5mL
0.1 mol/L
10mL
C
30℃
5mL
0.1 mol/L
5mL
0.1 mol/L
10mL
D
30℃
5mL
0.2 mol/L
5mL
0.2 mol/L
10mL
高二化学选择题简单题查看答案及解析
-
已知:Na2S2O3+H2SO4= S↓+SO2↑+H2O+ Na2SO4,通过析出硫的快慢可以说明反应速率的大小,请判断下列几种情况下,最先看到硫析出的是
选项
温度
Na2S2O3溶液的体积和物质的量浓度
H2SO4的体积和物质的量浓度
A
20℃
15mL0.1mol·L-1
15mL0.1mol·L-1
B
20℃
10mL0.2mol·L-1
10mL0.2mol·L-1
C
50℃
50mL0.1mol·L-1
50mL0.1mol·L-1
D
50℃
5mL0.5mol·L-1
5mL0.5mol·L-1
A. A B. B C. C D. D
高二化学选择题中等难度题查看答案及解析
-
硫代硫酸钠溶液与稀硫酸反应的化学方程式为:Na2S2O3+H2SO4=Na2SO4+SO2↑+S↓+H2O,可以通过出现浑浊的快慢来判断反应的快慢程度,下列各组实验中最先出现浑浊的是( )
实验
反应温度/℃
Na2S2O3溶液
稀H2SO4
V/mL
c/(mol·L-1)
V/mL
c/(mol·L-1)
A
25
5
0.1
20
0.1
B
25
5
0.2
10
0.2
C
35
5
0.1
20
0.1
D
35
5
0.2
10
0.2
A.A B.B C.C D.D
高二化学单选题中等难度题查看答案及解析
-
硫代硫酸钠溶液与稀硫酸反应的化学方程式为:Na2S2O3+H2SO4=Na2SO4+SO2↑+S↓+H2O,可以通过出现浑浊的快慢来判断反应的快慢程度,下列各组实验中最先出现浑浊的是 ( )
实验 反应温度/℃[ Na2S2O3溶液 稀H2SO4
V/mL c/(mol·L-1) V/mL c/(mol·L-1)
A 25 5 0.1 10 0.1
B 25 5 0.2 5 0.2
C 35 5 0.1 10 0.1
D 35 5 0.2 5 0.2
高二化学选择题中等难度题查看答案及解析
-
硫代硫酸钠溶液与稀硫酸反应的化学方程式为:Na2S2O3+H2SO4=Na2SO4+SO2↑+S↓+H2O,可以通过出现浑浊的快慢来判断反应的快慢程度,下列各组实验中最先出现浑浊的是( )
实验
反应温度/℃
Na2S2O3溶液
稀H2SO4
V/mL
c/(mol·L-1)
V/mL
c/(mol·L-1)
A
25
5
0.1
20
0.1
B
25
5
0.2
10
0.2
C
35
5
0.1
20
0.1
D
35
5
0.2
10
0.2
A. A B. B C. C D. D
高二化学选择题中等难度题查看答案及解析