-
X、Y、Z、W四种短周期元素在周期表中的位置关系如右图所示,其中Z元素原子的最外层电子数是其电子层数的2倍。
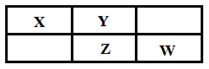
请回答下列问题:
(1)元素Z位于周期表中第_______周期,________族;
(2)这些元素的最高价氧化物对应的水化物中,水溶液酸性最强的是_______(写化学式);
(3)Y和Z组成的化合物的化学式为_______;
(4)W的单质和过量的X的氢化物可发生氧化还原反应,所得两种产物的电子式分别为____________、___________;
(5)W的最高价氧化物对应的水化物的浓溶液不稳定,受热可分解,产物之一是黄绿色气体,且当有28 mol 电子转移时,共产生9 mol 气体,写出该反应的化学方程式___________。
-
(10分)W、X、Y、Z四种短周期元素在元素周期表中的位置如右图所示,其中Z位于ⅦA族。

请回答下列问题。
(1)W的原子结构示意图为。能说明Z的非金属性比X的非金属性强的事实是________(举一例)。
(2)W、Y和氢3种元素所形成的一种化合物,其75%(体积分数)的溶液常用于医疗消毒,该化合物的结构简式为。用化学方程式表示该化合物在中学实验室的一种用途________。
(3)电解NaZ水溶液时,阴极的电极反应式为。工业上,以上述反应的阳极产物和Ca(OH)2为原料,制备漂白粉反应的化学方程式为________。
(4)已知:298K时,金属钠与Y2气体反应,生成1 mol Na2Y固体时,放出热量414 kJ;生成1 mol Na2Y2固体时,放出热量511 kJ。由Na2Y固体与Y2气体反应生成Na2Y2固体的热化学方程式为。
-
(10分)W、X、Y、Z四种短周期元素在元素周期表中的位置如右图所示,其中Z位于ⅦA族。请回答下列问题。

(1)W的原子结构示意图为________。能说明Z的非金属性比X的非金属性强的事实是________(举一例)。
(2)W、Y和氢3种元素所形成的一种化合物,其75%(体积分数)的溶液常用于医疗消毒,该化合物的结构简式为。用化学方程式表示该化合物在中学实验室的一种用途________。
(3)电解NaZ水溶液时,阴极的电极反应式为________。工业上,以上述反应的阳极产物和Ca(OH)2为原料,制备漂白粉反应的化学方程式为________。
(4)已知:298K时,金属钠与Y2气体反应,生成1 mol Na2Y固体时,放出热量414 kJ;生成1 mol Na2Y2固体时,放出热量511 kJ。由Na2Y固体与Y2气体反应生成Na2Y2固体的热化学方程式为________。
-
X、W、Y、Z均为短周期主族元素,原子序数依次增大,Y原子的最外层电子数是X的2倍,X、W、Y在周期表中的相对位置如右图所示。
回答下列问题:
(1)Y元素在元素周期表中的位置是 。
(2)列举一个事实证明Y、Z两种元素的非金属性强弱 ( 用化学方程式表示 ): 。
(3)W的最高价氧化物与强碱溶液反应的离子方程式为 。
(4)X的最高价氧化物对应水化物( H3XO3 ) 是一元弱酸,在横线上填写合适的结构简式:X (OH)3 + H2O  H+ +
H+ +
(5)已知25℃:
| Y的氢化物 | 一元酸HA |
| Ka1=9.1×10-8,Ka2=1.1×10-12 | Ka=1.1×10-10 |
写出Y的氢化物与钾盐KA溶液 ( A-表示酸根 ) 反应的化学方程式: 。
(6)在烧碱溶液中,以W单质和NiO( OH ) ( 氢氧化氧镍 ) 为两极组成一种新型电池,放电时NiO( OH )转化为Ni(OH)2,写出其正极的电极反应式: 。
-
短周期元素Q、R、T、W在元素周期表中的位置如右图所示,期中T所处的周期序数与主族序数相等,请回答下列问题:
 (1)T的原子结构示意图为_______.
(1)T的原子结构示意图为_______.
(2)元素的非金属性为(原子的得电子能力):Q______W(填“强于”或“弱于”)。
 (3) W的单质与其最高价氧化物的水化物浓溶液共热能发生反应,生成两种物质,其中一种是气体,反应的化学方程式为_____.
(3) W的单质与其最高价氧化物的水化物浓溶液共热能发生反应,生成两种物质,其中一种是气体,反应的化学方程式为_____.
(4)原子序数比R多1的元素是一种氢化物能分解为它的另一种氢化物,此分解反应的化学方程式是__________.
 (5)R有多种氧化物,其中甲的相对分子质量最小。在一定条件下,2L的甲气体与0.5L的氯气相混合,若该混合气体被足量的NaOH溶液完全吸收后没有气体残留,所生成的R的含氧酸盐的化学式是__________.
(5)R有多种氧化物,其中甲的相对分子质量最小。在一定条件下,2L的甲气体与0.5L的氯气相混合,若该混合气体被足量的NaOH溶液完全吸收后没有气体残留,所生成的R的含氧酸盐的化学式是__________.
(6)在298K下,Q、T的单质各1mol完全燃烧,分别放出热量aKJ和bKJ。又知一定条件下,T的单质能将Q从它的最高价氧化物中置换出来,若此置换反应生成3molQ的单质,则该反应在298K下的 =________(注:题中所设单质均为最稳定单质)
=________(注:题中所设单质均为最稳定单质)
-
X、Y、Z、W、M是五种原子序数依次增大的短周期元素,其中X、Y、M在周期表中的位置如右图所示,又知W的最外层电子数是内层电子数的3倍,试回答下列问题:
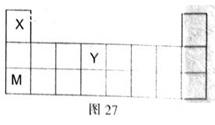
(1)Y在周期中的位置是:________,M的最高价氧化物的水化物电子式为:________。
(2)由这五种元素中的两种元素形成的既含极性共价键又含非极性共价键的化合物有很多种,请写出其中两种四原子分子的结构式:________、________。
(3)由这五种元素形成的单质或化合物中,能与水发生化学反应的有多种,请任写出其中一种与水反应后生成一种单质和一种化合物的化学反应方程式________。
(4)在微电子工业中,用Z的气态氢化物甲的水溶液作刻蚀剂H2O2的清除剂,所发生反应的产物不污染环境。写出该反应的化学方程式:________。
(5)在合成甲的反应过程中,反应速率与时间的图像如图所示,则在t1-t6时间内的甲的体积分数最小的时刻是________,t3时刻改变的外界条件是________,合成甲的反应是________反应(填“吸热”或“放热”)。
-
(8分)四种短周期元素在周期表中的相对位置如下所示,其中Z元素原子核外电子总数是其最外层电子数的3倍。

请回答下列问题:
(1)元素Z位于周期表中的位置________;
(2)这些元素的氢化物中,水溶液碱性最强的是_______________(写化学式);
(3)XW2的电子式为_______________;
(4)Y的最高价氧化物的化学式为________________;
(5)W和Y形成的一种二元化合物具有色温效应,请相对分子质量在170~190之间,且W的质量分数约为70%。该化合物的化学式为_________________。
-
(10分)四种短周期元素在周期表中的相对位置如下所示,其中Z元素原子核外电子总数是其最外层电子数的3倍。请回答下列问题:

(1)元素Z位于周期表中第_______周期,_______ 族;
(2)这些元素的氢化物中,水溶液碱性最强的是_______________(写化学式);
(3)XW2的电子式为_______________
(4)Y的最高价氧化物的水化物与其氢化物反应的离子方程式 。
-
镁、钡是位于同一主族的活泼的金属元素。
回答下列问题:
(1)镁在元素周期表中的位置是:______________;钡位于周期表第六周期,钡原子最外层电子的电子排布式是:________。
(2)铝也是一种活泼金属,铝的金属性比钡的_____(填“强”或“弱”)。工业上可用如下方法制取钡:2Al+4BaO 3Ba↑+BaO·Al2O3,该法制钡的主要原因是______(选填选项)
3Ba↑+BaO·Al2O3,该法制钡的主要原因是______(选填选项)
a.高温时Al的活泼性大于Ba b.高温时BaO·Al2O3比Al2O3稳定
c.Ba的沸点比Al的低 d.高温有利于BaO分解
两个烧杯分别盛有VmL、c mol/L的Ba(OH)2溶液,分别向其中滴入c mol/L的H2SO4 和NaHSO4溶液,两烧杯中溶液导电能力随滴入溶液体积的变化分别如下图中①、②所示。
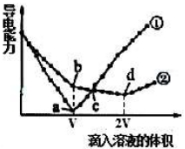
(3)写出Ba(OH)2溶液与H2SO4恰好反应的离子方程式:___________。
(4)写出b点溶液中大量存在的阴离子的电子式:_________。
(5)a、b、c、d点溶液呈中性的是____________________。
-
四种短周期元素在周期表中的相对位置如图所示,其中Z元素原子核外电子总数是其最外层电子数的3倍.
请回答下列问题:
(1)元素Z位于周期表中第______周期,______族;
(2)这些元素的氢化物中,水溶液碱性最强的是______(写化学式);
(3)XW2的电子式为______;
(4)Y的最高价氧化物的化学式为______;
(5)W和Y形成的一种二元化合物具有色温效应,其相对分子质量在170~190之间,且W的质量分数约为70%.该化合物的化学式为______.




