-
(8分)某工厂用FeC13溶液腐蚀镀有铜的绝缘板生产印刷电路。
(1)用离子方程式表示其化学原理________。
某实验小组的同学对该厂生产印刷电路后所得的废液进行了分析:取50.00 mL。废液,向其中加入0.64 g金属铜,金属铜全部溶解;又取50.00 mL废液,向其中加入足量AgNO3溶液,析出沉淀43.05 g。请回答以下问题:
(2)该厂生产后废液中所含金属阳离子有
(3)该厂原来使用的FeCl3溶液的物质的量浓度为________。(设反应前后溶液的体积无变化);
(4)若向500.00 mL废液中加入足量的稀硝酸,在
标准状况下生成NO气体4.48 L,则原废液中各
金属阳离子的物质的量浓度之比为________。(离
子与比值一一对应)。
高三化学计算题中等难度题查看答案及解析
-
某工厂用 FeCl3 溶液腐蚀镀有铜的绝缘板生产印刷电路。课外活动小组为确认生产后的废液的组成,进行如下实验:(1)取10mL 废液加入足量的 AgNO3 溶液,生成沉淀 8.61g。(2)另取 10mL废液放入铜片充分反应,铜片质量减少了0.256g。下列关于原废液组成的判断错误的是
A. 一定含有 Fe 2+、 Fe 3+、 Cu2+、 Clˉ B. c(Fe2+):c(Cu2+) = 2:1
C. c(Clˉ) = 6mol / L, c(Fe 2+) = 1.2mol / L D. c (Fe2+):c(Fe 3+) = 3:1
高三化学选择题困难题查看答案及解析
-
某工厂用FeCl3溶液腐蚀镀有铜的绝缘板生产印刷电路(已知发生的反应为:2FeCl3
Cu → 2FeCl2
CuCl2)。课外活动小组为确认生产后的废液的组成,进行如下实验:(1)取10mL废液加入足量的AgNO3溶液,生成沉淀 8.61g。(2)另取10mL废液放入铜片充分反应,铜片质量减少了0.256g。下列关于原废液及其形成的判断正确的是
A.c(
)︰c(
)
B.c(
)︰c(
)
C.c(
)
6mol/L,c(
)
0.6mol/L
D.该绝缘板腐蚀后质量减少0.384g
高三化学选择题困难题查看答案及解析
-
下列反应的离子方程式正确的是
A.
B.用FeC13溶液腐蚀电路板:
C.
溶液中通入过量
D.用食醋除去水瓶中的水垢:
高三化学选择题中等难度题查看答案及解析
-
下列反应的离子方程式正确的是
A.
B.用FeC13溶液腐蚀电路板:
C.向
溶液中通入过量
D. 用食醋除去水瓶中的水垢:
高三化学选择题中等难度题查看答案及解析
-
下列反应的离子方程式正确的是
A.
B.用FeC13溶液腐蚀电路板:
C.向
溶液中通入过量
D. 用食醋除去水瓶中的水垢:
高三化学选择题中等难度题查看答案及解析
-
铁及其化合物在日常生活中有广泛的应用,回答下列问题。
(1)FeC13具有净水作用,但腐蚀设备,FeC13溶液腐蚀钢铁设备,除H+作用外,另一主要原因是(用离子方程式表示)_________。
(2)为节约成本,工业上用NaC1O、氧化酸性FeCl2废液得到FeC13,完成NaClO3氧化FeCl2的离子方程式:___________。
口ClO3-+口Fe2++口_____=口Cl-+口Fe3++口_______。
(3)高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝、助凝、杀菌、除臭为一体的新型高效多功能绿色水处理剂,具有良好的应用前景。其生产工艺如图1所示:

①实验室模拟工业流程中过滤操作用到的主要玻璃仪器有______。
②在“反应液I”中加KOH固体的目的有两个,a是与“反应液I”中过量的Cl2继续反应,生成更多的KClO, b是_____。
③用K2FeO4给水消毒、杀菌时得到的Fe3+可以净水,Fe3+净水原因是______(用离子方程式表示)。
(4)从环境保护的角度看,制备K2FeO4较好的方法未电解法,其装置如图2所示。

电解过程中阳极电极反应式为________。
(5)钢铁腐蚀造成很大损失,有资料显示,全世界每年由于腐蚀二造成的报废的钢铁高达总产量的三分之一。防止钢铁腐蚀有很多措施,用图3装置防止钢铁腐蚀(烧杯中均为食盐水), X 极的电极材料应是______(填字母)。
A.锌 B.铜 C.银 D.石墨
高三化学填空题中等难度题查看答案及解析
-
(14分)金属单质及其化合物在工农业生产中应用广泛。
(1)用FeC13溶液腐蚀印刷电路板上的铜,向所得溶液中加入铁粉。对加入铁粉充分反应后的溶液分析合理的是_______。
a.若无固体剩余,则溶液中可能有Fe3+
b.若有固体存在,则溶液中一定有Cu2+和Fe2+
c.若溶液中有Cu2+,则可能有固体存在,且该固体中一定没有铁粉
d.若溶液中有Fe2+,则一定有固体存在
(2)Cu2O是一种半导体材料,制取Cu2O的电解池如图,则石墨电极接电源的_______(填“正”或“负”)极,电解池工作时,Cu电极的电极反应式为______;电解后溶液pH______(填“变大”、“变小”或“不变”)

(3)查阅资料可知:Cu2O为红色碱性氧化物,在酸性溶液中可发生反应:Cu2O+2H+=Cu+Cu2++H2O。请设计简单实验来验证某铜粉样品中是否有氧化亚铜:_____。
高三化学填空题困难题查看答案及解析
-
印刷电路的废腐蚀液含有大量CuC12、FeC12和FeC13,任意排放将导致环境污染及资源的浪费.可从该废液中回收铜,并将铁的化合物全部转化为FeCl3溶液,作为腐蚀液原料循环使用.测得某废腐蚀液中含CuCl2 1.5mol/L、FeCl2 3.0mol/L、FeCl3 1.0mol/L、HCl 3.0mol/L.取废腐蚀液200mL按如下流程在实验室进行实验:
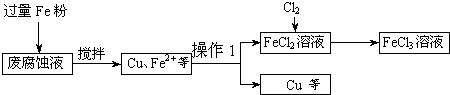
回答下列问题:
(1)上述方法获得的铜粉中含有杂质,除杂质所需试剂是______(填化学式).
(2)实验室可用固体KClO3与浓HCl反应制备Cl2,此反应中Cl2既是氧化产物,又是还原产物.反应的化学方程式为______ KCl+3Cl2↑+3H2O高三化学解答题中等难度题查看答案及解析
-
印刷电路的废腐蚀液含有大量CuC12、FeC12和FeC13,任意排放将导致环境污染及资源的浪费.可从该废液中回收铜,并将铁的化合物全部转化为FeCl3溶液,作为腐蚀液原料循环使用.测得某废腐蚀液中含CuCl2 1.5mol/L、FeCl2 3.0mol/L、FeCl3 1.0mol/L、HCl 3.0mol/L.取废腐蚀液200mL按如下流程在实验室进行实验:
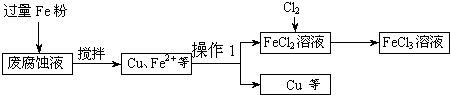
回答下列问题:
(1)上述方法获得的铜粉中含有杂质,除杂质所需试剂是______(填化学式).
(2)实验室可用固体KClO3与浓HCl反应制备Cl2,此反应中Cl2既是氧化产物,又是还原产物.反应的化学方程式为______ KCl+3Cl2↑+3H2O高三化学解答题中等难度题查看答案及解析