-
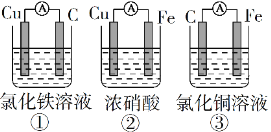
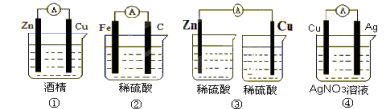
(Ⅰ)下列装置能组成原电池的是_____________ (填序号)

(Ⅱ)如上图④所示,若是原电池,请回答下列问题(若不是原电池,则不用回答)。
(1)负极材料是_______________________
(2)正极的电极反应式为________________________
(3)电池工作时总反应的离子方程式是____________________________
(4)导线中电子的流向________________________________
(5)阳离子的移动方向___________________________________
(6)该装置将________能转化为________能。
-
(9分)(Ⅰ)下列装置能组成原电池的是_____________ (填序号)

(Ⅱ)如上图④所示,若是原电池,请回答下列问题(若不是,则不用回答)。
(1)正极材料是_______________________
(2)负极的电极反应式为________________________
(3)电池工作时总反应的离子方程式是____________________________
(4)阴离子的移动方向___________________________________
(5)导线中电子的流向________________________________
-
电池在我们的生活中有着重要的应用,请回答下列问题:
(1)为了验证Fe2+与Cu2+氧化性强弱,下列装置能达到实验目的的是______(填序号),写出正极的电极反应式_______。若构建原电池时两个电极的质量相等,当导线中通过0.05 mol电子时,两个电极的质量差为________。
(2)将CH4设计成燃料电池,其利用率更高,装置如图所示(A、B为多孔碳棒)。
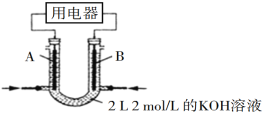
实验测得OH−定问移向B 电极,则_____(填“A”或“B”)处电极入口通甲烷,其电极反应式为___________。当消耗甲院的体积为33.6 L(标准状况下)时,假设电池的能量转化率为80%,则导线中转移电子的物质的量为________。
-
为了探究原电池的工作原理,某化学学习小组设计了一组实验,其装置如下图:
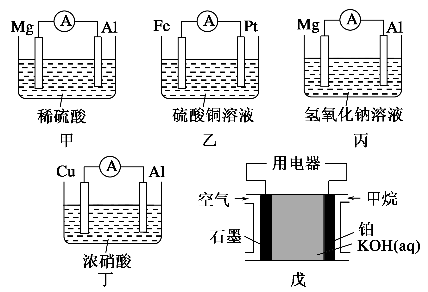
回答下列问题:
(1)根据原电池原理填写下表:
| 装置序号 | 正极 | 负极反应式 | 阳离子移动方向 |
| 甲 | | | |
| 乙 | | | |
| 丙 | | | |
| 丁 | | | |
| 戊 | | | |
(2)电极类型除与电极材料的性质有关外,还与________有关。
(3)根据上述电池分析,负极材料是否一定参加电极反应?_____
(填“是”“否”或“不一定”),请举例说明:__________________________________________。
(4)指出下列电池的放电过程中,电解质溶液酸碱性的变化:甲_______,丙_______,戊_______。(填酸性或碱性增强或减弱)
-
(1)下列装置能组成原电池的是______.(填序号)

(2)对于锌-铜-稀硫酸组成的原电池装置,当导线中有1mol电子通过时,锌片溶解了______g,铜片上析出______升 H2(标准状况下).电池总反应的化学方程式为______.
(3)如右图所示装置,若烧杯中溶液为氢氧化钠溶液,则负极为______,总反应方程为______.该装置将______能转化为______能.
(4)利用反应:Fe+2Fe3+=3Fe2+设计一个化学电池(电极材料和电解液自选),画出实验装置图,注明电解质溶液名称和正负极材料.

-
某课外小组分别用如图所示装置对原电池和电解原理进行实验探究.请回答:
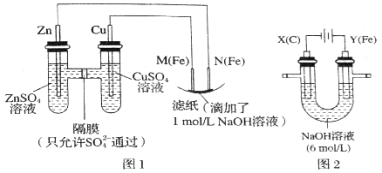
Ⅰ.用图 1 所示装置进行第一组实验.
(1)在保证电极反应不变的情况下,不能替代 Cu 作电极的是________(填字母序号).
A.石墨 B.铝 C.铂 D.银
(2)N 极发生反应的电极反应式为__________________________________.
Ⅱ.用图 2 所示装置进行第二组实验.实验过程中,观察到与第一组实验不同的现象:两极均有气体产生,Y极区溶液逐渐变成紫红色;停止实验,铁电极明显变细,电解液仍然澄清. 查阅资料得知,高铁酸根离子(FeO42﹣)在溶液中呈紫红色.
(3)电解过程中,X 极区溶液的 pH________(填“增大”“减小”或“不变”).
(4)电解过程中,Y 极发生的电极反应之一为 Fe﹣6e﹣+8OH﹣═FeO42﹣+4H2O 若在 X 极收集到672mL 气体,在 Y 极收集到 168mL 气体(均已折算为标准状况时气体体积),则 Y 电极(铁 电极)质量减少________g.
(5)在碱性锌电池中,用高铁酸钾作为正极材料,电池反应为2K2FeO4+3Zn=Fe2O3+ZnO+2K2ZnO2.该电池负极发生的反应的电极反应式为________.
-
理论上讲,任何自发的氧化还原反应都可以设计成原电池。请利用反应“Cu+2Ag+=2Ag+Cu2+”设计一个化学电池(正极材料用碳棒),回答下列问题:
(1)画出原电池装置图_______,该电池的负极发生_______反应(填“氧化”或“还原”),电解质溶液是_______;
(2)放电时银离子向__________(填“正极”或“负极”),正极上出现的现象是________。
(3)当反应进行一段时间后取出电极材料,测得某一电极增重了5.4g,则该原电池反应共转移了电子数目是___________。
-
(I)下列装置能组成原电池的是 (填序号)
(II)将CH4设计成燃料电池,装置如图所示(A、B为多孔碳棒)
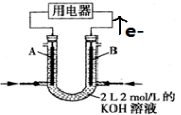
① (填A或B)处电极入口通甲烷,其电极反应式为 ;
②当消耗甲烷的体积为11.2 L(标准状况下)时,则导线中转移电子数为 ,消耗KOH的物质的量为 。
-
利用铜棒、锌片和200ml稀硫酸组成原电池,将化学能转化为电能,当铜棒上共产生3.36L(标准状况)气体时,硫酸恰好全部被消耗。请回答下列问题:
(1)该原电池的正极反应式为:________
(2)计算原稀硫酸的物质的量浓度。
(3)若将铜棒换成铁片,仍按题给方式组合起来,能否组成原电池呢?________(填“能”或“不能”) 若能组成原电池,此原电池的负极反应式是________
-
(题文)(1)在下图的8个装置中,属于原电池的是____________。

(2)依据氧化还原反应:2Ag+(aq)+Zn(s)===Zn2+(aq)+2Ag(s)设计的原电池如图所示。请回答下列问题:

①电极X的材料是______;电解质溶液Y是________;
②银电极为电池的______极,发生的电极反应为__________________;
(3)航天飞机常采用燃料电池作为电能来源,燃料电池一般指采用H2、CH4、CO、C2H5OH等可燃物质与O2一起构成的电池装置,它可直接将化学能转化为电能。如图是甲烷燃料电池原理示意图,回答下列问题:

①电池的负极是____(填“a”或“b”),该极的电极反应是____________。
②消耗标准状况下5.6 L O2时,有____mol电子发生转移。
③开始放电时,正极附近溶液的pH__________(填“增大”“减小”或“不变”)
④以铜为电极,用此电池作电源,电解以下溶液,开始阶段发生反应Cu+2H2O===Cu(OH)2+H2↑的有______________。
A.稀H2SO4 B.NaOH溶液 C.Na2SO4溶液
D.CuSO4溶液 E.NaCl溶液











