-
碱性硼化钒(VB2)—空气电池工作时反应为:4VB2 + 11O2 = 4B2O3 + 2V2O5。用该电池为电源,选用惰性电极电解硫酸铜溶液,实验装置如图所示。当外电路中通过0.04mol电子时,B装置内共收集到0.448L气体(标准状况),则下列说法正确的是
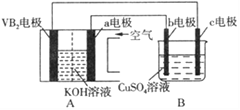
A. VB2电极发生的电极反应为:2VB2 + 11H2O - 22e- = V2O5 + 2B2O3 + 22H+
B. 外电路中电子由c电极流向VB2电极
C. 电解过程中,c电极表面先有红色物质析出,b电极有气泡产生
D. 若B装置内的液体体积为200 mL,则CuSO4溶液的物质的量浓度为0.1mol/L
-
碱性硼化钒(VB2)—空气电池工作时反应为:4VB2 + 11O2 = 4B2O3 + 2V2O5。用该电池为电源,选用惰性电极电解硫酸铜溶液,实验装置如图所示。当外电路中通过0.04mol电子时,B装置内共收集到0.448L气体(标准状况),则下列说法正确的是
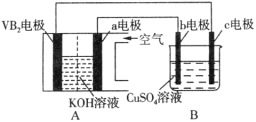
A.VB2电极发生的电极反应为:2VB2 + 11H2O - 22e- = V2O5 + 2B2O3 + 22H+
B.外电路中电子由c电极流向VB2电极
C.电解过程中,c电极表面先有红色物质析出,后有气泡产生
D.若B装置内的液体体积为100 mL,则CuSO4溶液的物质的量浓度为0.05 mol/L
-
硼化钒(VB2)—空气电池是目前储电能力最高的电池,电池示意图:
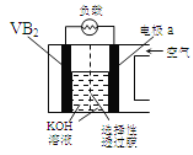
该电池工作时反应为:4VB2 + 11O2 = 4B2O3 + 2V2O5 。下列说法正确的是
A.VB2极发生的电极反应为:2VB2 + 22OH−-22e−=V2O5 + 2B2O3 + 11H2O
B.电极a为电池负极
C.电流由VB2极经负载流向电极a
D.图中选择性透过膜允许阳离子选择性透过
-
可用于电动汽车的铝—空气燃料电池,若以氢氧化钠溶液为电解液,铝合金为负极,空气电极为正极。下列说法正确的是( )
A.正极反应式为
B.负极反应式为
C.电池在工作过程中电解液的碱性保持不变
D.电池工作时,电子通过外电路从正极流向负极
-
肼(N2H4)﹣空气燃料电池是一种环保型碱性燃料电池,电解质溶液是20%~30%的KOH溶液。电池总反应为:N2H4+O2=N2↑+2H2O.下列关于该燃料电池工作时的说法正确的是( )
A. 负极的电极反应式是:N2H4+4OH﹣+4e﹣=4H2O+N2↑
B. 正极的电极反应式是:O2+4H- --4e﹣=2H2O
C. 溶液中阴离子向负极移动
D. 溶液中C﹙OH﹣﹚保持不变
-
金属(M)-空气电池(如图)具有原料易得、能量密度高等优点,有望成为新能源汽车和移动设备的电源。该类电池在碱性环境下的总反应方程式为:4M+nO2+2nH2O=4M(OH)n。已知:电池的“理论比能量”指单位质量电极材料理论上释放出的最大电能。下列说法不正确的是( )
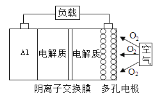
A. 采用多孔电极的目的是提高电极与电解质溶液的接触面积,并有利于氧气扩散至电极表面
B. 比较Mg、Al、Zn三种金属-空气电池,Al-空气电池的理论比能量最高
C. M-空气电池放电过程的正极反应式:4Mn++nO2+2nH2O+4ne–=4M(OH)n
D. 消耗氧气22.4 L(标准状况),有4 molOH-从右往左通过阴离子交换膜
-
下图是某碱性氢氧燃料电池的工作原理示意图,下列说法错误的是

A. 气体2 是氧气
B. C1 极为电源负极
C. 负极上的电极反应式为H2-2e- ==2H+
D. 装置中能量转化形式有:化学能→电能、电能→光能
-
镁燃料电池作为一种高能化学电源,具有良好的应用前景。下图是镁--空气燃料电池工作原理示意图。下列有关该电池的说法不正确的是( )
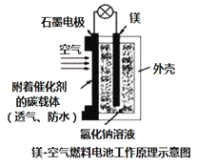
A.该电池Mg作负极,发生氧化反应
B.该电池的正极反应式为:
C.电池工作时,电子通过导线由Mg电极流向C电极
D.当电路中通过0.2mol电子时,消耗的 体积为1.12L
体积为1.12L
-
锌-空气电池(原理如图)适宜用作城市电动车的动力电源。该电池放电时Zn转化为ZnO转化为ZnO。该电池工作时下列说法正确的是
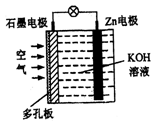
A. 氧气在石墨电极上发生氧化反应
B. 该电池的负极反应为Zn+H2O-2e-=ZnO+2H+
C. 电子由锌电极经电解质溶液流向石墨电极
D. 电池工作时锌电极不断被消耗
-
锌—空气电池(原理如图)适宜用作城市电动车的动力电源。该电池放电时Zn转化为ZnO。该电池工作时,下列说法正确的是
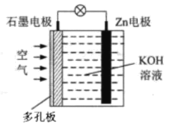
A.Zn电极是该电池的正极
B.Zn电极的电极反应:Zn+H2O-2e‾=ZnO+2H+
C.OH‾向石墨电极移动
D.标准状况下,当消耗11.2LO2时,电路中流过2mol电子







