-
高炉炼铁中发生的基本反应之一如下:
FeO(s)+CO(g) Fe(s)+CO2(g) ΔH>0,其平衡常数表达式为K= ,又知1 100 ℃时,K=0.28。
Fe(s)+CO2(g) ΔH>0,其平衡常数表达式为K= ,又知1 100 ℃时,K=0.28。
(1)温度升高,化学平衡移动后达到新的平衡,平衡常数 。(填“变大”“变小”或“不变”)
(2)1 100 ℃时测得高炉中c(CO2)=0.013 mol·L-1,c(CO)=0.05 mol·L-1,在这种情况下,该反应是否处于化学平衡状态: (填“是”或“否”),此时,化学反应速率是v(正) v(逆)(填“大于”“小于”或“等于”),其原因 。
-
高炉炼铁中发生的基本反应之一为:FeO(s)+CO(g) Fe(s)+CO2(g)ΔH>0,已知1 373 K时K=0.263。
Fe(s)+CO2(g)ΔH>0,已知1 373 K时K=0.263。
(1)该反应的平衡常数表达式为 。
(2)温度升高,化学平衡移动后,平衡常数K值 (填“增大”、“减小”或“不变”)。
(3)1 373 K时测得高炉中c(CO2)=0.025 mol/L,c(CO)=0.1 mol/L,在这种情况下,该反应是否处于化学平衡状态 (填“是”或“否”)。此时,化学反应速率v(正) v(逆)(填“大于”、“等于”或“小于”),其原因是 。
-
高炉炼铁过程中发生的主要反应为1/3Fe2O3(s) + CO(g)  2/3Fe(s) + CO2(g)
2/3Fe(s) + CO2(g)
已知该反应在不同温度下的平衡常数如下:

请回答下列问题:
(1)该反应的平衡常数表达式K=_____________,△H________0(填“>”、“<”或“=”);
(2)在一个容积为10L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各1.0 mol,反应经过l0 min达到平衡。求该时间范围内反应的平均反应速率υ(CO2)= _________ 、CO的平衡转化率= _____________:
(3)欲提高(2)中CO的平衡转化率,可采取的措施是_____________。
A.减少Fe的量
B.增加Fe203的量
C.移出部分CO2
D.提高反应温度
E.减小容器的容积
F.加入合适的催化剂
-
高炉炼铁中发生的反应为:FeO(s)+CO(g) Fe(s)+CO2(g) △H>0。已知t℃时,平衡常数K=0.25。
Fe(s)+CO2(g) △H>0。已知t℃时,平衡常数K=0.25。
(1)温度升高,化学平衡移动后达到新的平衡,平衡常数K_____(填“增大”、“减小”或“不变”,下同),高炉内CO2和CO的体积比____
(2)t℃时测得高炉中c(CO2)=0.020 mol·Lˉ1,c(CO)=0.1 mol·Lˉ1,在这种情况下,该反应是否处于化学平衡状态_______(填“是”或“否”),此时,化学反应速率是υ(正)_____υ(逆)(填“大于”、“小于”或“等于”),其原因是________________
(3)若在1L密闭容器中加入0.02mol FeO(s),并通入x mol CO,t℃时反应达到平衡。此时FeO(s)的转化率为50%,则x=_______________。
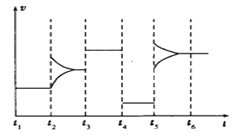
(4)如图为t2时刻后改变条件平衡体系中化学反应速率随时间变化的情况,且四个阶段各改变一种条件并且改变的条件均不同。已知,t3~t4阶段为使用催化剂,则t4时刻改变的条件为_____________,t5时刻改变的条件为____________
-
(12分)高炉炼铁中发生的基本反应如下:FeO(s)+CO(g)s Fe(s)+CO2(g) △H>0。
Fe(s)+CO2(g) △H>0。
(1)下列可以作为判断该反应已经达到化学平衡状态依据的是________。
a.高炉内压强不变
b.CO2的生成速率和CO的生成速率相等
c.混合气体中CO2的浓度不变
d.c(CO2)=c(CO)
(2)此反应的平衡常数表达式为K=________。
(3)温度升高平衡常数K值________(填“增大”“减小”、或“不变”)。
(4)已知1100℃时,K=0.263,此时测得高炉中c(CO2)=0.025mol/L ·c(CO)=0.1mol/L,在这种情况下,该反应是否处于化学平衡状态________(填“是”或“否”),此时化学反应速率是 ________
________ (填“<”、“>”或“=”),其原因是________。
(填“<”、“>”或“=”),其原因是________。
-
高炉炼铁过程中发生的主要反应为: Fe2O3(s)+CO(g)
Fe2O3(s)+CO(g)
 Fe(s)+CO2(g);在1000℃时,平衡常数为4.0;在1300℃时,平衡常数为3.5。下列说法中,正确的是( )
Fe(s)+CO2(g);在1000℃时,平衡常数为4.0;在1300℃时,平衡常数为3.5。下列说法中,正确的是( )
A. 平衡常数的表达式为:K=
B. 在1000℃时,10L的密闭容器中,加入Fe、Fe2O3、CO、CO2各1mol,10min达到平衡,υ(CO2)=0.006mol/(L·min)
C. 一段时间以后,铁的量不再变化,不能说明该反应达到平衡
D. 下图表示不同温度下,CO的转化率与时间关系图像

-
Ⅰ.高炉炼铁过程中发生的主要反应为:
 Fe2O3(s)+CO(g)⇌
Fe2O3(s)+CO(g)⇌ Fe(s)+CO2(g)
Fe(s)+CO2(g)
已知该反应在不同温度下的平衡常数如下:
| 温度/℃ | 1000 | 1150 | 1300 |
| 平衡常数 | 4.0 | 3.7 | 3.5 |
请回答以下问题:
(1)该反应的平衡常数表达式K=______,△H=______0(填“>”、“<”或“=”).
(2)在体积为10L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各1.0mol,反应经过10min后达到平衡,该时间范围内反应的平均反应速度v(CO2)=______,CO的平衡转化率为______.
Ⅱ.在氯氧化法处理含CN-的废水过程中,液氯在碱性条件下可以将氰化物氧化成氰酸盐(其毒性仅为氰化物的千分之一),氰酸盐进一步被氧化为无毒物质.
(1)某厂废水中含KCN,其浓度为650mg/L.现用氯氧化法处理,发生如下反应(其中N均为-3价):KCN+2KOH+Cl2═KOCN+2KCl+H2O,则被氧化的元素是______.
(2)投入过量液氯,可将氰酸盐进一步氧化为氮气,请配平下列化学方程式:
______KOCN+______KOH+______Cl2═______CO2+______N2+______KCl+______H2O
(3)若处理上述废水20L,使KCN完全转化为无毒物质,至少需液氯______g.
-
高炉炼铁过程中发生的反应: Fe2O3(s)+CO(g)
Fe2O3(s)+CO(g)
 Fe(s)+CO2(g),已知该反应在不同温度下的平衡常数如下表,下列说法不正确的是( )
Fe(s)+CO2(g),已知该反应在不同温度下的平衡常数如下表,下列说法不正确的是( )
| 温度/℃ | 1000 | 1150 | 1300 |
| 平衡常数 | 4.0 | 3.7 | 3.5 |
A.△H<0
B.该反应的平衡常数表达式是K=
C.其他条件不变,向平衡体系充入CO2气体,K值减小
D.其他条件不变,升高温度,可以降低CO的平衡转化率
-
高炉炼铁过程中发生的主要反应为
 Fe2O3(s)+CO(g)=
Fe2O3(s)+CO(g)= Fe(s)+CO2(g)已知该反应在不同温度下的平衡常数如下:
Fe(s)+CO2(g)已知该反应在不同温度下的平衡常数如下:
| 温度/℃ | 1000 | 1150 | 1300 |
| 平衡常数 | 4.0 | 3.7 | 3.5 |
请回答下列问题:
(1)该反应的平衡常数表达式K=______,△H______0(填“>”、“<”或“=”);
(2)在一个容积为10L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各1.0mol,反应经过10min后达到平衡.求该时间范围内反应的平均反应速率v(C02)=______、CO的平衡转化率=______:
(3)欲提高(2)中CO的平衡转化率,可采取的措施是______.
A.减少Fe的量 B.增加Fe23的量 C.移出部分C02
D.提高反应温度 E.减小容器的容积 F.加入合适的催化剂.
-
)高炉炼铁过程中发生的主要反应为
Fe2O3(s)+CO(g) Fe(s)+CO2(g)
Fe(s)+CO2(g)
已知该反应在不同温度下的平衡常数如下:
| 温度/℃ | 1 000 | 1 150 | 1 300 |
| 平衡常数 | 4.0 | 3.7 | 3.5 |
请回答下列问题:
(1)该反应的平衡常数表达式K= ,ΔH (填“>”“<”或“=”)0。
(2)在一个容积为10 L的密闭容器中,1 000 ℃时加入Fe、Fe2O3、CO、CO2各1.0 mol,反应经过10 min后达到平衡。求该时间范围内反应的平均反应速率v(CO2)= 、CO的平衡转化率= 。
(3)欲提高(2)中CO的平衡转化率,可采取的措施是 。
A.减少Fe的量
B.增加Fe2O3的量
C.移出部分CO2
D.提高反应温度
E.减小容器的容积
F.加入合适的催化剂
Fe(s)+CO2(g) ΔH>0,其平衡常数表达式为K= ,又知1 100 ℃时,K=0.28。


