-
(12分)高炉炼铁中发生的基本反应如下:FeO(s)+CO(g)s Fe(s)+CO2(g) △H>0。
Fe(s)+CO2(g) △H>0。
(1)下列可以作为判断该反应已经达到化学平衡状态依据的是________。
a.高炉内压强不变
b.CO2的生成速率和CO的生成速率相等
c.混合气体中CO2的浓度不变
d.c(CO2)=c(CO)
(2)此反应的平衡常数表达式为K=________。
(3)温度升高平衡常数K值________(填“增大”“减小”、或“不变”)。
(4)已知1100℃时,K=0.263,此时测得高炉中c(CO2)=0.025mol/L ·c(CO)=0.1mol/L,在这种情况下,该反应是否处于化学平衡状态________(填“是”或“否”),此时化学反应速率是 ________
________ (填“<”、“>”或“=”),其原因是________。
(填“<”、“>”或“=”),其原因是________。
-
高炉炼铁中发生的基本反应之一如下:
FeO(s)+CO(g) Fe(s)+CO2(g) ΔH>0,其平衡常数表达式为K= ,又知1 100 ℃时,K=0.28。
Fe(s)+CO2(g) ΔH>0,其平衡常数表达式为K= ,又知1 100 ℃时,K=0.28。
(1)温度升高,化学平衡移动后达到新的平衡,平衡常数 。(填“变大”“变小”或“不变”)
(2)1 100 ℃时测得高炉中c(CO2)=0.013 mol·L-1,c(CO)=0.05 mol·L-1,在这种情况下,该反应是否处于化学平衡状态: (填“是”或“否”),此时,化学反应速率是v(正) v(逆)(填“大于”“小于”或“等于”),其原因 。
-
高炉炼铁中发生的基本反应之一为:FeO(s)+CO(g) Fe(s)+CO2(g)ΔH>0,已知1 373 K时K=0.263。
Fe(s)+CO2(g)ΔH>0,已知1 373 K时K=0.263。
(1)该反应的平衡常数表达式为 。
(2)温度升高,化学平衡移动后,平衡常数K值 (填“增大”、“减小”或“不变”)。
(3)1 373 K时测得高炉中c(CO2)=0.025 mol/L,c(CO)=0.1 mol/L,在这种情况下,该反应是否处于化学平衡状态 (填“是”或“否”)。此时,化学反应速率v(正) v(逆)(填“大于”、“等于”或“小于”),其原因是 。
-
铁及其化合物在日常生活、生产中应用广泛,研究铁及其化合物的应用意义重大。试回答下列问题:
(1)已知:高炉炼铁过程中会发生如下反应:
①FeO(s)+CO(g)===Fe(s)+CO2(g) ΔH1
②3Fe2O3(s)+CO(g)===2Fe3O4(s)+CO2(g) ΔH2
③Fe3O4(s)+CO(g)===3FeO(s)+CO2(g) ΔH3
则反应Fe2O3(s)+3CO(g)===2Fe(s)+3CO2(g)的ΔH的表达式为_______________________________(用含ΔH1、ΔH2、ΔH3的代数式表示)。
(2)上述反应在高炉中大致分为三个阶段,各阶段主要成分与温度的关系如下表:
| 温度/℃ | 250 | 600 | 1000 | 2000 |
| 主要成分 | Fe2O3 | Fe3O4 | FeO | Fe |
1600 ℃时固体物质的主要成分为_____________(填化学式);若该温度下,测得固体混合物中m(Fe)∶m(O)=35∶4,则FeO被CO还原为Fe的百分率为______________(设其他固体杂质中不含Fe、O元素)。
(3)铁的某些化合物可用作CO与H2反应的催化剂。已知某种铁的化合物可用来催化反应:CO(g) + 3H2(g) CH4(g) + H2O(g) ΔH <0 。
CH4(g) + H2O(g) ΔH <0 。
在T ℃、a MPa时,将2 mol CO和6 mol H2充入某容积可变的密闭容器中,实验测得CO的物质的量在反应体系中所占百分比x(CO)如下表:
| t/min | 0 | 10 | 20 | 30 | 40 | 50 |
| x(CO) | 0.25 | 0.23 | 0.21 | 0.20 | 0.10 | 0.10 |
① T ℃ a MPa时,此反应的平衡常数K = ____________(保留1位小数)。达到平衡时CO的转化率为___________。

②上图表示该反应CO的平衡转化率与温度、压强的关系。
图中温度T1、T2、T3由低到高的顺序是________________。图中显示其它条件固定时,增加压强会导致平衡向___________(填“左”或“右”)移动。
-
铁及其化合物在日常生活、生产中应用广泛,研究铁及其化合物的应用意义重大。请回答下列问题:
(1)已知高炉炼铁过程中会发生如下反应:
FeO(s)+CO(g) Fe(s)+CO2(g) K1 ΔH1=a kJ·mol−1
Fe(s)+CO2(g) K1 ΔH1=a kJ·mol−1
3Fe2O3(s)+CO(g) 2Fe3O4(s)+CO2(g) K2 ΔH2=b kJ·mol−1
2Fe3O4(s)+CO2(g) K2 ΔH2=b kJ·mol−1
Fe3O4(s)+CO(g) 3FeO(s)+CO2(g) K3 ΔH3=c kJ·mol−1
3FeO(s)+CO2(g) K3 ΔH3=c kJ·mol−1
①Fe2O3(s)+3CO(g) 2Fe(s)+3CO2(g) ΔH=_____kJ·mol−1(用含a、b、c的代数式表示)。
2Fe(s)+3CO2(g) ΔH=_____kJ·mol−1(用含a、b、c的代数式表示)。
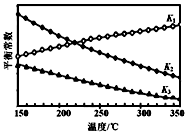
②上述反应对应的平衡常数K1、K2、K3随温度变化的曲线如图所示。则a_________b,(填“>”、“<”或“=”),理由是_________________。
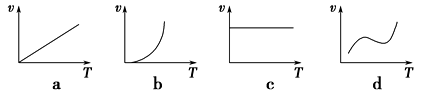
(2)铁的氧化物粉末和Al粉在镁条的引燃下可以发生铝热反应,下列反应速率(v)和温度(T)的关系示意图中与铝热反应最接近的是________。
(3)铁等金属可用作CO与H2反应的催化剂:CO(g)+3H2(g) CH4(g)+H2O(g)
CH4(g)+H2O(g)
ΔH<0。在T℃,将l mol CO和3 mol H2加入2 L的密闭容器中。实验测得n(CO)随时间的变化如下表:
| t/min | 0 | 10 | 20 | 30 | 40 | 50 |
| n(CO)/mol | 1.0 | 0.70 | 0.45 | 0.25 | 0.10 | 0.10 |
①下列能判断该反应达到平衡的标志是______(填序号)。
a.容器内压强不再发生变化 b.混合气体的密度不再发生变化
c.v正(CO)=3v逆(H2) d.混合气体的平均相对分子质量不再发生变化
②在0~20 min内v (H2)=______;在T℃时该反应的平衡常数K=_________。
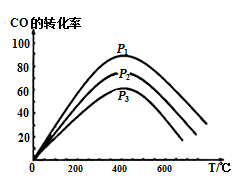
③下图表示该反应中CO的转化率与温度、压强的关系。图中压强P1、P2、P3由高到低的顺序是_________。
-
铁及其化合物在日常生活、生产中应用广泛,研究铁及其化合物的应用意义重大.回答下列问题:
(1)已知高炉炼铁过程中会发生如下反应:
FeO(s)+ CO(g)═Fe(s)+CO2(g)△H1
Fe2O3(s)+1/3 CO(g)═ 2/3 Fe3O4(s)+ 1/3 CO2(g)△H2
Fe3O4(s)+ CO(g)═3Fe(s)+CO2(g)△H3
Fe2O3(s)+ CO(g)═2Fe(s)+3CO2(g)△H4
则△H4 的表达式为_____(用含△H1、△H2、△H3 的代数式表示)。
(2)上述反应在高炉中大致分为三个阶段,各阶段主要成分与温度的关系如下:
| 温度 | 250℃ | 600℃ | 1000℃ | 2000℃ |
| 主要成分 | Fe2O3 | Fe3O4 | FeO | Fe |
1600℃时固体物质的主要成分为_____,该温度下若测得固体混合物中 m(Fe):m(O)=35:2, 则 FeO 被 CO 还原为 Fe 的百分率为_________(设其它固体杂质中不含 Fe、O 元素)。
(3)铁等金属可用作 CO 与氢气反应的催化剂.已知某种催化剂可用来催化反应 CO(g)+3H2(g) = CH4(g) +H2O(g)△H<0.在 T℃,106Pa 时将 l mol CO 和 3mol H2 加入体积可变的密闭容器 中.实验测得 CO 的体积分数 x(CO)如下表:
| t/min | 0 | 10 | 20 | 30 | 40 | 50 |
| x(CO) | 0.25 | 0.23 | 0.214 | 0.202 | 0.193 | 0.193 |
①能判断 CO(g)+3H2(g)⇌ CH4(g)+H2O(g)达到平衡的是_____(填序号)。
a.容器内压强不再发生变化 b.混合气体的密度不再发生变化
c.v 正(CO)=3v 逆(H2) d.混合气体的平均相对分子质量不再发生变化
②达到平衡时 CO 的转化率为___________;在 T℃106Pa 时该反应的压强平衡常数 Kp(用平衡分 压代替平衡浓度计算,分压=总压×物质的量分数)的计算式为_____。
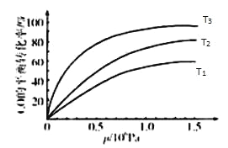
③图表示该反应 CO 的平衡转化率与温度、压强的关系.图中温度 T1、T2、T3 由高到低的顺序是_____,理由是_____________.
-
铁及其化合物在日常生活、生产中应用广泛,研究铁及其化合物的应用意义重大.回答下列问题:
(1)已知高炉炼铁过程中会发生如下反应:
FeO(s)+ CO(g)═Fe(s)+CO2(g)△H1
Fe2O3(s)+1/3CO(g)═ 2/3Fe3O4(s)+ 1/3 CO2(g)△H2
Fe3O4(s)+ CO(g)═3Fe(s)+CO2(g)△H3
Fe2O3(s)+ CO(g)═2Fe(s)+3CO2(g)△H4
则△H4 的表达式为_____(用含△H1、△H2、△H3 的代数式表示)。
(2)上述反应在高炉中大致分为三个阶段,各阶段主要成分与温度的关系如下:
| 温度 | 250℃ | 600℃ | 1000℃ | 2000℃ |
| 主要成分 | Fe2O3 | Fe3O4 | FeO | Fe |
1600℃时固体物质的主要成分为_____,该温度下若测得固体混合物中 m(Fe):m(O)=35:2, 则 FeO 被 CO 还原为 Fe 的百分率为_________(设其它固体杂质中不含 Fe、O 元素)。
(3)铁等金属可用作 CO 与氢气反应的催化剂.已知某种催化剂可用来催化反应 CO(g)+3H2(g) = CH4(g) +H2O(g)△H<0.在 T℃,106Pa 时将 l mol CO 和 3mol H2 加入体积可变的密闭容器 中.实验测得 CO 的体积分数 x(CO)如下表:
| t/min | 0 | 10 | 20 | 30 | 40 | 50 |
| x(CO) | 0.25 | 0.23 | 0.214 | 0.202 | 0.193 | 0.193 |
①能判断 CO(g)+3H2(g)⇌ CH4(g)+H2O(g)达到平衡的是_____(填序号)。
a.容器内压强不再发生变化 b.混合气体的密度不再发生变化
c.v 正(CO)=3v 逆(H2) d.混合气体的平均相对分子质量不再发生变化
②达到平衡时 CO 的转化率为___________;在 T℃106Pa 时该反应的压强平衡常数 Kp(用平衡分 压代替平衡浓度计算,分压=总压×物质的量分数)的计算式为_____。
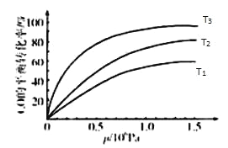
③图表示该反应 CO 的平衡转化率与温度、压强的关系.图中温度 T1、T2、T3 由高到低的顺序是_____,理由是_____________.
-
铁及其化合物在日常生活、生产中应用广泛,研究铁及其化合物的应用意义重大.回答下列问题:
(1)已知高炉炼铁过程中会发生如下反应:
FeO(s)+CO(g)═Fe(s)+CO2(g)△H1
Fe2O3(s)+ CO(g)═
CO(g)═ Fe3O4(s)+
Fe3O4(s)+ CO2(g)△H2
CO2(g)△H2
Fe3O4(s)+CO(g)═3Fe(s)+CO2(g)H3
Fe2O3(s)+CO(g)═2Fe(s)+3CO2(g)H4
则△H4的表达式为__________(用含△H1、△H2、△H3的代数式表示).
(2)上述反应在高炉中大致分为三个阶段,各阶段主要成分与温度的关系如下:
| 温度 | 250℃ | 600℃ | 1000℃ | 2000℃ |
| 主要成分 | Fe2O3 | Fe3O4 | FeO | Fe |
1600℃时固体物质的主要成分为__________,该温度下若测得固体混合物中m(Fe):m(O)=35:2,则FeO被CO还原为Fe的百分率为__________(设其它固体杂质中不含Fe、O元素).
(3)铁等金属可用作CO与氢气反应的催化剂.已知某种催化剂可用来催化反应CO(g)+3H2(g)⇌CH4(g)+H2O(g)△H<0.在T℃,106Pa时将lmolCO和3molH2加入体积可变的密闭容器中.实验测得CO的体积分数x(CO)如下表:
| t/min | 0 | 10 | 20 | 30 | 40 | 50 |
| x(CO) | 0.25 | 0.23 | 0.214 | 0.202 | 0.193 | 0.193 |
①能判断CO(g)+3H2(g) CH4(g)+H2O(g)达到平衡的是__________(填序号).
CH4(g)+H2O(g)达到平衡的是__________(填序号).
a.容器内压强不再发生变化 b.混合气体的密度不再发生变化
c.v正(CO)=3v逆(H2) d.混合气体的平均相对分子质量不再发生变化
②达到平衡时CO的转化率为__________;在T℃106Pa时该反应的压强平衡常数Kp(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)的计算式为__________;
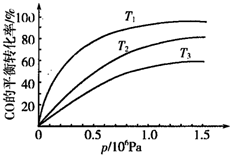
③图表示该反应CO的平衡转化率与温度、压强的关系.图中温度T1、T2、T3由高到低的顺序是__________,理由是__________。
-
“低碳循环”引起各国的高度重视,已知煤、甲烷等可以与水蒸气反应生成以CO和H2为主的合成气,合成气有广泛应用。试回答下列问题:
(1)高炉炼铁是CO气体的重要用途之一,其基本反应为:FeO(s)+CO(g) Fe(s)+CO2(g) ΔH>0。已知在1 100 ℃时,该反应的化学平衡常数K=0.263。
Fe(s)+CO2(g) ΔH>0。已知在1 100 ℃时,该反应的化学平衡常数K=0.263。
①温度升高,化学平衡移动后达到新的平衡,此时平衡常数K值 (填“增大”、“减小”或“不变”);
②1 100 ℃时测得高炉中,c(CO2)=0.025 mol·L-1,c(CO)=0.1 mol·L-1,则在这种情况下,该反应向 进行(填“左”或“右”),判断依据是 。
(2)目前工业上也可用CO2来生产燃料甲醇,有关反应为:CO2(g)+3H2(g)  CH3OH(g)+H2O(g) ΔH=-49.0 kJ·mol-1,现向体积为1 L的密闭容器中,充入1 mol CO2和3 mol H2,反应过程中测得CO2和CH3OH(g)的浓度随时间的变化如图所示。
CH3OH(g)+H2O(g) ΔH=-49.0 kJ·mol-1,现向体积为1 L的密闭容器中,充入1 mol CO2和3 mol H2,反应过程中测得CO2和CH3OH(g)的浓度随时间的变化如图所示。
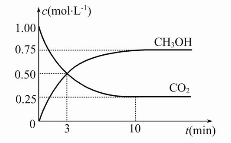
①从反应开始到平衡,氢气的平均反应速率v(H2)= 。
②反应达到平衡后,下列措施能使 增大的是 (填符号)。
增大的是 (填符号)。
A.升高温度 B.再充入H2 C.再充入CO2 D.将H2O(g)从体系中分离
E.充入He(g)
-
“低碳循环”引起各国的高度重视,已知煤、甲烷等可以与水蒸气反应生成以CO和H2为主的合成气,合成气有广泛应用。试回答下列问题:
(1)高炉炼铁是CO气体的重要用途之一,其基本反应为:
FeO(s)+CO(g)  Fe(s)+CO2(g) ΔH >0
Fe(s)+CO2(g) ΔH >0
已知在1100℃时,该反应的化学平衡常数K=0.263。
①温度升高,化学平衡移动后达到新的平衡,此时平衡常数K值__________(填“增大”、“减小”或“不变”);
②1100℃时测得高炉中,c(CO2)=0.025mol·L-1,c(CO)=0.1 mol·L-1,则在这种情况下,该反应向_______进行(填“左”或“右”),判断依据是________
________。
(2)一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO)。
已知:2CO(g) + O2(g)=2CO2(g) ΔH =–566 kJ·mol―1
2H2O(g) =2H2(g) + O2(g) ΔH =+484 kJ·mol―1
CH3OH(g) + 1/2O2(g)=CO2(g) + 2H2(g) ΔH =–192.9 kJ·mol―1
请写出CO与H2在一定条件下反应生成CH3OH(g)的热化学方程式
。
(3)目前工业上也可用CO2来生产燃料甲醇,有关反应为:CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH =-49.0 kJ·mol-1,现向体积为1 L的密闭 容器中,充入1mol CO2和3mol H2,反应过程中测得CO2和CH3OH(g)的浓度随时间的变化如图所示。
CH3OH(g)+H2O(g) ΔH =-49.0 kJ·mol-1,现向体积为1 L的密闭 容器中,充入1mol CO2和3mol H2,反应过程中测得CO2和CH3OH(g)的浓度随时间的变化如图所示。
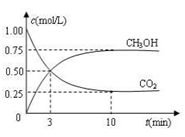
①从反应开始到平衡,氢气的平均反应速率v(H2)=________________;
②反应达到平衡后,下列措施能使 增大的是______(填符号)。
增大的是______(填符号)。
A.升高温度 B.再充入H2 C.再充入CO2
D.将H2O(g)从体系中分离 E.充入He(g)
Fe(s)+CO2(g) △H>0。
________
(填“<”、“>”或“=”),其原因是________。








