-
现代生产、生活和国防中大量使用电池.下列有关电池的说法正确的是( )
A.碱性锌锰电池性能好于普通电池的原因是能反复使用
B.碱性锌锰电池的正极是MnO2,当电池中有6.5g Zn反应时,将产生0.2molMnOOH
C.铅蓄电池放电时,负极的质量减少
D.使用碱性电解质的氢氧燃料电池,负极的电极反应是H2-2e-=2H+高二化学选择题中等难度题查看答案及解析
-
现代生产、生活和国防中大量使用电池。下列有关电池的说法正确的是
A.碱性锌锰电池性能好于普通电池的原因是能反复使用
B.碱性锌锰电池的正极是MnO2,当电池中有6.5g Zn反应时,将产生0.2molMnOOH
C.铅蓄电池放电时,负极的质量减少
D.使用碱性电解质的氢氧燃料电池,负极的电极反应是H2 - 2e- = 2H+
高二化学选择题中等难度题查看答案及解析
-
现代生产、生活和国防中大量使用电池。如照相机、手机、汽车、卫星等均要使用电池。了解常见电池的工作原理是中学生的必修课之一。请同学们用所学知识回答以下问题。
(1)铅蓄电池放电时的总反应:Pb+PbO2+2H2SO4=2PbSO4+2H2O。请写出放电时正极反应的电极反应式:_________________________。
(2)依据氧化还原反应Zn(s)+Cu2+(aq)===Zn2+(aq)+Cu(s)设计的原电池如图所示。
①请在图中标出电极材料及电解质溶液(写化学式)①___________,②____________,③_______________,④__________________
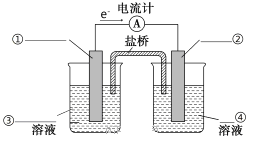
②盐桥中装有含琼胶的KCl饱和溶液,电池工作过程中盐桥中的Cl-向________极移动(填“左”或“右”)。
(3)燃料电池是一种连续地将燃料和氧化剂的化学能直接转换成电能的化学电池。下图是一个化学过程的示意图。
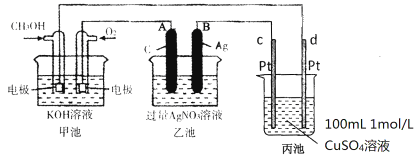
①A(石墨)电极的名称是_______________。
②通入CH3OH的电极的电极反应式是________________________________。
③乙池中反应的化学方程式为________________________________________。
④当电路中通过0.01mol电子时,丙池溶液的c(H+) = __________mol/L(忽略电解过程中溶液体积的变化)。
高二化学综合题困难题查看答案及解析
-
化学与生产、生活息息相关,下列叙述错误的是( )
A.碱性锌锰干电池比普通锌锰干电池性能好,比能量和可储存时间均有提高
B.汽车加大油门、把食物放在冰箱里,食品包装袋内放置小包除氧剂,都是为了改变反应物转化率而采取的措施
C.1kg人体脂肪可存储约32200kJ能量,一般人每行走1km大约要消耗170kg能量,如果每天步行5kg,一年(按365天计)中消耗的脂肪大约是9.6kg
D.炒菜用铁锅未及时洗净(残余中含NaCl),可能发生电化学腐蚀生成红褪色锈斑
高二化学单选题简单题查看答案及解析
-
化学与社会、生活密切相关。对下列现象或事实的解释正确的是
选项
现象或事实
解释
A
碱性锌锰电池比普通锌锰电池性能好
锌在碱性介质中被氧化成更高价态
B
配制FeCl2溶液时加入少量铁粉
抑制Fe2+的水解
C
施肥时,草木灰(有效成分为K2CO3)不能与铵盐氮肥混合使用
它们反应生成氨气会降低肥效
D
纯水和干木头都不导电,但木头用水浸湿后却可以导电
水和干木头的某些成分发生化学反应
高二化学选择题中等难度题查看答案及解析
-
化学与社会、生活密切相关。对下列现象或事实的解释正确的是
选项
现象或事实
解释
A
碱性锌锰电池比普通锌锰电池性能好
锌在碱性介质中被氧化成更高价态
B
施肥时,草木灰(有效成分为K2CO3)不能与铵盐氮肥混合使用
它们反应生成氨气会降低肥效
C
配制FeCl2溶液时加入少量铁粉
抑制Fe2+的水解
D
纯水和干木头都不导电,但木头用水浸湿后却可以导电
水和干木头的某些成分发生化学反应
A. A B. B C. C D. D
高二化学单选题困难题查看答案及解析
-
迄今为止,由化学能转变的热能或电能仍然是人类使用的主要的能源。
I.请仔细观察下列两种电池的构造示意图,完成下列问题:

(1)碱性锌锰电池比普通锌锰电池(干电池)性能好,放电电流大。试从影响反应速率的因素分析其原因是________。
(2)碱性锌锰电池的总反应式:Zn+2MnO2+2H2O=2MnOOH+Zn(OH)2,则负极的电极反应式为________。
Ⅱ.下面是一个将化学能与电能相互转化的装置。回答下列问题:

(1)写出通入O2一极的电极反应方程式为________。
(2)a电极是________极,能否写出其电极反应方程式________(填“能”或“不能”),若“能”写出其电极反应方程式,若“不能”说明其理由。
(3)下列说法不正确的是( )
A.此装置用于电镀铜时,电解一段时间,硫酸铜溶液的浓度不变
B.U型管中,OH—在a极放电
C.若a为纯净金属,b为粗制金属,该装置可用于粗制金属的精炼
D.电子经导线流入b电极
Ⅲ.某同学运用所学知识,自选材料设计实验,实现了在通常条件下不能发生的反应:Cu+H2SO4(稀)=CuSO4+H2↑。请在下面框中画出能够实验这一反应的装置图,并在图中进行必要的标注。

高二化学填空题困难题查看答案及解析
-
电化学的应用十分广泛,是现代生产、生活、国防,乃至整个人类生活不可缺的物质条件。请根据所给材料回答下列问题:
(1)请结合组成原电池的条件,将氧化还原反应:2Fe3++Cu=2Fe2++Cu2+设计成一个原电池。
①电解液:___,
②正极材料:___;
③负极反应式:___。
(2)用吸收H2后的稀土储氢合金作为电池负极材料(用MH表示),NiO(OH)作为电池正极材料,KOH溶液作为电解质溶液,可制得高容量,长寿命的镍氢电池。电池充放电时的总反应为:NiO(OH)+MH
Ni(OH)2+M
①电池放电时,负极的电极反应式为___。
②当该电池充电时,与外电源正极连接的电极上发生的反应是___。
A.H2O的还原 B.NiO(OH)的还原 C.H2的氧化 D.Ni(OH)2的氧化
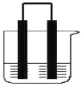
(3)按如图电解饱和食盐水溶液,写出该电解池中发生反应的总反应式:___;将充分电解后所得溶液逐滴加入到酚酞试液中,观察到的现象是:___。

高二化学综合题中等难度题查看答案及解析
-
化学与生产、生活、科技密切相关,下列有关说法错误的是
A. 为保护轮船的外壳,常在外壳上镶入锌块
B. 明矾溶于水后产生具有吸附性的胶体粒子,可作漂白剂
C. 燃料电池的能量转换效率远高于普通燃料燃烧的能量转换效率
D. 锅炉水垢中的硫酸钙可用碳酸钠溶液处理,使之转化为碳酸钙,再用酸除去
高二化学单选题中等难度题查看答案及解析
-
化学与生产生活实际密切联系。下列说法不正确的是
A.氢能可再生,没有污染,现已用作火箭和燃料电池的燃料
B.在环保领域,酸性或碱性废水的处理常常利用中和反应
C.为防止电池中的重金属等污染土壤和水体,应积极开发废电池的综合利用技术
D.保护轮船船体,多采用外加电流的阴极保护法
高二化学选择题中等难度题查看答案及解析