-
A、B、C、D、E、X、F是周期表中前四周期的七种元素,它们的原子序数依次增大。A元素的核外电子数和电子层数相等,是宇宙中最丰富的元素。B的最外层电子数为其内层电子数的2倍,D基态原子的s能级和p能级上电子数相等,E在短周期元素中第一电离能最小,X与D同主族,F在周期表的第八列。
(1)基态F原子的核外有_______种运动状态的电子。基态F3+的最外层电子排布式是________。
(2)B、C、D三种元素的电负性由大到小的排列是_______(填元素符号)。
(3)A、B、D 形成BA2D型分子,该分子的空间构型为________。
(4)BC-中B原子的杂化轨道类型是_______,该离子中含有的σ键与π键的数目之比为_____。写出一种与该分子互为等电子体的单质分子的结构式_______。
(5)E2X与E2D相比较熔点较高的是______(填化学式),原因是__________。
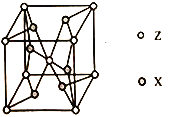
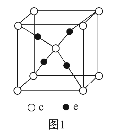
(6)奧氏体是B溶解在F中形成的一种间隙固溶体,无磁性,其晶胞为面心立方结构,如图所示,则该物质的化学式为_______。若晶体密度为d g.cm-3,则晶胞中最近的两个B原子的距离为______pm(阿伏加德罗常数的值用NA表示,写出简化后的计算式即可)。
-
A、B、C、D、E、X、F是周期表中前四周期的七种元素,它们的原子序数依次增大。A元素的核外电子数和电子层数相等,是宇宙中最丰富的元素。B的最外层电子数为其内层电子数的2倍,D基态原子的s能级和p能级上电子数相等,E在短周期元素中第一电离能最小,X与D同主族,F在周期表的第八列。
(1)基态F原子的核外有_______种运动状态的电子。基态F3+的最外层电子排布式是________。
(2)B、C、D三种元素的电负性由大到小的排列是_______(填元素符号)。
(3)A、B、D 形成BA2D型分子,该分子的空间构型为________。
(4)BC-中B原子的杂化轨道类型是_______,该离子中含有的σ键与π键的数目之比为_____。写出一种与该分子互为等电子体的单质分子的结构式_______。
(5)E2X与E2D相比较熔点较高的是______(填化学式),原因是__________。
(6)奧氏体是B溶解在F中形成的一种间隙固溶体,无磁性,其晶胞为面心立方结构,如图所示,则该物质的化学式为_______。若晶体密度为d g.cm-3,则晶胞中最近的两个B原子的距离为______pm(阿伏加德罗常数的值用NA表示,写出简化后的计算式即可)。
-
W、X、Y、Z为原子序数依次增大的前四周期元素,元素W是宇宙中最丰富的元素,元素X的原子的最外层电子数是其内层电子数的3倍,元素Z的基态原子核外电子有24种运动状态,Y、X、Z不在同一周期,且元素Y的基态原子核外p电子比s电子多5个。
(1)Z的基态原子的核外电子排布式为____________________。
(2)Z的氧化物是石油化工中重要的催化剂之一,可催化异丙苯裂化生成苯和丙烯
①1 mol丙烯分子中含有 键与
键与 键数目之比为__________________。
键数目之比为__________________。
②苯分子中碳原子的杂化类型为_________________。
③Z的一种氧化物ZO5中,Z的化合价为+6,则其中过氧键的数目为______________。
(3)W、X、Y三种元素的电负性由小到大的顺序为_________________(用元素符号表示)。
(4)ZY3的熔点为1152℃,其在熔融状态下能够导电,据此可判断ZY3晶体属于____________(填晶体类型)。
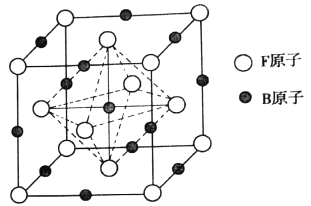
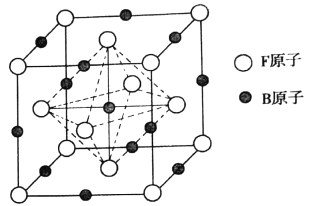
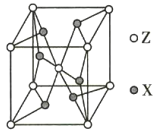
(5)ZX2晶体的晶胞结构如图所示。若该化合物的相对分子质量为M,晶胞边长为a pm,阿伏加德罗常数的值为NA,则该晶体的密度为_________ g/cm3。
-
现有七种元素,其中A、B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大.请根据下列相关信息,回答问题.
| A元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B元素原子的核外p电子数比s电子数少1 |
C原子的第一至第四电离能分别是:
I1=738kJ/mol I2=1451kJ/mol I3=7733kJ/mol I4=10540kJ/mol |
| D原子核外所有p轨道全满或半满 |
| E元素的主族序数与周期数的差为4 |
| F是前四周期中电负性最小的元素 |
| G在周期表的第七列 |

(1)已知BA5为离子化合物,写出其电子式______.
(2)B基态原子中能量最高的电子,其电子云在空间有______个方向,原子轨道呈______形
(3)某同学根据上述信息,推断C基态原子的核外电子排布如图:该同学所画的电子排布图违背了______.
(4)G位于______族______区,价电子排布式为______.
(5)DE3中心原子的杂化方式为______,用价层电子对互斥理论推测其空间构型为______.
(6)检验F元素的方法是______,请用原子结构的知识解释产生此现象的原因是______.
(7)若某单质晶体中原子的堆积方式如图甲所示,其晶胞特征如图乙所示,原子之间相互位置关系的平面图如图丙所示.则晶胞中该原子的配位数为______,该单质晶体中原子的堆积方式为四种基本模式中的______.
-
(15分)
现有七种元素,其中A、B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答问题.
| A元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B元素原子的核外p电子数比s电子数少1 |
| C原子的第一至第四电离能分别是: I1=738kJ/mol I2 = 1451 kJ/mol I3 = 7733kJ/mol I4 = 10540kJ/mol |
| D原子核外所有p轨道全满或半满 |
| E元素的主族序数与周期数的差为4 |
| F是前四周期中电负性最小的元素 |
| G在周期表的第七列 |
⑴已知BA5 为离子化合物,写出其电子式________.
⑵B基态原子中能量最高的电子,其电子云在空间有________个方向,原子轨道呈________形
 ⑶某同学根据上述信息,推断C基态原子的核外电子排布为:
⑶某同学根据上述信息,推断C基态原子的核外电子排布为:
该同学所画的电子排布图违背了.
⑷G位于________族________区,价电子排布式为________.
⑸DE3 中心原子的杂化方式为________,用价层电子对互斥理论推测其空间构型
为________.
⑹检验F元素的方法是________,请用原子结构的知识解释产生此现象的原因是________.
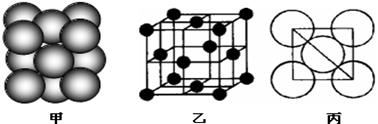
⑺若某单质晶体中原子的堆积方式如下图甲所示,其晶胞特征如下图乙所示,原子之间相互位置关系的平面图如下图丙所示。则晶胞中该原子的配位数为________ ,该单质晶体中原子的堆积方式为四种基本模式中的________.
-
(15分)现有七种元素,其中A、B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答问题.
| A元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B元素原子的核外p电子数比s电子数少1 |
| C原子的第一至第四电离能分别是: I1=738kJ/mol I2 = 1451 kJ/mol I3 = 7733kJ/mol I4 = 10540kJ/mol |
| D原子核外所有p轨道全满或半满 |
| E元素的主族序数与周期数的差为4 |
| F是前四周期中电负性最小的元素 |
| G在周期表的第七列 |
⑴已知BA5 为离子化合物,写出其电子式________.
⑵B基态原子中能量最高的电子,其电子云在空间有________个方向,原子轨道呈________形
⑶某同学根据上述信息,推断C基态原子的核外电子排布为:
该同学所画的电子排布图违背了________.
⑷G位于________族________区,价电子排布式为________.
⑸DE3 中心原子的杂化方式为________,用价层电子对互斥理论推测其空间构型为________.
⑹检验F元素的方法是________,请用原子结构的知识解释产生此现象的原因是________.
⑺若某单质晶体中原子的堆积方式如下图甲所示,其晶胞特征如下图乙所示,原子之间相互位置关系的平面图如下图丙所示。则晶胞中该原子的配位数为________ ,该单质晶体中原子的堆积方式为四种基本模式中的________.

-
(15分)现有七种元素,其中A、B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答问题.
| A元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B元素原子的核外p电子数比s电子数少1 |
| C原子的第一至第四电离能分别是: I1=738kJ/mol I2 = 1451 kJ/mol I3 = 7733kJ/mol I4 = 10540kJ/mol |
| D原子核外所有p轨道全满或半满 |
| E元素的主族序数与周期数的差为4 |
| F是前四周期中电负性最小的元素 |
| G在周期表的第七列 |
⑴已知BA5 为离子化合物,写出其电子式________.
⑵B基态原子中能量最高的电子,其电子云在空间有________个方向,原子轨道呈________形
⑶某同学根据上述信息,推断C基态原子的核外电子排布为:
该同学所画的电子排布图违背了________.
⑷G位于________族________区,价电子排布式为________.
⑸DE3 中心原子的杂化方式为________,用价层电子对互斥理论推测其空间构型为________.
⑹检验F元素的方法是________,请用原子结构的知识解释产生此现象的原因是________.
⑺若某单质晶体中原子的堆积方式如下图甲所示,其晶胞特征如下图乙所示,原子之间相互位置关系的平面图如下图丙所示。则晶胞中该原子的配位数为________ ,该单质晶体中原子的堆积方式为四种基本模式中的________.

-
W、X、Y、Z为原子序数依次增大的前四周期元素,元素W是宇宙中最丰富的元素,元素X的原子最外层电子数是其内层的3倍,元素Z的基态原子核外电子有24种运动状态,Y、X、Z不在同一周期,且Y原子核外p电子比s电子多5个。
(1)Z基态原子的核外电子排布式为__________。
(2)Z的氧化物是石油化工中重要的催化剂之一,如催化异丙苯( )裂化生成苯和丙烯。
)裂化生成苯和丙烯。
①1mol丙烯分子中含有σ键与π键数目之比为_______。
②苯分子中碳原子轨道的杂化类型为__________。
③Z的一种氧化物ZO5中,Z的化合价为+6,则其中过氧键的数目为_______个。
(3)W、X、Y三种元素的电负性由小到大顺序为__________。(请用元素符号回答)
(4)ZY3熔点为1152℃,熔融状态下能够导电,据此可判断ZY3晶体属于__________(填晶体类型)。
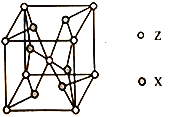
(5)ZX2晶体的晶胞结构如图,每个Z原子周围最近的X 原子数目为__________。若该化合物的相对分子质量为M,晶胞边长为acm,阿伏加德罗常数为NA,则该晶体的密度为_________g/cm3。
-
W、X、Y、Z为原子序数依次增大的前四周期元素,元素W是宇宙中最丰富的元素,元素X的原子最外层电子数是其内层的3倍,元素Z的基态原子核外电子有24种运动状态,Y、X、Z不在同一周期,且Y原子核外p电子比s电子多5个。
(1)Z基态原子的核外电子排布式为__________。
(2)Z的氧化物是石油化工中重要的催化剂之一,如催化异丙苯( )裂化生成苯和丙烯。
)裂化生成苯和丙烯。
①1mol丙烯分子中含有σ键与π键数目之比为_______。
②苯分子中碳原子轨道的杂化类型为__________。
③Z的一种氧化物ZO5中,Z的化合价为+6,则其中过氧键的数目为_______个。
(3)W、X、Y三种元素的电负性由小到大顺序为__________。(请用元素符号回答)
(4)ZY3熔点为1152℃,熔融状态下能够导电,据此可判断ZY3晶体属于__________(填晶体类型)。
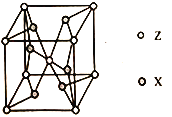
(5)ZX2晶体的晶胞结构如图,每个Z原子周围最近的X 原子数目为__________。若该化合物的相对分子质量为M,晶胞边长为acm,阿伏加德罗常数为NA,则该晶体的密度为_________g/cm3。
-
W、X、Y、Z为原子序数依次增大的前四周期元素,元素W是宇宙中最丰富的元素,元素X的原子最外层电子数是其内层的3倍,元素Z的基态原子核外电子有24种运动状态,Y、X、Z不在同一周期,且Y原子核外p电子比s电子多5个。
(1)Z基态原子的核外电子排布式为__________。
(2)Z的氧化物是石油化工中重要的催化剂之一,如催化异丙苯( )裂化生成苯和丙烯。
)裂化生成苯和丙烯。
①1mol丙烯分子中含有σ键与π键数目之比为_______。
②苯分子中碳原子轨道的杂化类型为__________。
③Z的一种氧化物ZO5中,Z的化合价为+6,则其中过氧键的数目为_______个。
(3)W、X、Y三种元素的电负性由小到大顺序为__________。(请用元素符号回答)
(4)ZY3熔点为1152℃,熔融状态下能够导电,据此可判断ZY3晶体属于__________(填晶体类型)。
(5)ZX2晶体的晶胞结构如图,每个Z原子周围最近的X 原子数目为__________。若该化合物的相对分子质量为M,晶胞边长为acm,阿伏加德罗常数为NA,则该晶体的密度为_________g/cm3。