与实际化工生产功能相符合的化学方程式是
A. 工业制取乙烯: C2H5OHCH2=CH2↑+H2O
B. 工业合成盐酸:H2 + Cl2 2HCl
C. 工业获取氯化钠:2Na + Cl2 2NaCl
D. 工业制漂粉精:2Ca(OH)2+2Cl2 → Ca(ClO)2+CaCl2+2H2O
高三化学单选题中等难度题
与实际化工生产功能相符合的化学方程式是
A. 工业制取乙烯: C2H5OHCH2=CH2↑+H2O
B. 工业合成盐酸:H2 + Cl2 2HCl
C. 工业获取氯化钠:2Na + Cl2 2NaCl
D. 工业制漂粉精:2Ca(OH)2+2Cl2 → Ca(ClO)2+CaCl2+2H2O
高三化学单选题中等难度题
与实际化工生产功能相符合的化学方程式是
A. 工业制取乙烯: C2H5OHCH2=CH2↑+H2O
B. 工业合成盐酸:H2 + Cl2 2HCl
C. 工业获取氯化钠:2Na + Cl2 2NaCl
D. 工业制漂粉精:2Ca(OH)2+2Cl2 → Ca(ClO)2+CaCl2+2H2O
高三化学单选题中等难度题查看答案及解析
与实际化工生产功能相符合的化学方程式是( )
A.工业合成氨:N2+3H22NH3
B.工业合成盐酸:H2+Cl22HCl
C.工业获取氯化钠:2Na+Cl22NaCl
D.工业制取氯气:2NaCl+2H2O2NaOH+H2↑+Cl2↑
高三化学多选题简单题查看答案及解析
下列有关化工生产原理正确的是
A. 工业制取烧碱:Na2O+H2O=2NaOH
B. 工业合成盐酸:H2+Cl22HCl
C. 工业制取乙烯:C2H5OHCH2=CH2↑+H2O
D. 工业制漂粉精:2Ca(OH)2+2Cl2 =Ca(ClO)2+CaCl2+2H2O
高三化学单选题中等难度题查看答案及解析
(14分)苯乙烯(C6H5CH=CH2)是合成橡胶和塑料的单体,用来生产丁苯橡胶、聚苯乙烯等。工业上以乙苯(C6H5CH2CH3)为原料,采用催化脱氢的方法制取苯乙烯,反应方程式为:
C6H5CH2CH3(g) C6H5CH=CH2(g)+H2(g)
H
(1)已知:H2和CO的燃烧热(H)分别为-285.8 kJ.mol
和-283.0 kJ.mol
;
C6H5CH2CH3(g)+CO2 (g) C6H5CH=CH2(g)+CO(g)+H2O(l)
H=+114.8 kJ·mol-1
则制取苯乙烯反应的H为_________
(2)向密闭容器中加入1 mol乙苯,在恒温恒容条件下合成苯乙烯,达平衡时,反应的能量变化为QkJ。下列说法正确的是 _________。
A.升高温度,正反应速率减小,逆反应速率增大
B.若继续加入1 mol乙苯,苯乙烯转化率增大
C.压缩体积,平衡逆向移动,反应物浓度增大,生成物浓度减小
D.相同条件下若起始加入1 mol苯乙烯和1 mol氢气,
达平衡时反应能量变化为(H-Q)kJ
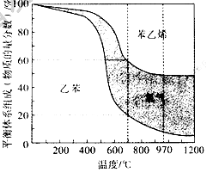
(3)向2 L密闭容器中加入1 mol乙苯发生反应,达到平衡状态时,平衡体系组成(物质的量分数)与温度的关系如图所示。700时,乙苯的平衡转化率为_______,此温度下该反应的平衡常数为 ______;温度高于970
时,苯乙烯的产率不再增加,其原因可能是_________。
(4)含苯乙烯的废水排放会对环境造成严重污染,可采用电解法去除废水中的苯乙烯,基本原理是在阳极材料MOx上生成自由基MOx(OH),其进一步氧化有机物生成CO2 ,该阳极的电极反应式为_________,若去除0.5 mol苯乙烯,两极共收集气体_________mol。
高三化学简答题极难题查看答案及解析
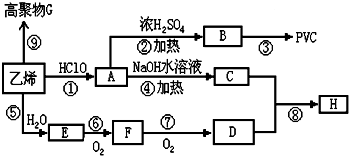
高三化学解答题中等难度题查看答案及解析
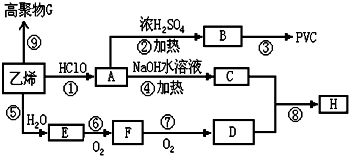
高三化学解答题中等难度题查看答案及解析
(2013•重庆二模)下列工业生产所涉及的化学用语表达不正确是( )
A.工业上制取氯气:MnO2+4HClCl2↑+MnCl2+H2O
B.工业上合成氨:N2+3H2 2NH3
C.工业上制取粗硅:SiO2+2CSi+2CO↑
D.工业上生产漂白粉:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O
高三化学选择题中等难度题查看答案及解析
下列工业生产所涉及的化学用语表达不正确是
A.工业上制取氯气:MnO2+4HClCl2↑+MnCl2+H2O
B.工业上合成氨:N2+3H2 2NH3
C.工业上制取粗硅:SiO2+2C Si+2CO↑
D.工业上生产漂白粉:
高三化学单选题中等难度题查看答案及解析
下列方程式正确的是( )
A.小苏打与盐酸反应的离子方程式:CO32−+H+=CO2↑+H2O
B.乙烯与氯化氢加成的化学方程式:CH2=CH2+HClCH3=CH2Cl
C.碳酸钾在水中的电离方程式:K2CO32K++CO32−
D.醋酸钠水解的离子方程式:CH3COO−+H2OCH3COOH+OH−
高三化学单选题简单题查看答案及解析
苯乙烯是重要的基础有机化工原料。工业中以乙苯(C6H5-CH2CH3)为原料,采用催化脱氢的方法制取苯乙烯(C6H5-CH=CH2)的反应方程式:
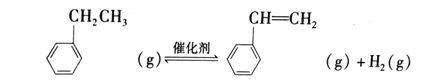 △H(1)已知:
△H(1)已知:
| 化学键 | C-H | C-C | C=C | H-H |
| 键能/kJ·molˉ1 | 412 | 348 | 612 | 436 |
计算上述反应的△H=________ kJ·mol-1。
(2)一定条件下,在体积不变的密闭容器中,反应过程中各物质浓度随时间变化的关系如下图所示。在t1时刻加入H2,t2时刻再次达到平衡。物质X为__________,判断理由是_______________________。
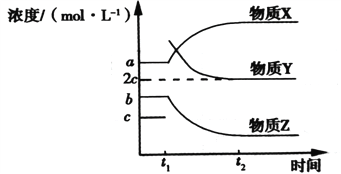
(3)在体积为2L的恒温密闭容器中通入2mol乙苯蒸汽,2分钟后达到平衡,测得氢气的浓度是0.5mol/L,则乙苯蒸汽的反应速率为_________________;维持温度和容器体积不变,向上述平衡中再通入1mol氢气和1mol乙苯蒸汽,则v正_______v逆(填“大于”、“小于”或“等于”)。
(4)实际生产时反应在常压下进行,且向乙苯蒸气中掺入水蒸气,利用热力学数据计算得到温度和投料比M对乙苯平衡转化率的影响可用如图表示。[M=n(H2O)/n(乙苯)]
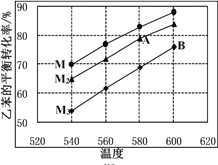
① 比较图中A、B两点对应的平衡常数大小:KA________KB
② 图中投料比(M1、M2、M3)的大小顺序为________。
高三化学综合题中等难度题查看答案及解析