-
下列有关硅的叙述中,正确的是
A.工业上通常以SiO2为原料,用氧化剂与其反应制备单质硅
B.硅是构成矿物和岩石的主要元素,硅在地壳中的含量在所有的元素中居第一 位
C.硅的化学性质不活泼,在自然界中可以以游离态存在
D.硅在电子工业中,是重要的半导体材料
高三化学单选题中等难度题查看答案及解析
-
下列有关硅的叙述中,正确的是
A.工业上通常以SiO2为原料,用氧化剂与其反应制备单质硅
B.硅是构成矿物和岩石的主要元素,硅在地壳中的含量在所有元素中居第一位
C.硅的化学性质不活泼,在自然界中可以以游离态存在
D.硅在电子工业中,是重要的半导体材料
高三化学选择题中等难度题查看答案及解析
-
下列关于硅单质及其化合物的叙述正确的是( )
① 硅是构成岩石和许多矿物的基本元素 ② 水玻璃可用作制备木材防火剂的原料
③ 制造光导纤维的主要原料是SiO2 ④ 制玻璃和水泥均需要石灰石作为原料
⑤ 硅胶可用作催化剂的载体和袋装食品的干燥剂
⑥ 高纯度的硅除了用于制造计算机芯片外,在太阳能发电过程中也具有重要的作用
A.①②③⑤ B.①③④⑤ C.①③⑥ D.全部
高三化学选择题简单题查看答案及解析
-
下列关于硅单质及其化合物的叙述正确的是 ( )
① 硅是构成岩石和许多矿物的基本元素 ② 水玻璃可用作制备木材防火剂的原料
③ 制造光导纤维的主要原料是SiO2 ④ 制玻璃和水泥均需要石灰石作为原料
⑤ 硅胶可用作催化剂的载体和袋装食品的干燥剂
⑥ 高纯度的硅除了用于制造计算机芯片外,在太阳能发电过程中也具有重要的作用
A.①②③⑤ B.①③④⑤ C.①③⑥ D.全部
高三化学选择题中等难度题查看答案及解析
-
下列关于硅单质及其化合物的叙述正确的是( )
①硅是构成岩石和许多矿物的基本元素 ②水玻璃可用作制备木材防火剂的原料
③制造光导纤维的主要原料是SiO2 ④制玻璃和水泥均需要石灰石作为原料
⑤硅胶可用作催化剂的载体和袋装食品的干燥剂
⑥高纯度的硅除了用于制造计算机芯片外,在太阳能发电过程中也具有重要的作用.
A.①②③⑤
B.①③④⑤
C.①③⑥
D.全部高三化学选择题中等难度题查看答案及解析
-
下列关于硅单质及其化合物的叙述正确的是( )
①硅是构成岩石和许多矿物的基本元素
②制造光导纤维的主要原料是Si
③水玻璃可用作制备木材防火剂的原料
④制玻璃和水泥均需要石灰石作为原料
⑤高纯度的硅除了用于制造计算机芯片外,在太阳能发电过程中也具有重要的作用.
⑥硅胶可用作催化剂的载体和袋装食品的抗氧化剂
A.①②③⑤ B.①③④⑤ C.①③⑥ D.全部
高三化学选择题中等难度题查看答案及解析
-
下列关于硅及其化合物的说法不正确的是( )
A.硅是构成一些岩石和矿物的基本元素
B.高纯度的硅单质可用于制作芯片
C.粗硅制备单晶硅不涉及氧化还原反应
D.二氧化硅可用来制造光导纤维高三化学选择题中等难度题查看答案及解析
-
有关硅元素的下列叙述中正确的是( )
A. 常温时硅可和强碱及强酸溶液反应
B. 硅与任何酸都不反应
C. 硅是构成矿物岩石的主要原料,其化合态硅几乎全部是硅石和硅酸盐
D. 硅的性质很稳定,能以游离态存在于自然界
高三化学选择题中等难度题查看答案及解析
-
硅是构成矿物和岩石的主要成分,单质硅及其化合物具有广泛的用途。完成下列填空:
(1)某些硅酸盐具有筛选分子的功能。一种硅酸盐的组成为:M2O·R2O3·2SiO2·nH2O,已知元素M、R均位于元素周期表的第3周期,两元素原子的质子数之和为24。
①写出M原子核外能量最高的电子的电子排布式:___________。
②常温下,不能与R单质发生反应的是_______(选填序号)。
a.CuCl2溶液 b.Fe2O3 c.浓硫酸 d.NaOH溶液 e.Na2CO3固体
(2)氮化硅(Si3N4)陶瓷材料硬度大、熔点高。可由下列反应制得:SiO2+C+N2
Si3N4+CO
①Si3N4中氮元素的化合价为-3,请解释Si3N4中氮元素化合价为负价的原因__________________。
②C3N4的结构与Si3N4相似,请比较二者熔点高低,并说明理由:______________________。
③配平上述反应的化学方程式,并标出电子转移的数目和方向。_______________。
(3)一种用工业硅(含少量铁、铜等金属的氧化物)制备Si3N4的主要流程如下:
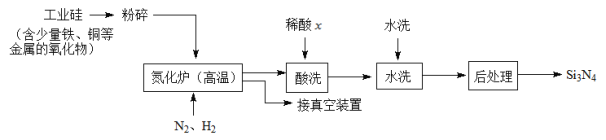
①将工业硅粉碎的目的是______________________________。
②适量的H2是为了排尽设备中的空气,但H2在高温下也能还原工业硅中的某些金属化物。
可能是______(选填:“盐酸”“硝酸”或“硫酸”),理由是_____________________。
高三化学综合题中等难度题查看答案及解析
-
硅是构成矿物和岩石的主要成分,单质硅及其化合物具有广泛的用途。完成下列填空:
I.某些硅酸盐具有筛选分子的功能,一种硅酸盐的组成为:M2O·R2O3·2SiO2·nH2O,已知元素M、R均位于元素周期表的第3周期。两元素原子的质子数之和为24。
(1)该硅酸盐中同周期元素原子半径由大到小的顺序为________________;
(2)写出M原子核外能量最高的电子的电子排布式:__________________;
(3)常温下,不能与R单质发生反应的是___________(选填序号);
a.CuCl2溶液 b.Fe2O3 c.浓硫酸 d.Na2CO3溶液
(4)写出M、R两种元素的最高价氧化物对应的水化物反应的离子方程式:____________________________________________。
II.氮化硅(Si3N4)陶瓷材料硬度大、熔点高。可由下列反应制得:SiO2+C+N2
Si3N4+CO
(5)Si3N4晶体中只有极性共价键,则氮原子的化合价为______,被还原的元素为______________。
(6)C3N4的结构与Si3N4相似。请比较二者熔点高低。并说明理由:_____________________。
(7)配平上述反应的化学方程式,并标出电子转移的数目和方向。_________________
(8)如果上述反应在10L的密闭容器中进行,一段时间后测得气体密度增加了2.8g/L,则制得的Si3N4质量为_____________。
高三化学综合题中等难度题查看答案及解析