-
电解精炼铜的阳极泥中含有大量的贵重金属和硒、碲等非金属元素。实验室从电解精炼铜的阳极泥中提取金、银、硒的流程如下:
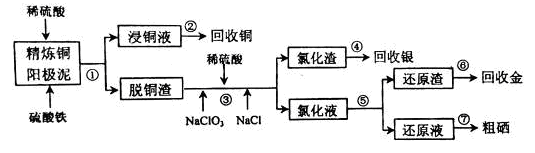
已知:单质金在酸性环境下与NaClO3、NaCl反应生成NaAuCl4;NaAuCl4可被Fe2+、SO2还原为单质金;硒的化合物不能被Fe2+还原,而能被SO2还原。
请回答下列问题:
(1)步骤①所得“浸铜液”中铜元素的存在形态为 (用化学式表示);加入稀硫酸的目的是 。
(2)写出步骤③中金元素进入“氯化液”的离子反应方程式 ;银元素进入“氯化渣”中,则其存在的形态为 (用化学式表示)。
(3)步骤⑤需在氯化液中加入适当的试剂,可选择的试剂为 (填代号)。
A.FeSO4·7H2O B.FeCl3 C.SO2 D.Na2SO3
若“氯化液”中c(AuCl4-)为0.01mol·L-1,则处理500mL该“氯化液”需消耗该物质的质量为 g。
(4)步骤②可以通过电解的方法得到单质铜,则电解时阴极的电极反应式为 ;在步骤③中,硒元素被氧化成亚硒酸,则步骤⑦制粗硒的化学反应方程式 。
-
某大型精炼铜厂,在电解铜的阳极泥中含有 3-14% Se 元素,(Se和S同主族化学性质相似)以Se单质、Cu2Se存在,还含有稀有金 属及贵金属.从阳极泥中提取Se 的流程如下:
属及贵金属.从阳极泥中提取Se 的流程如下:

已知:SeO2在773K时为气态
(1)流程②的作用 工业提取 Se 的流程中,可循环利用的物质是
(2)H2SeO3与SO2的离子反应方程式为 .
(3)上述工业提取 Se 的流程中,SeO2、H2SO4 (浓)、SO2 的氧化性由强到弱的顺序是
(4)单质硒可能成为环境污染物,可通过与浓HNO3反应生成SeO2来回收Se,Se和浓HNO3反应的还原产物为NO和NO2,且NO和NO2的物质的量之比为1:1,写出Se和浓HNO3的反应方程式: 如不对该反应还原产物的比例作限制,该反应 出现多组配平系数(填“可能”或“不可能”)
-
某大型精炼铜厂,在电解铜的阳极泥中含有 3-14% Se 元素,(Se和S同主族化学性质相似)以Se单质、Cu2Se存在,还含有稀有金属及贵金属.从阳极泥中提取Se 的流程如下:

已知:SeO2在773K时为气态
(1)流程②的作用 工业提取Se的流程中,可循环利用的物质是
(2)H2SeO3与SO2的离子反应方程式为 .
(3)上述工业提取Se的流程中,SeO2、H2SO4(浓)、SO2的氧化性由强到弱的顺序是
(4)电解铜阳极泥中Se 的质量分数的测定
称取一定量电解铜阳极泥样品以合适方法溶解,配成混酸溶液,移取一定体积上述溶液于锥形瓶中,加入KMnO4标准溶液{只发生Se(+4)转化为Se(+6),反应完全后,用Fe2+标准溶液滴至终点。通过计算可以测得电解铜阳极泥中Se的质量分数的测定。若用FeCl2溶液为Fe2+标准溶液滴至终点,对测定Se的质量分数结果是否有影响,理由是
(5)单质硒可能成为环境污染物,可通过与浓HNO3反应生成SeO2来回收Se,Se和浓HNO3反应的还原产物为NO和NO2,且NO和NO2的物质的量之比为1:1,写出Se和浓HNO3的反应方程式:______________。如不对该反应还原产物的比例作限制,该反应 出现多组配平系数(填“可能”或“不可能”)
-
电解精炼锡后的阳极泥中除含有一定量的Sn外,还含有Ag、Bi、Cu等金属,极具回收价值。某锡冶炼厂采用纯湿法工艺从阳极泥中提取Ag、Bi、Cu,流程如下:
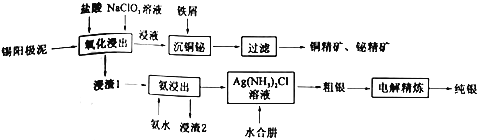
已知:①BiCl3+H2O BiOCl+2HCl
BiOCl+2HCl
②SnO2不溶于稀酸和碱溶液
(1)锡阳极泥在“氧化浸出”前需粉碎处理,目的是__________________________。
(2)“氧化浸出"时Cu发生反应的离子方程式为______________________。
(3)浸渣1的主要成分为AgCl和SnO2,则“氨浸出“时发生反应的化学方程式为______________。
(4)水合肼(N2H4·H2O)起_________作用(填“还原”或“氧化”)。已知N2H4为二元弱碱,在水中的电离与氨相似,其第一步电离的方程式为________________________。
(5)粗银电解冶炼时用_________作阳极,用_________溶液作电解液。
(6)“沉铜铋”时应将溶液的pH调至0.5~1.0之间,目的是____________________。
-
精炼铜工业中阳极泥的综合利用具有重要意义。一种从铜阳极泥(主要含有铜、银、金、少量的镍)中分离提取多种金属元素的工艺流程如下:
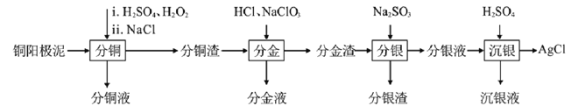
已知:ⅰ分金液中含金离子主要成分为[AuCl4]-;分金渣的主要成分为AgCl;
ⅱ分银液中含银离子主要成分为[Ag(SO3)2]3-,且存在[Ag(SO3)2]3— Ag++2SO
Ag++2SO
ⅲ“分铜”时各元素的浸出率如下表所示。

(1)由表中数据可知,Ni的金属性比Cu______。分铜渣中银元素的存在形式为(用化学用语表示)______。“分铜”时,如果反应温度过高,会有明显的放出气体现象,原因是_______。
(2)“分金”时,单质金发生反应的离子方程式为________。
(3)Na2SO3溶液中含硫微粒物质的量分数与pH的关系如图所示。
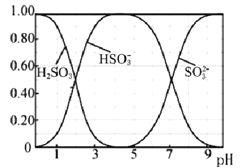
“沉银”时,需加入硫酸调节溶液的pH=4,分析能够析出AgCl的原因为_______。调节溶液的pH不能过低,理由为______(用离子方程式表示)。
(4)已知Ksp[Ag2SO4]=1.4×10-5,沉银时为了保证不析出Ag2SO4,应如何控制溶液中SO42—浓度(假定溶液中Ag+浓度为0.1mol/L)。________。
(5)工业上,用镍为阳极,电解0.1 mol/L NiCl2溶液与一定量NH4Cl组成的混合溶液,可得高纯度的球形超细镍粉。当其他条件一定时,NH4Cl的浓度对阴极电流效率及镍的成粉率的影响如图所示:
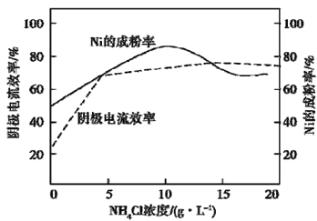
为获得髙纯度的球形超细镍粉,NH4Cl溶液的浓度最好控制为_______g/L,当NH4Cl溶液的浓度大于15g/L时,阴极有无色无味气体生成,导致阴极电流效率降低,该气体为_______。
-
Se是制光电池的一种原料。电解铜的阳极泥中含有3%-14%的Se 元素(Se元素以Se单质和Cu2Se的形式存在),还含有稀有金属及贵金属。从阳极泥中提取Se的流程如下:

请回答下列向题:
(1)浓硫酸溶解Cu2Se生成CuSO4、SO2、SeO2的化学方程式为__________________。
(2)流程②的目的是_____________________。
(3)流程④的操作名称是_____________________。
(4)SO2与SeO2(g)反应的离子方程式为________________。根据上述提取Se的工艺流程可知,SeO2、H2SO4(浓)、SO2的氧化性由强到弱的顺序是_____________。
(5)工业提取Se的流程中,可循环利用的物质是________________。(填化学式)
(6)①称取5.000g电解铜阳极泥样品。以合适方法溶解,配成250.0mL混酸溶液
②移取上述溶液25.00mL于锥形瓶中,加入30.0mL0.0100mol/LKMnO4标准溶液(Se由+4价转化为+6价)。
③反应完全后,用0.05000mol/L(NH4)2Fe(SO4)2标准溶液滴至终点,消耗(NH4)2Fe(SO4)2标准溶液10.00mL。
则电解铜阳极泥样品中Se的质量分数为__________________。若用FeCl2标准溶液代替(NH4)2Fe(SO4)2标准溶液进行滴定,对测定Se的质量分数结果__________(其“偏高”或“偏低”“ 无影响”)
-
硒(Se)、碲(Te)为VIA族元素,是当今高新技术新材料的主要成分之一,电解精炼铜的阳极泥主要成分为Cu2Te、Ag2Se和少量金属单质及其他化合物,工业上从其中回收碲、硒的一种工艺流程如下:

已知:
I.Se 单质难溶于水。TeO2微溶于水,易溶于较浓的强酸和强碱;
II.元素碲在溶液中主要以Te4+、TeO32-、HTeO3-等形式存在;
III.25℃时,亚碲酸(H2TeO3)的Ka1=1×10-3,Ka2=2×10-8。
(1)Se的氢化物的电子式是_______________。0.1mol/L的H2TeO3电离度(当弱电解质在溶液里达到电离平衡时,溶液中已经电离的电解质分子数占原来总分子数的百分数叫做电离度) 约为_____________________。
(2) 加入浓硫酸焙烧前常将阳极泥中大块颗粒先粉碎,其目的是_______________________。
(3) SeO2 与SO2在冷却后通入水中反应的化学方程式_________________________________。反应后分离出Se单质的操作①为_________________(填操作名称)。
(4)焙砂中碲以TeO2形式存在,与足量NaOH溶液反应后得到的溶液①,其溶质的主要成分为_______(填化学式,过量的NaOH除外)。工业上也可以通过电解溶液①得到单质碲。已知电解时的电极均为石墨,则阴极的电极反应式为__________________________________。
(5)向溶液①中加入硫酸时控制溶液的pH 为4.5~5.0,生成TeO2沉淀,如果H2SO4过量,将导致碲的回收率__________(填“偏高”、“偏低”或“无影响”)。
(6)将纯净的TeO2先溶于盐酸得到四氯化碲,然后再将SO2通入到溶液中得到Te单质,请写出由四氯化碲得到Te单质的离子方程式________________________________。
(7)上述流程中可循环利用的物质_______________(填化学式)。
-
硒(Se)、碲(Te)为VIA族元素,是当今高新技术新材料的主要成分之一,电解精炼铜的阳极泥主要成分为Cu2Te、Ag2Se和少量金属单质及其他化合物,工业上从其中回收碲、硒的一种工艺流程如下:

已知:
I.Se 单质难溶于水。TeO2微溶于水,易溶于较浓的强酸和强碱;
II.元素碲在溶液中主要以Te4+、TeO32-、HTeO3-等形式存在;
III.25℃时,亚碲酸(H2TeO3)的Ka1=1×10-3,Ka2=2×10-8。
(1)Se的氢化物的电子式是_______________。0.1mol/L的H2TeO3电离度(当弱电解质在溶液里达到电离平衡时,溶液中已经电离的电解质分子数占原来总分子数的百分数叫做电离度) 约为_____________________。
(2) 加入浓硫酸焙烧前常将阳极泥中大块颗粒先粉碎,其目的是_______________________。
(3) SeO2 与SO2在冷却后通入水中反应的化学方程式_________________________________。反应后分离出Se单质的操作①为_________________(填操作名称)。
(4)焙砂中碲以TeO2形式存在,与足量NaOH溶液反应后得到的溶液①,其溶质的主要成分为_______(填化学式,过量的NaOH除外)。工业上也可以通过电解溶液①得到单质碲。已知电解时的电极均为石墨,则阴极的电极反应式为__________________________________。
(5)向溶液①中加入硫酸时控制溶液的pH 为4.5~5.0,生成TeO2沉淀,如果H2SO4过量,将导致碲的回收率__________(填“偏高”、“偏低”或“无影响”)。
(6)将纯净的TeO2先溶于盐酸得到四氯化碲,然后再将SO2通入到溶液中得到Te单质,请写出由四氯化碲得到Te单质的离子方程式________________________________。
(7)上述流程中可循环利用的物质_______________(填化学式)。
-
电解精炼铜的阳极泥中含有多种贵重金属,从中提取金、银、铂的一种工艺如下:

(1)王水是 的混合液,其体积比为 。
(2)滤渣的成分是 ,反应Ⅰ中肼(N2H4)的作用是 。
(3)反应Ⅱ的离子方程式为 ;当生成19.7gAu时,25℃和101kPa下反应消耗 L SO2(此条件下的气体摩尔体积为24.5L/mol,相对原子质量Au:197)。
(4)电解法精炼银时,粗银应与直流电源的 极(填“正”或“负”)相连,当用AgNO 3 和HNO 3 混合溶液做电解质溶液时,发现阴极有少量红棕色气体,则产生该现象的电极反应式为 。
(5)金和浓硝酸反应的化学方程式为:Au+6HNO3(浓)=Au(NO3)3+3NO2↑+3H2O,但该反应的平衡常数很小,所以金和浓硝酸几乎不反应,但金却可以溶于王水,原因是 。
-
电解精炼铜的阳极泥中主要含Ag、Au等贵重金属,还含有少量 CeF4。以下是从精炼铜的阳极泥中回收银、金的流程图:
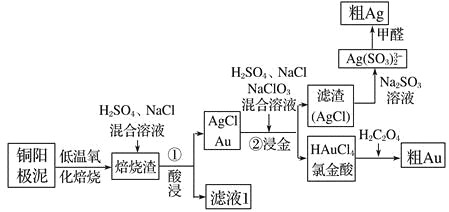
已知:①Ce 常见的化合价为+3、+4 价;②CeF4 很稳定,1000℃ 时仍不分解。
(1)①酸浸步骤中有少量黄绿色气体生成,滤液 1 中含有CeCl3,写出焙烧渣酸浸生成 CeCl3的化学方程式_________________________________________ 。
(2)铜阳极泥氧化时,采用“低温焙烧”而不采用“高温焙烧”的原因是__________
(3)“②浸金”反应中, H2SO4 的作用为_________________________,该步骤的分离操作中, 需要对所得的 AgCl 进行水洗。判断 AgCl 已经洗涤干净的方法是:取最后一次洗涤液,滴________________________试剂,出现_______现象,证明 AgCl 未洗涤干净。
(4)氯金酸(HAuCl4)在 pH 为 2~3 的条件下被草酸还原为 Au,同时放出二氧化碳气体,写出该反应方程式_____________________________________________
(5)甲醛还原法沉积银,(Ag(SO3 )2 3-)通常是在搅拌下于室温及弱碱性条件下进行,甲醛被氧化为碳酸氢根离子,则该反应的离子方程式为 _______________
(6)电解法精炼银,用 10A 的电流电解 30min,若电解效率(通过一定电量时阴极上实际沉积的金属质量与通过相同电量时理论上应沉积的金属质量之比)为 80%,此时可得到银单质的质量为__________ (保留 1 位小数,法拉第常数 96500C/mol)。












