-
(1)已知:①Fe(s)+ O2(g)=FeO(s) ∆H1=-272.0kJ/mol
O2(g)=FeO(s) ∆H1=-272.0kJ/mol
②2Al(s)+ O2(g)=Al2O3(s) ∆H1=-1675.7kJ/mol
O2(g)=Al2O3(s) ∆H1=-1675.7kJ/mol
Al和FeO发生铝热反应的热化学方程式是__________________。某同学认为,铝热反应可用于工业炼铁,你的判断是_____(填“能”或“不能”),理由是________。
(2)反应物与生成物均为气态的某可逆反应在不可条件下的反应历程分别为A、B如图所示。
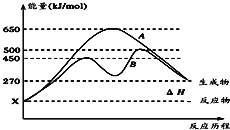
①据图判断该反应是_______(填“吸”或“放”)热反应。
②其中B历程表明此反应采用的条件为________(填字母)。
A.升高温度 B.增大反应物的浓度 C.降低温度 D.使用催化剂
(3)铝热法是常用的金属冷炼方法之一。已知:
4A1(s)+3O2(g)=2Al2O3(s) ∆H=-3352kJ/mol
Mn(s)+O2(g)=MnO2(s) ∆H=-521kJ/mol
Al与MnO2反应冶炼金属Mn的热化学方程式是___________________。
(4)中国气象局的数据显示,2013年企国平均雾霾天数为52年来之最。形成雾霾的主要成分为生产生活中排放的废气,汽车尾气及扬尘等。用CH4可以消除汽车尾气中氮氧化物的污染。
已知:CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(l) ∆H=-955kJ/mol
2NO2(g)=N2O4(g) ∆H=-56.9kJ/mol
写出CH4催化还原N2O4(g)生成N2和H2O(l)的热化学方程式________________。
-
(1)已知:下列两个热化学方程式: Fe(s) + 1/2O2(g)  FeO(s)
FeO(s)  =-272.0KJ/mol,2Al(s) + 3/2O2(g)
=-272.0KJ/mol,2Al(s) + 3/2O2(g)  Al2O3(s)
Al2O3(s)  =-1675.7KJ/mol 则 Al(s)的单质和FeO(s)反应的热化学方程式是____________________________。
=-1675.7KJ/mol 则 Al(s)的单质和FeO(s)反应的热化学方程式是____________________________。
(2)对于下列反应:2SO2 + O2  2SO3 , 如果2min内SO2的浓度由6 mol/L下降为2 mol/L,那么,用O2浓度变化来表示的反应速率为_____________。如果开始时SO2浓度为4mol/L,2min后反应达平衡,若这段时间内v(O2)为0.5mol/(L· min),那么2min时SO2的浓度为 。
2SO3 , 如果2min内SO2的浓度由6 mol/L下降为2 mol/L,那么,用O2浓度变化来表示的反应速率为_____________。如果开始时SO2浓度为4mol/L,2min后反应达平衡,若这段时间内v(O2)为0.5mol/(L· min),那么2min时SO2的浓度为 。
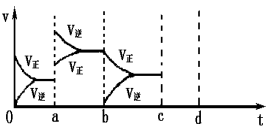
(3)如图表示在密闭容器中反应:2SO2+O2 2SO3+Q达到平衡时,由于条件改变而引起反应速度和化学
2SO3+Q达到平衡时,由于条件改变而引起反应速度和化学 平衡的变化情况,ab过程中改变的条件可能是 ;bc过程中改变的条件可能是 ;
平衡的变化情况,ab过程中改变的条件可能是 ;bc过程中改变的条件可能是 ;
(4)若增大压强时,将反应速度变化情况画在c—d处
-
已知:
2Fe(s)+O2(g) =2FeO(s) △H=-544kJ·mol-1
4Al(s)+3O2(g) =2Al2O3(s) △H=-3350kJ·mol-1
则2Al(s) +3FeO(s) =Al2O3(s) + 3Fe(s)的△H是
A.- 859 kJ·mol-1 B.+859 kJ·mol-1
C.-1403 kJ·mol-1 D.-2491 kJ·mol-1
-
以氧化铝为原料,通过碳热还原法可合成氮化铝(AlN);通过电解法可制取铝。回答下列问题:
(1)已知:2Al2O3(s)=4Al(g)+3O2(g) ΔH1=3351kJ·molˉ1
2C(s)+O2(g)=2CO(g) ΔH2=-221kJ·molˉ1
2Al(g)+N2(g)=2AlN(s) ΔH3=-318kJ·molˉ1
碳热还原Al2O3合成AlN的总热化学方程式是___。
(2)工业上用电解熔融氧化铝的方法来制取金属铝。纯净氧化铝的熔点很高(约2045℃),在实际生产中,通过加入助熔剂冰晶石(Na3AlF6)在1000℃左右就可以得到熔融体。
如图是电解槽的示意图。
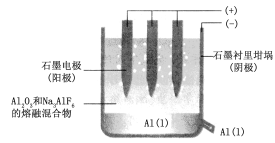
①写出电解时阳极的电极反应式:___。
②电解过程中生成的氧气全部与石墨电极反应生成CO和CO2气体。因此,需要不断补充石墨电极。工业生产中,每生产9吨铝阳极损失5.4吨石墨。每生产9吨铝转移电子的物质的量为___mol,生成的二氧化碳的物质的量为___mol。
(3)可用于电动汽车的铝—空气燃料电池,通常以NaCl溶液或NaOH溶液为电解质溶液,以铝合金为负极。
①以NaCl溶液为电解质溶液时,正极反应式为___。
②以NaOH溶液为电解质溶液时,负极反应式为___。
-
已知:2Al (s)+
 O2(g)═Al2O3(s)△H=-1 644.3kJ•mol-1
O2(g)═Al2O3(s)△H=-1 644.3kJ•mol-1
2Fe (s)+ O2(g)═Fe2O3(s)△H=-815.88kJ•mol-1
O2(g)═Fe2O3(s)△H=-815.88kJ•mol-1
试写出铝粉与氧化铁粉末发生铝热反应的热化学方程式______.
-
已知反应:Mg(OH)2=MgO(s)+H2O(g)、2Al(OH)3(s)=Al2O3(s)+H2O(g)均为吸热反应1mol Mg(OH)2分解吸热81.5kJ,1mol Al(OH)3分解吸热87.7kJ,其中,氧化镁熔点2852℃;氧化铝熔点2050℃
(1)Mg(OH)2和Al(OH)3起阻燃作用的主要原因是______.
(2)等质量Mg(OH)2和Al(OH)3相比,阻燃效果较好的是______,原因是______.
(3)常用阻燃剂主要有三类:A.卤系,如四溴乙烷(熔点0℃,沸点:243.5℃);B.磷系,如磷酸三苯酯(熔点48.5℃,沸点370℃);C.无机类,主要是Mg(OH)2和Al(OH)3.从环保的角度考虑,应用时较理想的阻燃剂是______填序号).
-
Fe2O3(s)+ C(s) ===
C(s) ===  CO2(g)+2Fe(s) ΔH1=+234.1 kJ/mol;C(s)+O2(g) === CO2(g) ΔH2=-393.5 kJ/mol;则2Fe(s)+
CO2(g)+2Fe(s) ΔH1=+234.1 kJ/mol;C(s)+O2(g) === CO2(g) ΔH2=-393.5 kJ/mol;则2Fe(s)+ O2(g) === Fe2O3(s)的ΔH是( )
O2(g) === Fe2O3(s)的ΔH是( )
A.-627.6 kJ/mol B.-824.4 kJ/mol
C.-744.7 kJ/mol D.-169.4 kJ/mol
-
Fe2O3(s)+ C(s)===
C(s)=== CO2(g)+2Fe(s) ΔH1=+234.1 kJ/mol;C(s)+O2(g)===CO2(g) ΔH2=-393.5 kJ/mol;则2Fe(s)+
CO2(g)+2Fe(s) ΔH1=+234.1 kJ/mol;C(s)+O2(g)===CO2(g) ΔH2=-393.5 kJ/mol;则2Fe(s)+ O2(g)===Fe2O3(s)的ΔH是
O2(g)===Fe2O3(s)的ΔH是
A.-627.6 kJ/mol B.-824.4 kJ/mol
C.-744.7 kJ/mol D.-169.4 kJ/mol
-
钒的化合物常用于制作催化剂和新型电池。回答下列问题:
(1)金属钒可由铝热反应制得。已知25℃、101 kPa时,
4A1(s)+3O2(g)=2Al2O3 (s) △H1=a kJ·mol-1
4V(s) +5O2 (g)=2V2O5(s) △H2=b kJ·mol-1
则用铝热反应冶炼金属V(s)的热化学方程式为_____________________。
⑵V2O5为橙黄至砖红色固体,无味、有毒,微溶于水,是许多有机和无机反应的催化剂。下图表示的是25℃时,部分含钒微粒的存在形式、浓度和存在的pH范围(其余可溶性微粒均未标出),图中“[V]”表示含钒微粒的浓度,虚线表示[V]或pH的范围尚未准确确定。
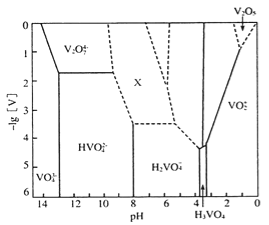
①V2O5溶于足量2mol • L-1NaOH溶液中,发生反应的离子方程式为_________________,向反应后的溶液中,滴加硫酸溶液至过量(pH<1)的过程中,开始溶液保持澄淸,滴加一段时间后,观察到有橙黄色沉淀产生,继续滴加硫酸溶液,沉淀又消失。则沉淀消失过程中发生反应的化学方程式为_______________。
②上述滴加硫酸溶液的过程中,先后发生如下反应:
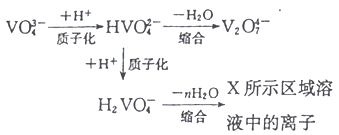
则“X所示区域溶液中的离子”不可能是___________(填序号);
a.V3O93- b.V4O103- c. V4O124-
(3)V2O5是反应2SO2+O2 2SO3的催化剂。其他条件不变,加入V2O5后,该反应的速率加快的原因是_______________;恒温恒压下,加人V2O5,该反应的平衡常数________________ (填“增大”、 “减小”或“不变”);
2SO3的催化剂。其他条件不变,加入V2O5后,该反应的速率加快的原因是_______________;恒温恒压下,加人V2O5,该反应的平衡常数________________ (填“增大”、 “减小”或“不变”);
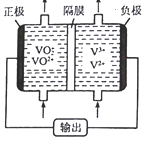
(4)下图所示为可充电的全钒液流电池构造示意图,该电池中的隔膜只允许H+通过。电池放电时,负极区溶液的pH将_____________(填“增大”、“减小”或“不变”),电池充电时,阳极的电极反应式为_____________________。
-
明矾石的主要成分是K2SO4·Al2(SO4)3·2Al2O3·6H2O,还含有杂质Fe2O3。利用明矾石来制取纯净的Al2O3、K2FeO4和H2SO4的工艺流程如图所示。

请回答下列问题:
(1)焙烧炉中发生反应的化学方程式为2Al 2(SO4) 2Al2O3+6SO2↑+3O2↑,若生成102gAl2O3,转移的电子数目为 .
2Al2O3+6SO2↑+3O2↑,若生成102gAl2O3,转移的电子数目为 .
(2)生成沉淀I的离子方程式为 ,沉淀II的化学式为 。
(3)溶液经加硫酸调节pH后,过滤,洗涤,可得沉淀I,证明沉淀I已洗涤干净的实验操作和现象是 。
(4)写出Cl2将沉淀Ⅱ氧化为K2FeO4的化学方程式: 。
(5)从滤液中得到K2SO4晶体的方法是 。
(6)K2FeO4也可以铁为电极,通过电解浓的KOH溶液来制取,写出电解法制取K2FeO4的阳极反应式:
O2(g)=FeO(s) ∆H1=-272.0kJ/mol
O2(g)=Al2O3(s) ∆H1=-1675.7kJ/mol






