-
甲、乙两池电极材料都是铁棒与碳棒(如图)。诸回答下列问题:
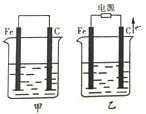
(1)若两池中均盛放CuSO4溶液,反应一段时间后:
①有红色物质析出的是:甲池中的_____棒;乙池中的____棒。
②在乙池中阳极的电极反应是____________。
(2)若两池中均盛放饱和NaCl溶液。
①写出乙池中总反应的离子方程式:___________________。
②将湿润的淀粉KI试纸放在乙池附近,发现试纸变蓝,待一段时间后又发现蓝色褪去,这是因为过量的Cl2将生成的I2氧化。若反应的Cl2和I2的物质的量之比为5:1,且生成两种酸。该反应的化学方程式为______________。
-
Ⅰ.如图所示,甲、乙两装置电极材料都是铁棒与碳棒,请回答下列问题:
(1)若两装置中均为CuSO4溶液,反应一段时间后:
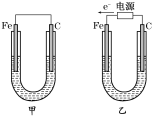
①有红色物质析出的分别是甲、乙装置中的________。
A.甲中的Fe棒,乙中的Fe棒 B.甲中的C棒,乙中的Fe棒
C. 甲中的C 棒,乙中的Fe棒 D.甲中的C棒,乙中的C棒
②乙装置中阳极的电极反应式是:____________________________________________。
(2)若两装置中均为饱和NaCl溶液:
①写出乙装置中总反应的离子方程式:_________________________________________。
②将湿润的淀粉KI试纸放在乙装置碳极附近,发现试纸变蓝,解释其原因:___________。
Ⅱ.如图为绿色电源“甲烷燃料电池”的工作原理示意图。

负极的电极反应为______________________
-
甲、乙两电池电极材料都是铁棒与碳棒,请回答下列问题:

(1)若两电池中均为CuSO4溶液,反应一段时间后:
①有红色物质析出的是甲池中的________棒,乙池中的________棒.(填“Fe”或“C”)
②乙池中的阳极反应式为:________________.
③乙池中总反应的化学方程式为:________________.
(2)若两池中均为饱和NaCl溶液,溶液中滴两滴酚酞.
①乙池中总的离子方程式为:________________.
②甲池C极上的电极反应式为:________________.
③甲池中首先出现红色的是_____极;乙池中首先出现红色的是______极(填“Fe”或“C”)
-
下图所示装置中,甲、乙、丙三个烧杯依次分别盛放足量的KI溶液、足量的CuSO4溶液和K2SO4溶液,电极均为石墨电极。接通电源,经过一段时间后,测得乙中c电极质量增加32 g。据此回答问题:
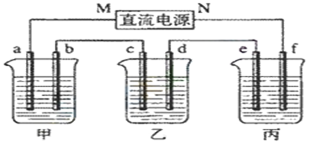
(1) 电源的N端为_________极;
(2) 电极b上发生的电极反应为____________________________________________;
(3) 电极f上生成的气体在标准状况下的体积_________________________________;
(4) 电解开始时,在甲烧杯的中央,滴几滴淀粉溶液,你能观察到的现象是______________;
(5) 电解前后溶液的pH变化情况,(填增大、减小或不变)甲溶液___________;乙溶液_____________。
-
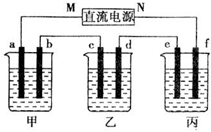
如图甲乙丙三个烧杯依次分别盛放氢氧化钠溶液、硫酸铜溶液、硫酸钾溶液,电极均为石墨电极,通电一段时间,乙中c电极质量增加64克,据此回答问题:
①电源的N端为________极;
②电极b上发生的电极反应为________;
③电极b上生成的气体在标准状况下的体积________升;
④电极e上生成的气体在标准状况下的体积________升.
-
由U形管、质量为m g的铁棒、质量为m g的碳棒和1 L 0.2 mol·L-1 CuCl2溶液组成的装置如图所示,下列说法正确的是
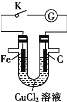
A.打开K,铁棒上有紫红色物质析出
B.闭合K,碳棒上有紫红色固体析出
C.闭合K,当电路中有0.3NA个电子通过时,理论上碳棒与铁棒的质量差为9.6 g
D.闭合K,铁棒表面发生的电极反应为Cu2++2e-=Cu
-
如图所示:甲为稀硫酸,乙为氯化铜溶液,电极材料用元素符号表示,则下列说法中正确的是

A.甲装置将电能转变为化学能
B.乙装置中左边的碳棒上有红色金属析出
C.甲中Cu为阳极
D.甲中Fe的质量少了0.56g,乙中右边的碳棒质量增加了0.64g
-
(8分)如图甲乙丙三个烧杯依次分别盛放氢氧化钠溶液、硫酸铜溶液、硫酸钾溶液,电极均为石墨电极 ,通电一段时间,乙中c电极质量增加64克,据此回答问题
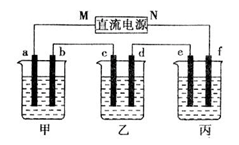
①电源的N端为 ___________极
②电极b上发生的电极反应为__________________________________
③电极b上生成的气体在标准状况下的体积______________________升
④电极e上生成的气体在标准状况下的体积_______________________升
-
(11)下图所示装置中,甲、乙、丙三个烧杯依次分别盛放100g 5.00%的NaOH溶液、足量的CuSO4溶液和100g 10.00%的K2SO4溶液,电极均为石墨电极。接通电源,经过一段时间后,测得丙中K2SO4浓度为10.47%,乙中c电极质量增加。据此回答问题:
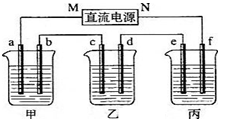
①电源的N端为________极;
②电极b上发生的电极反应为________;
③列式计算电极b上生成的气体在标准状态下的体积:________;
④电极c的质量变化是________g;
⑤电解前后各溶液的酸、碱性大小是否发生变化,简述其原因:
甲溶液________; 乙溶液________; 丙溶液________;
(2)如果电解过程中铜全部析出,此时电解能否继续进行,为什么?________。
-
下图所示装置中,甲、乙、丙三个烧杯依次分别盛放100 g 5.00%的NaOH溶液、足量的CuSO4溶液和100 g 10.00%的K2SO4溶液,电极均为石墨电极。
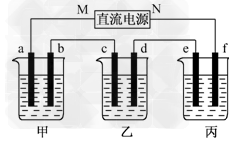
(1)接通电源,经过一段时间后,测得丙中K2SO4浓度为10.47%,乙中c电极质量增加。据此回答问题:
①电源的N端为____________________极;
②电极b上发生的电极反应为____________________;
③列式计算电极b上生成的气体在标准状况下的体积:________________;
④电极c的质量变化是__________g;
⑤电解前后各溶液的酸、碱性大小是否发生变化,简述其原因:甲溶液______________________________;乙溶液______________________________;丙溶液______________________________;
(2)如果电解过程中铜全部析出,此时电解能否继续进行,为什么? ________________________________________。










