已知:

根据以上热化学方程式判断,下列说法正确的是
A. CO的燃烧热为283kJ
B. 由题可知CO比CO2稳定
C. 
D. 与
反应放出509kJ热量时,电子转移数为
高三化学选择题中等难度题
已知:

根据以上热化学方程式判断,下列说法正确的是
A. CO的燃烧热为283kJ
B. 由题可知CO比CO2稳定
C. 
D. 与
反应放出509kJ热量时,电子转移数为
高三化学选择题中等难度题
已知:

根据以上热化学方程式判断,下列说法正确的是
A. CO的燃烧热为283kJ
B. 由题可知CO比CO2稳定
C. 
D. 与
反应放出509kJ热量时,电子转移数为
高三化学选择题中等难度题查看答案及解析
已知C2H2 (g) + O2 (g) → 2CO2 (g) + H2O (g)+1256 kJ,下列说法正确的是
A. 1 份乙炔完全燃烧可放热1256 kJ
B. 反应中乙炔做还原剂、被还原
C. 乙炔完全燃烧时,生成2 mol液态水,所放热量小于2512 kJ
D. 若有10 mol电子发生转移,则需消耗2.5 mol O2
高三化学单选题中等难度题查看答案及解析
已知热化学方程式:
①CO(g)+1/2O2(g)=CO2(g) △H= -283.0kJ/mol
②H2(g)+1/2O2(g)=H2O(g) △H= -241.8kJ/mol
据此判断下列说法正确的是
A. H2(g)+1/2O2(g)=H2O(l) △H>-241.8kJ/mol
B.H2(g)的燃烧热△H =-241.8 kJ/mol
C.H2(g)转变成H2O(g)的化学反应一定放出能量
D. CO(g)+ H2O(g)= CO2(g) + H2(g)的△H =-41.2kJ/mol
高三化学选择题中等难度题查看答案及解析
已知热化学方程式:
①CO(g)+1/2O2(g)=CO2(g) △H= -283.0kJ/mol
②H2(g)+1/2O2(g)=H2O(g) △H= -241.8kJ/mol
据此判断下列说法正确的是
A.H2(g)+1/2O2(g)=H2O(l) △H>-241.8kJ/mol
B.H2(g)的燃烧热△H =-241.8 kJ/mol
C.H2(g)转变成H2O(g)的化学反应一定放出能量
D.CO(g)+ H2O(g)= CO2(g) + H2(g)的△H =-41.2kJ/mol
高三化学选择题中等难度题查看答案及解析
根据碘与氢气反应的热化学方程式
①
②
下列判断正确的是
A.中通入
,反应放热9.48 kJ
B.1 mol固态碘与1 mol气态碘所含的能量相差17.00 kJ
C.反应①的产物比反应②的产物稳定
D.反应②的反应物总能量比反应①的反应物总能量低
高三化学选择题简单题查看答案及解析
下列说法或表示法正确的是( )
A.CO(g)的燃烧热是283.0kJ·mol-1,则表示CO(g)的燃烧热的热化学方程式为:2CO(g)+O2(g)=2CO2(g) △H=-283.0kJ·mol-1
B.当反应物的总能量比生成物的总能量高时,为吸热反应;当生成物的总能量比反应物的总能量高时,则为放热反应
C.在稀溶液中:H+(aq)+OH-(aq)=H2O(l) △H=-57.3kJ·mol-1,若将含0.5molH2SO4的浓硫酸与含lmolNaOH的溶液混合,放出的热量等于57.3kJ
D.在101kPa时,2gH2完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为2H2(g)+O2(g)=2H2O(l) △H=-571.6kJ·mol-1
高三化学单选题中等难度题查看答案及解析
下列说法或表示方法中正确的是
A.等质量的硫蒸气和硫固体分别完全燃烧,后者放出热量更多
B.由金刚石,
石墨,
可知,金刚石比石墨稳定
C.在、
时,
完全燃烧生成液态水,放出
热量,氢气燃烧的热化学方程式为
D.在稀溶液中:,若将含
的浓溶液与含
的溶液混合,放出的热量大于
高三化学单选题简单题查看答案及解析
已知: 2CO(g)+O2(g)=2CO2(g)△H=-566kJ/mol
Na2O2(s)+CO2(g)=Na2CO3(s)+O2(g)△H=-226kJ/mol
根据以上热化学方程式判断,下列说法正确的是( )
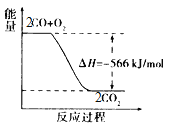
A.CO 的燃烧热为566kJ/mol
B.上图可表示由CO生成CO2的反应过程和能量关系
C.2Na2O2(s)+2CO2(s)=2Na2CO3(s)+O2(g) △H<-452 kJ/mol
D.CO2(g)与Na2O2(s)反应放出452kJ 热量时,电子转移数为1.204×1024 (个)
高三化学单选题中等难度题查看答案及解析
高三化学选择题中等难度题查看答案及解析
已知:2CO(g)+O2(g)=2CO2(g) ΔH=-566 kJ/mol
 Na2O2(s)+CO2(g)=Na2CO3(s)+
Na2O2(s)+CO2(g)=Na2CO3(s)+ ΔH=-226 kJ/mol
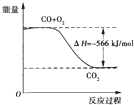
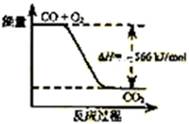
根据以上热化学方程式判断,下列说法正确的是
A.CO的燃烧热为283 kJ
B.右图可表示由CO生成CO2的反应过程和能量关系
C.2Na2O2(s)+2CO2(s)=2Na2CO3(s)+O2(g) ΔH>-452 kJ/mol
D.CO(g)与Na2O2(s)反应放出509 kJ热量时,电子转移数为6.02×1023
高三化学选择题简单题查看答案及解析