-
1 L 0.5 mol·L-1 H2SO4溶液与足量Ba(OH)2稀溶液反应放出a kJ热量;1 L 0.5 mol·L-1 HCl溶液与足量NaOH稀溶液充分反应放出b kJ热量;则500 mL 0.4 mol·L-1 BaCl2溶液与足量稀硫酸反应放出的热量为( )
A. 0.4(a+2b) kJ B. 0.4(a-2b) kJ
C. 0.2(a-2b) kJ D. 0.2(a+2b) kJ
高二化学选择题中等难度题查看答案及解析
-
下列说法或表达式正确的是( )
A. 0.5mol 稀 H2 SO 4与0.5mol 稀 Ba (OH )2溶液反应放出akJ热量,则中和热为 akJ/ mol
B.
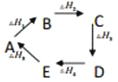 则热量变化关系式: △H1+△H3+△H5=-(△H2+△H4)
则热量变化关系式: △H1+△H3+△H5=-(△H2+△H4)C. △H与反应方程式中的化学计量数,物质的状态和可逆反应均有关
D. 同温同压下, H2( g)+ Cl 2(g)= 2HCl (g)在光照和点燃条件下的△H不同
高二化学单选题中等难度题查看答案及解析
-
下列说法或表达式正确的是( )
A. 0.5mol 稀 H2 SO 4与0.5mol 稀 Ba (OH )2溶液反应放出akJ热量,则中和热为 akJ/ mol
B.
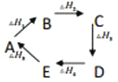 则热量变化关系式: △H1+△H3+△H5=-(△H2+△H4)
则热量变化关系式: △H1+△H3+△H5=-(△H2+△H4)C. △H与反应方程式中的化学计量数,物质的状态和可逆反应均有关
D. 同温同压下, H2( g)+ Cl 2(g)= 2HCl (g)在光照和点燃条件下的△H不同
高二化学单选题中等难度题查看答案及解析
-
下列说法正确的是( )
A.1 mol H2SO4与1 mol Ba(OH)2完全中和所放出的热量为中和热
B.强酸和强碱的稀溶液发生中和反应一定是放热反应,弱酸和弱碱反应一定也是放热反应
C.CO是不稳定的氧化物,它能继续和氧气反应生成稳定的CO2,故反应一定是吸热反应
D.酸和碱
发生中和反应生成1 mol 水,这时的反应热叫中和热
高二化学选择题中等难度题查看答案及解析
-
下列说法正确的是
A.1 mol H2SO4与1 mol Ba(OH)2完全中和所放出的热量为中和热
B.强酸和强碱的稀溶液发生中和反应一定是放热反应,弱酸和弱碱反应一定也是放热反应
C.CO是不稳定的氧化物,它能继续和氧气反应生成稳定的CO2,故反应一定是吸热反应
D.酸和碱发生中和反应生成1 mol 水,这时的反应热叫中和热
高二化学选择题中等难度题查看答案及解析
-
下列说法正确的是( )
A.在稀溶液中,1 mol H2SO4(aq)与1 mol Ba(OH)2(aq)完全中和所放出的热量为中和热
B.表明参加反应物质的量和反应热的关系的化学方程式叫做热化学方程式
C.凡是在加热或点燃条件下进行的反应都是吸热反应
D.101 kPa时,1 mol碳燃烧所放出的热量为碳的燃烧热
高二化学单选题简单题查看答案及解析
-
向足量H2SO4溶液中加入100 mL 0.4 mol·L-1 Ba(OH)2溶液,放出的热量是5.12 kJ。如果向足量Ba(OH)2溶液中加入100 mL 0.4 mol·L-1盐酸时,放出的热量为2.2 kJ。则Na2SO4溶液与BaCl2溶液反应的热化学方程式为 ( )。
A.Ba2+(aq)+SO
(aq)===BaSO4(s) ΔH=-2.92 kJ·mol-1
B.Ba2+(aq)+SO
(aq)===BaSO4(s) ΔH=-18 kJ·mol-1
C.Ba2+ (aq)+SO
(aq)===BaSO4(s) ΔH=-73 kJ·mol-1
D.Ba2+(aq)+SO
(aq)===BaSO4(s) ΔH=-0.72 kJ·mol-1
高二化学选择题中等难度题查看答案及解析
-
向足量H2SO4溶液中加入100 mL 0.4 mol·L-1 Ba(OH)2溶液,放出的热量是5.12 kJ。如果向足量Ba(OH)2溶液中加入100 mL 0.4 mol·L-1盐酸时,放出的热量为2.2 kJ。则Na2SO4溶液与BaCl2溶液反应的热化学方程式为
A.Ba2+(aq)+SO42-(aq)=BaSO4(s) ΔH=+73 kJ·mol-1
C.Ba2+(aq)+SO42-(aq)=BaSO4(s) ΔH=-73 kJ·mol-1
B.Ba2+(aq)+SO42-(aq)=BaSO4(s) ΔH=+18 kJ·mol-1
D.Ba2+(aq)+SO42-(aq)=BaSO4(s) ΔH=-18 kJ·mol-1
高二化学选择题中等难度题查看答案及解析
-
向足量H2SO4溶液中加入100 mL 0.4 mol·L-1Ba(OH)2溶液,放出的热量是5.12 kJ。如果向足量Ba(OH)2溶液中加入100 mL 0.4 mol·L-1盐酸时,放出的热量为2.2 kJ。则Na2SO4溶液与BaCl2溶液反应的热化学方程式为( )
A. Ba2+(aq)+SO42-(aq) =BaSO4(s)ΔH=-2.92 kJ·mol-1
B. Ba2+(aq)+SO42-(aq) =BaSO4(s)ΔH=-18 kJ·mol-1
C. Ba2+(aq)+SO42-(aq) =BaSO4(s)ΔH=-73 kJ·mol-1
D. Ba2+(aq)+SO42-(aq)=BaSO4(s)ΔH=-0.72 kJ·mol-1
高二化学单选题中等难度题查看答案及解析
-
向足量H2SO4溶液中加入100 mL 0.4 mol·L-1Ba(OH)2溶液,放出的热量是5.12 kJ。如果向足量Ba(OH)2溶液中加入100 mL 0.4 mol·L-1盐酸时,放出的热量为2.2 kJ。则Na2SO4溶液与BaCl2溶液反应的热化学方程式为( )
A. Ba2+(aq)+SO42-(aq) =BaSO4(s)ΔH=-2.92 kJ·mol-1
B. Ba2+(aq)+SO42-(aq) =BaSO4(s)ΔH=-18 kJ·mol-1
C. Ba2+(aq)+SO42-(aq) =BaSO4(s)ΔH=-73 kJ·mol-1
D. Ba2+(aq)+SO42-(aq)=BaSO4(s)ΔH=-0.72 kJ·mol-1
高二化学选择题中等难度题查看答案及解析