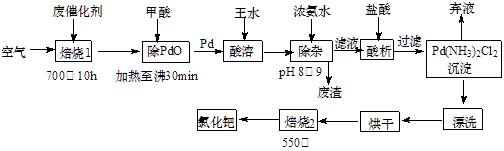-
催化剂中毒是微量杂质和催化剂活性中心的某种化学成分作用,形成没有活性的物质.CO会使合成氨的催化剂(还原铁)中毒,CO易与Fe发生反应Fe+5CO═Fe(CO)5.除去CO的化学反应方程式(HAc表示醋酸):Cu(NH3)2Ac+CO+NH3═Cu(NH3)3(CO)Ac.
请回答下列问题:
(1)C、N、O的第一电离能由小到大的顺序为______.
(2)写出基态Fe的核外电子排布式______.
(3)配合物Cu(NH3)3(CO)Ac中含有的化学键是______.
A.金属键 B.离子键 C.非极性键 D.配位键 E.氢键 F.极性键
(4)等电子体指价电子数和原子数(氢等轻原子不计在内)相同的分子、离子或基团.写出与CO互为等电子体的离子______(任写一个).
(5)在一定条件下NH3与CO能合成化肥尿素[CO(NH2)2],尿素中C原子轨道的杂化类型为______.
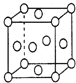
(6)铜金合金形成的晶胞如图所示.其中Cu、Au原子个数比为______,预测其熔点比铜的______(填“高”“相等”或“低”).

-
纳米材料二氧化钛(TiO2)具有很高的化学活性,可做性能优良的催化剂。工业上以金红石(主要成分是TiO2,主要杂质是SiO2)制取纳米级二氧化钛的流程如下:

| 资料卡片 |
| 物质 | 熔点 | 沸点 |
| SiCl4 | -70 ℃ | 57.6 ℃ |
| TiCl4 | -25 ℃ | 136.5 ℃ |
| | |
(1)写出氯化时生成TiCl4的化学方程式________________________。
(2)操作Ⅰ、操作Ⅱ名称分别是______________、____________。
(3)写出TiCl4水解的化学方程式________________。
(4)如在实验室中完成灼烧TiO2·xH2O放在________(填字母序号)中加热。
(5)据报道:“生态马路”是在铺设时加入一定量的TiO2,TiO2受太阳光照射后,产生的电子被空气或水中的氧获得,生成H2O2。H2O2能清除路面空气中的CxHy、CO等,其主要是利用了H2O2的________(填“氧化性”或“还原性”)。
(6)某研究小组用下列装置模拟“生态马路”的部分原理并测定CO的转化效率(夹持装置已略去)。

①B装置中的药品名称为________,若通入2.24 L(已折算成标准状况)CO气体和足量空气,最终测得装置C增重1.1 g,则CO的转化率为________。
②实验①中,当CO气体全部通入后,还要再通一会儿空气,其目的是____________。
-
合成氨是人类科学技术上的一项重大突破,是化学和技术对社会发展与进步的巨大贡献之一。在制取合成氨原料气的过程中,常混有一些杂质,如CO会使催化剂中毒。除去CO的化学反应方程式(HAc表示醋酸):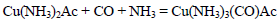
请回答下列问题:
(1)C,N,O的第一电离能由大到小的顺序为 。
(2)写出基态Cu+的核外电子排布式 。
(3)配合物Cu(NH3)3(CO)Ac中心原子的配位数为 。
(4)写出与CO互为等电子体的离子 。(任写一个)
(5)在一定条件下NH3与CO2能合成化肥尿素[CO(NH2)2],尿素中 C原子和N原子轨道的杂化类型分别为 ;1 mol尿素分子中,σ键的数目为 。
-
合成氨是人类科学技术上的一项重大突破,是化学和技术对社会发展与进步的巨大贡献之一。在制取合成氨原料气的过程中,常混有一些杂质,如CO会使催化剂中毒。除去CO的化学反应方程式(HAc表示醋酸):
Cu(NH3)2Ac + CO + NH3 = Cu(NH3)3(CO)Ac
请回答下列问题:
(1)C、N、O的第一电离能由大到小的顺序为▲ 。
(2)写出基态Cu+的核外电子排布式▲ 。
(3)配合物Cu(NH3)3(CO)Ac中心原子的配位数为▲ 。
(4)写出与CO互为等电子体的离子▲ 。(任写一个)
(5)在一定条件下NH3与CO2能合成化肥尿素[CO(NH2)2],尿素中 C原子轨道的杂化类型分别为▲ ;1 mol尿素分子中,σ键的数目为▲ 。

(6)铜金合金形成的晶胞如上图所示,其中Cu、Au原子个数比为▲ 。
-
合成氨是人类科学技术上的一项重大突破,是化学和技术对社会发展与进步的巨大贡献之一。在制取合成氨原料气的过程中,常混有一些杂质,如CO会使催化剂中毒。除去CO的化学反应方程式(HAc表示醋酸):Cu(NH3)2Ac + CO + NH3⇌Cu(NH3)3(CO)Ac。请回答下列问题:
(1)C、N、O的第一电离能由大到小的顺序为________。
(2)写出基态Cu+的核外电子排布式_______。
(3)配合物Cu(NH3)3(CO)Ac中心原子的配位数为______。
(4)写出与CO互为等电子体的阴离子______。(任写一个)
(5)在一定条件下NH3与CO2能合成化肥尿素[CO(NH2)2],1mol尿素分子中,σ键的数目为______。
(6)已知铜的晶胞结构如图所示,则在铜的晶胞中所含铜原子数及配位数比为______。
-
工业上合成氨,CO易与铁触媒作用导致铁触媒失去催化活性:Fe+5CO═Fe(CO)5。为了防止催化剂铁触媒中毒,要除去CO,发生的反应为Cu(NH3)2OOCCH3+CO+NH3═Cu(NH3)3(CO)OOCCH3。回答下列问题:
(1)下列氮原子的电子排布图表示的状态中,能量最低的是__(填字母序号)。
a.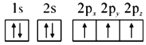 b.
b.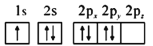
c.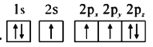 d.
d.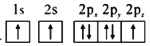
(2)写出CO的一种常见等电子体的结构式:___;C、N、O的第一电离能由大到小的顺序为__(用元素符号表示)。
(3)与O同族的元素还有S、Se、Te,它们氢化物的沸点大小为H2O>H2Te>H2Se>H2S,其原因是___。
(4)配合物[Cu(NH3)2]OOCCH3中,铜显+1价,1mol[Cu(NH3)2]+中含有σ键的数目___。则其中碳原子的杂化轨道类型是__,NH3分子的价电子对互斥理论模型是___。
(5)已知铜的一种氧化物Cu2O晶体的晶胞结构如图所示:
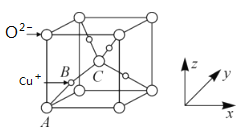
①若坐标参数A为(0,0,0),B为( ,
, ,
, ),则C的坐标参数为__;
),则C的坐标参数为__;
②若阿伏加德罗常数为NA,该晶胞的边长为apm,则晶体的密度为___g•cm-3。
-
工业上合成氨,CO易与铁触媒作用导致铁触媒失去催化活性:Fe+5CO═Fe(CO)5。为了防止催化剂铁触媒中毒,要除去CO,发生的反应为Cu(NH3)2OOCCH3+CO+NH3═Cu(NH3)3(CO)OOCCH3。回答下列问题:
(1)下列氮原子的电子排布图表示的状态中,能量最低的是______(填字母序号)。
a.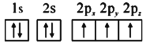 b.
b.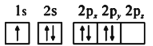
c.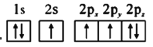 d.
d.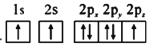
(2)写出CO的一种常见等电子体的结构式:_______;C、N、O的电负性由大到小的顺序为______(用元素符号表示)。
(3)与O同族的元素还有S、Se、Te,它们简单氢化物的沸点从高到低的顺序为______,其原因为______。
(4)配合物[Cu(NH3)2]OOCCH3中,铜显+1价, [Cu(NH3)2]+中中心离子的电子排布式为______,其中碳原子的杂化轨道类型是______,NH3分子的VSEPR模型为______。
(5)已知铜的一种氧化物Cu2O晶体的晶胞结构如图所示:
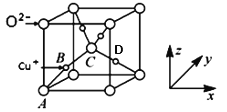
①若以A点为原点建立坐标系,A的坐标为(0,0,0),B的坐标为( ),则D的坐标为______;
),则D的坐标为______;
②若阿伏加德罗常数为NA,该晶胞的边长为a pm,则晶体的密度为______g•cm-3。
-
在制取合成氨原料气的过程中,常混有一些杂质,如CO会使催化剂中毒。除去CO的化学方程式为(HAc表示醋酸)Cu(NH3)2Ac+CO+NH3=Cu(NH3)3(CO)Ac。
请回答下列问题:
(1)化合物Cu(NH3)3(CO)Ac中,铜元素的化合价为___。
(2)该反应中含有的第二周期非金属元素的第一电离能由大到小的顺序是___。
(3)写出基态Cu2+的电子排布式:___,向Cu2+的溶液中加入过量NaOH溶液,可生成Cu2+配位数为4的配位离子,写出该配位离子的结构式___。
(4)CO与N2互为等电子体,二者沸点较高的是___,理由是____。
(5)在一定条件下,NH3和CO2能合成尿素CO(NH2)2,尿素中碳原子和氮原子的杂化轨道类型分别是:___和___。
(6)Cu与O形成的某种化合物的晶胞结构如图所示。
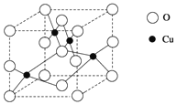
①在一个晶胞中,氧原子的数目为___。
②该化合物的化学式为____。
③晶胞的边长为apm,则该晶胞的密度为_____g•cm-3。
-
【化学——选修2:化学与技术】(15分)
有机合成中常用的钯/活性炭催化剂若长期使用,会被铁、有机化合物等杂质污染而失去活性,成为废催化剂。一种由废催化剂制取PdCl2的工艺流程如下:
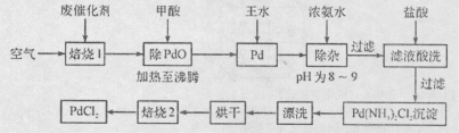
(1)“焙烧1”通入空气的目的是使有机化合物、活性炭等可燃物通过燃烧而除掉,通入空气过多反而不利于实现目的,其原因是 。
(2)甲酸在反应中被氧化为二氧化碳,写出甲酸与PdO反应的化学方程式:___ 。
(3)加浓氨水时,钯转变为可溶性[Pd(NH3)4]2+,此时铁的存在形式是 (写化学式)。
(4)加入浓氨水的过程中,需要控制溶液的pH为8~9,实验室检测溶液pH的操作方法是: 。
(5)“焙烧2”的目的是: 。
(6)与焙烧2产生的气体组成元素相同的化合物是 ,该物质与空气形成一种环保型碱性燃料电池,其负极反应式为______________________________。
(7) Pd中加入王水的反应可以表示为Pd+HCl+HNO3→A+B↑+H2O(未配平)。其中B为无色有毒气体,该气体在空气中不能稳定存在;A中含有三种元素,其中Pd元素的质量分数为42.4%,H元素的质量分数为0.8%。则A的化学式为 。
-
(12分)美日科学家因研发“有机合成中的钯催化的交叉偶联”而获得2010年度诺贝尔化学奖。有机合成常用的钯/活性炭催化剂长期使用,催化剂会被杂质(如:铁、有机物等)污染而失去活性,成为废催化剂,故需对其回收再利用。一种由废催化剂制取氯化钯(PdCl2)的工艺流程如下:
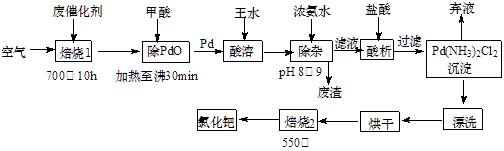
(1)甲酸在反应中的作用是 (选填:“氧化剂”或“还原剂”);
(2)加浓氨水时,钯元素转变为可溶性[Pd(NH3)4]2+,此时铁元素的存在形式是________(写化学式);
(3)王水是浓硝酸与浓盐酸按体积比1∶3混合而成的,钯在王水中溶解的过程中有化合物A和一种无色、有毒气体B生成。
① 气体B的化学式为________,
② 经测定,化合物A由3种元素组成,有关元素的质量分数为Pd:42.4%,H:0.8%。则A的化学式为________;
(4)700℃“焙烧1”的目的是,550℃“焙烧2”的目的是________。






 b.
b.
 d.
d.

 b.
b.
 d.
d.