-
I.过氧化钡常温下缓慢分解,不溶于水,常用作氧化剂、漂白剂等。请回答:
(1)BaO2的电子式为__________。
(2)BaO2在有水存在下,通过与二氧化碳作用,分解生成过氧化氢,其化学反应方程式为__________。
(3)BaCl2在氨水中与H2O2反应可得到BaO2沉淀,用一个离子反应方程式表示其原理__________。
(4)配平下列反应方程式:
( )MnO4- + ( )BaO2 + __________= ( )Ba2++( )Mn2+ + __________+( )H2O
Ⅱ、2.38g化合物甲,在空气中充分煅烧后,得固体残留物乙1.82g和标准状况下896mL气体A,该气体能使品红溶液褪色,加热后品红溶液恢复至原色。所得固体残留物乙能全部溶于稀硫酸得溶液B,能部分溶于NaOH溶液中得溶液C和0.8g残留物D。取少量溶液B,滴加KSCN溶液,发现溶液变为血红色。
请推测并回答:
(1)用离子反应方程式解释溶液变为血红色的原因:__________。
(2)写出形成溶液C的化学方程式:__________。
(3)写出气体A通入溶液B中,发生氧化还原的离子反应方程式:__________。
(4)写出化合物甲的化学式__________。
(5)有人认为:化合物甲中部分元素所形成的合金,在气体A中可逐渐形成化合物甲,试从氧化还原的角度,分析该说法的合理性:__________。
-
I.过氧化钡常温下缓慢分解,不溶于水,常用作氧化剂、漂白剂等。请回答下列问题:
(1)BaO2的电子式为 __________________。
(2)BaCl2在氨水中与H2O2反应可得到BaO2沉淀,用一个离子反应方程式表示该原理为__________________________________________。
(3)配平下列反应方程式: (____)MnO4- + ( ) BaO2+= ( ) Ba2++ ( ) Mn2++ ( ) O2+ ( ) H2O
II、化合物甲由三种元素组成,某研究性学习小组按如下流程探究其组成:

已知:气体A能使品红溶液褪色,加热后品红溶液恢复至原色。取少量溶液B,滴加KSCN溶液,发现溶液变为血红色。 请推测并回答:
(4)用离子反应方程式解释溶液变为血红色的原因:____________________________。
(5)写出形成溶液C的化学方程式:________________________________________。
(6)写出气体A通入溶液B中,发生氧化还原的离子反应方程式:_______________________。
(7)写出化合物甲的化学式______________________________。
-
二氧化氯是国际上公认的对环境无二次污染的消毒杀菌剂。它常温下为气体,易溶于水,受热易分解。甲醇法制制备二氧化氯的工艺如图:
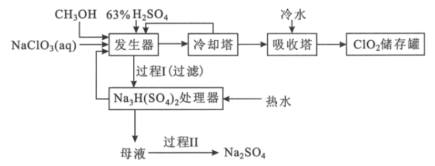
回答下列问题:
(1)ClO2可用于纸浆漂白、杀菌消毒是因其具有___性。
(2)加入“发生器”的浓硫酸先稀释为63%H2SO4,冷却后加入反应器的原因是___。实际操作中再“发生器”中加入适量NaCl以加快反应速率,若NaCl过量会发生成污染环境的一种气体的分子式为___。
(3)若1molCH3OH反应时转移6mole-,则“发生器”中发生反应的主要化学方程式为___。
(4)Na2SO4·10H2O和Na2SO4的溶解度曲线如图所示,则“过程Ⅱ”的操作是:加热浓缩至有大量晶体析出、___、经干燥得Na2SO4固体。
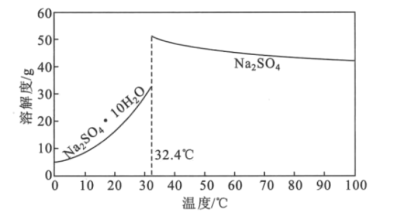
(5)采用惰性电极为阳极,通过电解亚氯酸钠溶液的方法也可以制备二氧化氯,其阳极的电极反应式为___。
(6)与甲醇法制备二氧化氯相比,电解法的优点是___(写出2点)。
-
过氧化钙是一种温和的氧化剂,常温下为白色的固体,无臭无味,能潮解,难溶于水,可与水缓慢反应;不溶于醇类、乙醚等,易与酸反应,常用作杀菌剂、防腐剂等。某实验小组拟选用如下装置(部分固定装置略)制备过氧化钙。
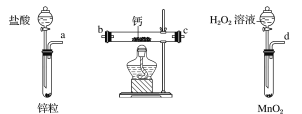
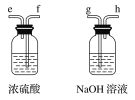
(1)请选择必要的装置,按气流方向连接顺序为_____________(填仪器接口的字母编号,装置可重复使用)。
(2)根据完整的实验装置进行实验,实验步骤如下:①检验装置的气密性后,装入药品;②打开分液漏斗活塞通入一段时间气体,加热药品;③反应结束后,_______________(填操作);④拆除装置,取出产物。
(3)一小组同学利用CaCl2在碱性条件下与H2O2反应制得。制备CaO2的实验方案和装置示意图如下:

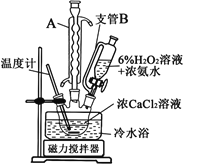
①三颈烧瓶中发生的主要反应的化学方程式为___________________________________;
②支管B的作用是_________________________;
③步骤③中洗涤CaO2·8H2O的液体X的最佳选择是____________;
A.无水乙醇 B.浓盐酸 C.水 D.CaCl2溶液
④该反应常用冰水浴控制温度在0℃左右,其可能的原因该反应是放热反应,温度低有利于提高CaO2·8H2O产率;________________________________________。
(4)测定产品中CaO2含量的实验步骤如下:
步骤一:准确称取a g产品于有塞锥形瓶中,加入适量蒸馏水和过量的b g KI晶体,再滴入少量2 mol·L-1的硫酸,充分反应。
步骤二:向上述锥形瓶中加入几滴________(作指示剂)。
步骤三:逐滴加入浓度为c mol·L-1的Na2S2O3溶液至反应完全,滴定至终点,记录数据,再重复上述操作2 次,得出三次平均消耗Na2S2O3溶液的体积为V mL。
CaO2的质量分数为________(用字母表示)。(已知:I2 + 2S2O ===2I-+ S4O
===2I-+ S4O )
)
-
过氧化钙是一种温和的氧化剂,常温下为白色的固体,无臭无味,能潮解,难溶于水,可与水缓慢反应;不溶于醇类、乙醚等,易与酸反应,常用作杀菌剂、防腐剂等。某实验小组拟选用如下装置(部分固定装置略)制备过氧化钙。
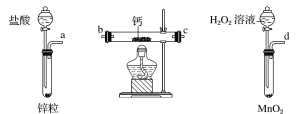
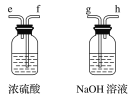
(1)请选择必要的装置,按气流方向连接顺序为_____________(填仪器接口的字母编号,装置可重复使用)。
(2)根据完整的实验装置进行实验,实验步骤如下:①检验装置的气密性后,装入药品;②打开分液漏斗活塞通入一段时间气体,加热药品;③反应结束后,_______________(填操作);④拆除装置,取出产物。
(3)一小组同学利用CaCl2在碱性条件下与H2O2反应制得。制备CaO2的实验方案和装置示意图如下:

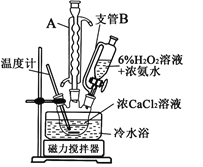
①三颈烧瓶中发生的主要反应的化学方程式为___________________________________;
②支管B的作用是_________________________;
③步骤③中洗涤CaO2·8H2O的液体X的最佳选择是____________;
A.无水乙醇 B.浓盐酸 C.水 D.CaCl2溶液
④该反应常用冰水浴控制温度在0℃左右,其可能的原因该反应是放热反应,温度低有利于提高CaO2·8H2O产率;________________________________________。
(4)测定产品中CaO2含量的实验步骤如下:
步骤一:准确称取a g产品于有塞锥形瓶中,加入适量蒸馏水和过量的b g KI晶体,再滴入少量2 mol·L-1的硫酸,充分反应。
步骤二:向上述锥形瓶中加入几滴________(作指示剂)。
步骤三:逐滴加入浓度为c mol·L-1的Na2S2O3溶液至反应完全,滴定至终点,记录数据,再重复上述操作2 次,得出三次平均消耗Na2S2O3溶液的体积为V mL。
CaO2的质量分数为________(用字母表示)。(已知:I2 + 2S2O ===2I-+ S4O
===2I-+ S4O )
)
-
过氧化钙是一种温和的氧化剂,常温下为白色的固体,无臭无味,能潮解,难溶于水,可与水缓慢反应;不溶于醇类、乙醚等,易与酸反应,常用作杀菌剂、防腐剂等。某实验小组拟选用如下装置(部分固定装置略)制备过氧化钙。
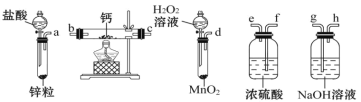
(1)请选择必要的装置,按气流方向连接顺序为_____(填仪器接口的字母编号,装置可重复使用)。
实验步骤如下:
①检验装置的气密性后,装入药品;
②打开分液漏斗活塞通入一段时间气体,加热药品;
③反应结束后,熄灭酒精灯,待反应管冷却至室温,停止通入氧气,并关闭分液漏斗的活塞;
④拆除装置,取出产物。
(2)一小组同学利用CaCl2在碱性条件下与H2O2反应制得。制备CaO2的实验方案和装置示意图如下:
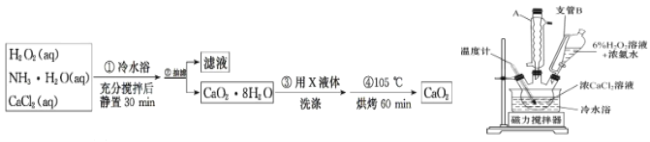
①三颈烧瓶中发生的主要反应的化学方程式为______________________________。
②支管B的作用是_____。
③步骤③中洗涤CaO2·8H2O的液体X 的最佳选择是_____;
A.无水乙醇 B.浓盐酸 C.水 D.CaCl2溶液
④该反应常用冰水浴控制温度在0℃左右,其可能的原因该反应是放热反应,温度低有利于提高CaO2·8H2O产率;_____。
(3)测定产品中CaO2 含量的实验步骤如下:
步骤一:准确称取a g 产品于有塞锥形瓶中,加入适量蒸馏水和过量的b g KI 晶体,再滴入少量2 mol·L-1的硫酸,充分反应。
步骤二:向上述锥形瓶中加入几滴_____(作指示剂)。
步骤三:逐滴加入浓度为 c mol·L-1 的 Na2S2O3 溶液至反应完全,滴定至终点,记录数据,再重复上述操作2次,得出三次平均消耗Na2S2O3 溶液的体积为V mL。CaO2的质量分数为 _________(用字母表示)。(已知:I2+ 2S2O32-=2I-+ S4O62-)
-
过氧化钙(CaO2)难溶于水,在常温下稳定,在潮湿空气及水中缓慢分解放出氧气,因而广泛应用于渔业、农业、环保等许多方面。下图是以大理石(主要杂质是氧化铁)等为原料制取过氧化钙(CaO2)的流程。
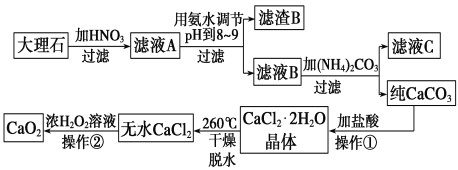
请回答下列问题:
(1)操作①应包括下列操作中的____________。(填序号)
A.溶解 B.过滤 C.蒸馏 D.分液 E.蒸发结晶
(2)用氨水调节pH至8~9的目的是_________________________________。
(3)若测得滤液C中c(CO32-)=10-3mol/L,则Ca2+____(填“是”或“不”)沉淀完全。[已知c(Ca2+)≤10-5 mol/L时即可视为沉淀完全;Ksp(CaCO3)=4.96×10-9]
(4)若在滤液C中,加入HNO3使溶液呈酸性以得到副产物NH4NO3,则酸化后溶液中c(NH4+) _______c(NO3-)(填“≥”、“≤”、“<”、“>”或“=”)。
(5)操作②是:在低温下,往过氧化氢浓溶液中投入无水氯化钙进行反应,一段时间后,再加入氢氧化钠溶液,当调节溶液pH至9~11,才出现大量沉淀。写出该反应的化学方程式_________________________;用简要的文字解释用氢氧化钠调节pH至9~11的原因____________。
(6)已知大理石含CaCO3的质量分数为a,m g大理石可以制得n g CaO2,请计算:CaCO3 转化为CaO2过程中,Ca原子的利用率__________________。
-
过氧化钙 难溶于水,在常温下稳定,在潮湿空气及水中缓慢分解放出氧气,因而广泛应用于渔业、农业、环保等许多方面。下图是以大理石
难溶于水,在常温下稳定,在潮湿空气及水中缓慢分解放出氧气,因而广泛应用于渔业、农业、环保等许多方面。下图是以大理石 主要杂质是氧化铁
主要杂质是氧化铁 等为原料制取过氧化钙
等为原料制取过氧化钙 的流程。
的流程。
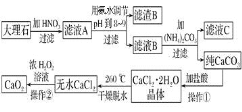
请回答下列问题:
 操作
操作 应包括下列操作中的________。
应包括下列操作中的________。 填序号
填序号
A 溶解  过滤
过滤  蒸馏
蒸馏  分液
分液  蒸发结晶
蒸发结晶
 用氨水调节pH至
用氨水调节pH至 的目的是________。
的目的是________。
 若测得滤液C中
若测得滤液C中 ,则
,则 ________
________ 填“是”或“不”
填“是”或“不” 沉淀完全。
沉淀完全。 已知
已知 时即可视为沉淀完全;
时即可视为沉淀完全;
 若在滤液C中,加入
若在滤液C中,加入 使溶液呈酸性以得到副产物
使溶液呈酸性以得到副产物 ,则酸化后溶液中
,则酸化后溶液中 ____________
____________ 填“
填“ ”、“
”、“ ”、“
”、“ ”、“
”、“ ”或“
”或“ ”
” 。
。
 操作
操作 是:在低温下,往过氧化氢浓溶液中投入无水氯化钙进行反应,一段时间后,再加入氢氧化钠溶液,当调节溶液pH至
是:在低温下,往过氧化氢浓溶液中投入无水氯化钙进行反应,一段时间后,再加入氢氧化钠溶液,当调节溶液pH至 ,才出现大量沉淀。写出该反应的化学方程式________;用简要的文字解释用氢氧化钠调节pH至
,才出现大量沉淀。写出该反应的化学方程式________;用简要的文字解释用氢氧化钠调节pH至 的原因_________。
的原因_________。
 已知大理石含
已知大理石含 的质量分数为a,
的质量分数为a, 大理石可以制得
大理石可以制得 ,请计算:
,请计算: 转化为
转化为 过程中,Ca原子的利用率________。
过程中,Ca原子的利用率________。
-
过氧化钙(CaO2)难溶于水,在常温下稳定,在潮湿空气及水中缓慢分解放出氧气,因而广泛应用于渔业、农业、环保等许多方面。下图是以大理石(主要杂质是氧化铁)等为原料制取过氧化钙(CaO2)的流程。
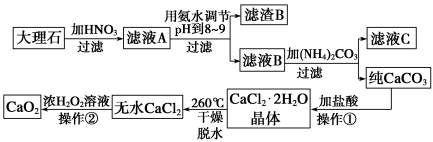
请回答下列问题:
(1)操作①应包括下列操作中的____________。(填序号)
A溶解 B过滤 C蒸馏 D分液 E蒸发结晶
(2)用氨水调节pH至8~9的目的是____________________。
(3)若测得滤液C中c(CO)=10-3 mol/L,则Ca2+________(填“是”或“不”)沉淀完全。[已知c(Ca2+)≤10-5 mol/L时即可视为沉淀完全;Ksp(CaCO3)=4.96×10-9]
(4)若在滤液C中,加入HNO3使溶液呈酸性以得到副产物NH4NO3,则酸化后溶液中c(NH)________c(NO)(填“≥”、“≤”、“<”、“>”或“=”)。
(5)操作②是:在低温下,往过氧化氢浓溶液中投入无水氯化钙进行反应,一段时间后,再加入氢氧化钠溶液,当调节溶液pH至9~11,才出现大量沉淀。写出该反应的化学方程式________;用简要的文字解释用氢氧化钠调节pH至9~11的原因_____________。
(6)已知大理石含CaCO3的质量分数为a,m g大理石可以制得n g CaO2,请计算:CaCO3 转化为CaO2过程中,Ca原子的利用率________。
-
过硫酸钠(Na2S2O8)也叫高硫酸钠、过二硫酸钠,是白色晶状粉末,易溶于水,加热至65℃就会发生分解,用作漂白剂、氧化剂、乳液聚合促进剂。某化学小组对Na2S2O8制备和性质进行探究。
I.实验室制备Na2S2O8
(查阅资料)工业制备过硫酸钠的反应原理:
主反应:(NH4)2S2O8+2NaOH Na2S2O8+2NH3↑+2H2O
Na2S2O8+2NH3↑+2H2O
副反应:2NH3+3Na2S2O8+6NaOH 6Na2SO4+6H2O+N2
6Na2SO4+6H2O+N2
设计如图实验装置:
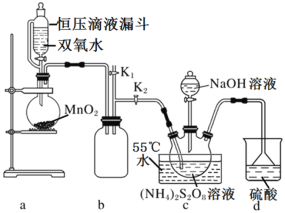
(1)恒压滴液漏斗的优点是___。
(2)装置a中反应产生的气体需要持续通入装置c的目的是___;装置b、d的作用分别是___、___。
(3)反应完毕,将三颈圆底烧瓶中的溶液减压浓缩、结晶过滤、洗涤干燥,可得过硫酸钠,减压浓缩的原因是___。
II.探究Na2S2O8的性质
(1)酸性过硫酸钠溶液,在Ag+催化作用下可以把Mn2+氧化为MnO4-,该方法可用于检验Mn2+,所得溶液除去Ag+后加入BaCl2溶液可以产生白色沉淀。
①用酸性Na2S2O8溶液检验Mn2+时的实验现象为___。
②该反应的离子方程式为____。
(2)过硫酸钠溶液与铜反应只生成两种盐且反应先慢后快,某同学推测反应先慢后快的原因可能是生成的Cu2+对反应起催化作用,设计实验方案检验该推测是否正确___。(供选择试剂:Cu、Na2S2O8溶液、Na2SO4溶液、CuSO4溶液、Cu(NO3)2溶液、CuCl2溶液、蒸馏水)
















